- Che cos’è l’acidità?
- Che cos’è il pH?
- Perché l’acidità è importante?
- Sintomi di un pH troppo basso (il substrato è troppo acido)
- Sintomi di un pH troppo alto (substrato troppo alcalino)
- Cosa determina il pH?
- Misurare il valore del pH
- Prendendo campioni
- I valori corretti di pH per ogni mezzo
- Correggere il valore del pH
Che cos’è l’acidità?
L’acidità è essenziale per la vita sulla terra. L’acidità determina spesso le caratteristiche, la qualità, l’assorbibilità e la solubilità di molte sostanze. È così che gli enzimi, che sono responsabili di quasi tutti i processi biologici negli organismi, funzionano, ma solo con la giusta acidità. Una piccola fluttuazione dell’acidità del sangue è mortale.
Che cos’è il pH?
Il pH (pondus Hydrogenii) indica l’acidità o l’alcalinità di una soluzione. Il valore del pH varia solitamente tra 0 e 14. Una soluzione con un valore di pH tra 0 e 7 è acida e una tra 7 e 14 è alcalina. L’aceto e la cola hanno un valore di pH inferiore a 3. La soda e il sapone hanno un valore pH superiore a 8. Un valore pH di 7 è considerato neutro. L’acqua pura a temperatura ambiente ha un pH di 7. Il pH dell’acqua di rubinetto è generalmente un po’ più alto a causa della presenza di calcio.
Molti ambienti naturali come la nostra pelle, i substrati delle piante e i mezzi di nutrizione sono leggermente acidi e hanno un valore di pH tra 5 e 6,5. Se guardiamo le cose che piacciono alle persone, vediamo che sono generalmente sostanze leggermente acide o neutre come l’acqua. Anche le piante preferiscono sostanze leggermente acide. Un valore di pH di circa 5,5 si verifica così spesso in natura che alcuni esperti di piante considerano questo valore come “neutro”.
Perché l’acidità è importante?
L’acidità ha un’influenza sostanziale sull’assorbibilità e la solubilità di una serie di elementi alimentari (vedi figura 1).
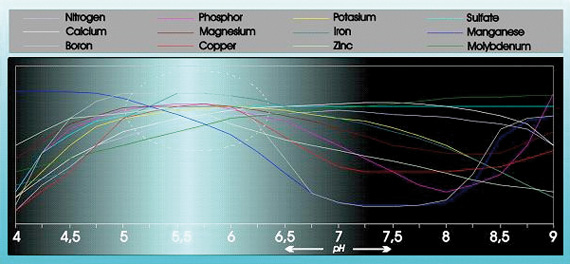
Fig. 1
Inoltre l’acidità ha una notevole influenza sulla struttura, la scomposizione delle sostanze organiche e la micro vita nel terreno. Il pH influenza anche il modo in cui gli elementi alimentari, i metalli pesanti, i pesticidi e altri microrganismi presenti nel terreno vengono espulsi dal terreno.
Un valore di pH troppo basso o troppo alto può essere dannoso per le vostre piante, quindi è importante farlo bene. Ma come si fa a sapere quando il pH è sbagliato? Per esperienza! Quindi, per aiutarvi, abbiamo elencato alcuni dei sintomi che potreste osservare:
Sintomi di un pH troppo basso (il substrato è troppo acido)
- La maggior parte dei nutrienti si scioglie facilmente, il che può causare un eccesso di manganese, alluminio e ferro;
- Le carenze di fosforo, potassio, magnesio e molibdeno possono essere causate da un risciacquo eccessivo;
- Carenza di magnesio, soprattutto nei substrati freddi;
- Il suolo è generalmente povero;
- La vita del suolo è inibita.
Sintomi di un pH troppo alto (substrato troppo alcalino)
- La maggior parte delle sostanze nutritive si scioglie meno facilmente, facendo precipitare i composti di calcio, ferro e fosfato;
- Ridotto assorbimento di manganese, fosfato e ferro in particolare ma anche di rame, zinco e boro. Questo causerà delle carenze, in particolare nei substrati di coltivazione umidi e freddi.
- Nei terreni sabbiosi la degradazione delle sostanze organiche aumenta considerevolmente se il pH è alto.
Cosa determina il pH?
Uno dei fattori più importanti che determina il valore del pH in una soluzione o nel substrato è la capacità tampone. La capacità tampone in questo caso significa che è presente una sorta di equilibrio che si ripristina continuamente. Per esempio, se si mette una goccia di acido in 1 litro di acqua di rubinetto che ha un pH di 7, avrà poca influenza sull’acidità. Tuttavia, se si mette una goccia d’acido in 1 litro d’acqua demineralizzata (acqua della batteria), il pH scenderà immediatamente in modo drammatico. Questo perché l’acqua di rubinetto contiene bicarbonato mentre l’acqua demineralizzata no. Il bicarbonato è la sostanza tampone più importante per i valori di pH tra 5,5 e 7,5 in acqua.
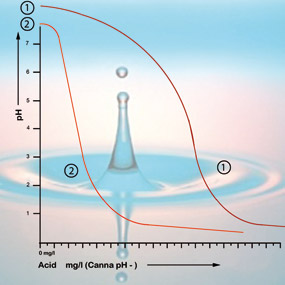 Il bicarbonato si lega all’acido nella soluzione che rilascia anidride carbonica nell’atmosfera. Questo è il modo in cui l’acido viene neutralizzato e i cambiamenti nell’acidità saranno solo minori finché c’è ancora bicarbonato presente.
Il bicarbonato si lega all’acido nella soluzione che rilascia anidride carbonica nell’atmosfera. Questo è il modo in cui l’acido viene neutralizzato e i cambiamenti nell’acidità saranno solo minori finché c’è ancora bicarbonato presente.
Con un valore di pH di 5,3 tutto il bicarbonato è stato utilizzato e la soluzione non ha più buffer. Il pH è ora instabile e cambierà immediatamente se viene aggiunto dell’acido (vedi figura 2). La quantità di acido necessaria per portare una soluzione di alimentazione all’acidità corretta può quindi essere calcolata in base al contenuto di bicarbonato. Il contenuto di bicarbonato dell’acqua di rubinetto è generalmente dato dalla società dell’acqua in milligrammi per litro.
La capacità tampone e l’acidità del substrato dipendono dalla sua composizione e freschezza. La presenza di materiale organico, di calcio e di bicarbonato determina generalmente il pH. L’argilla contiene sempre carbonato di calcio e ha un valore di pH relativamente alto che è difficile da cambiare, mentre la torba e i terreni sabbiosi sono acidi.
La pianta stessa ha anche una grande influenza sull’acidità. Le radici secernono sostanze acide o alcaline a seconda dello stadio di sviluppo della coltura, del cibo disponibile, delle differenze di temperatura delle radici e dell’intensità della luce. Così si capisce perché il pH dell’ambiente radicale può fluttuare costantemente. Un sofisticato equilibrio alimentare durante le diverse fasi di sviluppo manterrà il pH dell’ambiente radicale entro limiti accettabili.
Anche la micro-vita, i livelli di CO2 e la crescita delle alghe possono avere un effetto sull’acidità dell’ambiente radicale e del serbatoio dei nutrienti.
Misurare il valore del pH

È abbastanza facile misurare il pH – hai bisogno di alcuni indicatori di pH come le cartine tornasole o un set di test del pH. Questi sono relativamente economici ma non sono sempre accurati e possono a volte deviare da 1 a 2 unità di pH. Tutti i misuratori di pH sono generalmente più costosi e l’accuratezza dipende dal tipo di misuratore e dalla calibrazione regolare con il liquido di calibrazione.
Prendendo campioni

Il pH dell’acqua usata per irrigare le piante è importante ma l’acidità intorno alle radici è essenziale. Quindi quando si misura il pH è molto importante prendere il campione nel modo corretto per ottenere buoni risultati. Il campione ha età acidità nell’ambiente delle radici.
È facile prendere campioni e misurare il pH in un sistema di ricircolo, basta misurare la soluzione di alimentazione ricircolata.
Nei sistemi di substrato senza ricircolo, la soluzione di alimentazione viene prelevata dal substrato (lana di roccia, agrofoam, ecc.) in diversi punti. Gli esperti discutono da un anno e un giorno sulla questione di dove prelevare i campioni. Noi raccomandiamo, come fanno molti laboratori rispettabili, di prelevare campioni dai punti in cui si trovano le radici, cioè sotto e intorno al gocciolatore. Prendete piccoli campioni dal maggior numero di posti possibile. Prendete sempre tutti i campioni allo stesso tempo e preferibilmente dopo il secondo gocciolamento durante il ciclo luce – giorno – giorno.
 Nei substrati di terra, cocco e torba basta prendere una piccola quantità di substrato da diversi punti.
Nei substrati di terra, cocco e torba basta prendere una piccola quantità di substrato da diversi punti.
Potete misurare al meglio l’acidità del vostro campione usando il metodo “1:1,5 volume estratto”. Puoi farlo facilmente da solo rendendo il terreno di coltura così umido che l’acqua ti scorre tra le dita quando lo impasti e lo schiacci con forza (foto 1). Usate un becher da 250 ml, per esempio. Riempire il misurino fino a 150 ml con acqua de-mineralizzata. Aggiungere il terreno di coltura fino a raggiungere un volume di 250 ml (foto 2). Agitare bene e lasciare riposare per qualche ora. Poi filtrare e misurare il pH.

I valori corretti di pH per ogni mezzo
Quando si coltiva in substrato, valori di pH tra 5,0 e 6,4 vanno bene per l’ambiente radicale. Non ci saranno effetti negativi se i valori sono un po’ più alti o più bassi. Gli effetti negativi immediati si vedranno solo con valori inferiori a 4 e superiori a 8, un valore di pH inferiore a 4 spesso causa danni immediati alle radici. Inoltre, i metalli pesanti, tra cui il manganese e il ferro vengono assorbiti così bene che possono avvelenare la pianta (necrosi). I valori tra 7 e 8 non sono immediatamente dannosi per la pianta. Le sostanze nutritive come il ferro, il fosfato e il manganese sono meno disponibili allora, il che porterà a carenze (clorosi e problemi di sviluppo) a lungo termine.
Correggere il valore del pH
 Se l’acidità dell’ambiente radicale è tra 5 e 6,4 allora il pH del vostro ambiente di coltivazione è ok e non dovete prendere nessuna misura correttiva. Cercate di evitare di correggere il pH a meno che non sia veramente necessario. E’ più probabile che faccia più male che bene; la pianta ama la sua pace e tranquillità. E’ più importante monitorare come cambia l’acidità su un periodo più lungo. Se il valore scende al di sotto del pH 5 o sale al di sopra del pH 6,4 allora è consigliabile iniziare gradualmente a fare aggiustamenti.
Se l’acidità dell’ambiente radicale è tra 5 e 6,4 allora il pH del vostro ambiente di coltivazione è ok e non dovete prendere nessuna misura correttiva. Cercate di evitare di correggere il pH a meno che non sia veramente necessario. E’ più probabile che faccia più male che bene; la pianta ama la sua pace e tranquillità. E’ più importante monitorare come cambia l’acidità su un periodo più lungo. Se il valore scende al di sotto del pH 5 o sale al di sopra del pH 6,4 allora è consigliabile iniziare gradualmente a fare aggiustamenti.
Correggere l’acidità è più facile abbassando l’acidità della soluzione di alimentazione con acido nitrico durante la fase di crescita e acido fosforico durante la fase di fioritura o, a seconda dei casi, alzarla con potassa caustica, bicarbonato di potassio e CANNA RHIZOTONIC. Assicurarsi che il pH della soluzione utilizzata non scenda troppo al di sotto di 5,0. Quando si coltiva in lana di roccia, le fibre saranno danneggiate, causando il rilascio di molto materiale alcalino a valori di pH molto bassi. Inoltre, il pH è più difficile da controllare a causa dell’assenza di bicarbonato
Un pH elevato nell’ambiente delle radici può anche essere causato dal bicarbonato che si è accumulato. Per porvi rimedio, mantenete un drenaggio del 20% o sciacquate con una soluzione più acida.
È utile annotare le misurazioni del pH sia della soluzione aggiunta che della soluzione di alimentazione nel substrato. Avrete una buona idea della progressione del pH e dell’effetto delle misure prese.
- Gli enzimi di scissione delle proteine hanno bisogno di un ambiente acido (succhi gastrici) e gli enzimi di scissione dei carboidrati di un ambiente alcalino (saliva).
- L’acidità di una soluzione è determinata dal rapporto tra ioni idrogeno (= acido) e ioni idrossido (= alcalino). Un terreno di coltura con un pH basso ha già una grande quantità di protoni. Questi elementi vengono anche sciacquati via perché i protoni respingono le molecole del mezzo nel substrato.
- Il bicarbonato è la sostanza che, in combinazione con il calcio, è responsabile delle incrostazioni. In combinazione con il sodio, il bicarbonato è usato nei medicinali per contrastare l’eccesso di acido gastrico (Alka-seltzer).
- Alcuni laboratori lavorano anche con la durezza del bicarbonato. Per tradurlo in mg/l di bicarbonato bisogna moltiplicare la durezza del bicarbonato per 21,8.
Per esempio: la durezza del bicarbonato è 11, allora 1 litro d’acqua contiene (11 x 21.8=) 240 mg/litro di bicarbonato. -
Terreno sabbioso: Terreno erboso pH 4.6 … 5.2 Terreno edificabile pH 5.0 … 5.6 A argilla: argilla marina pH 6.0 … 7.2 argilla di fiume pH 6.2 … 6.4 Peat: non trattata pH 4.0 - Se c’è una crescita significativa delle alghe, il pH aumenterà perché l’anidride carbonica sarà rimossa dalla soluzione. I batteri possono trasformare alcune forme di azoto in modo da avere un effetto acidificante. Grandi quantità di CO2 nell’aria generano più anidride carbonica nella soluzione di alimentazione e viceversa.
- Utilizzare solo soda in piccole quantità, perché contiene sodio, e le piante hanno bisogno solo di una quantità molto piccola di sodio. Ricordate, alte concentrazioni di sodio danneggiano la pianta.
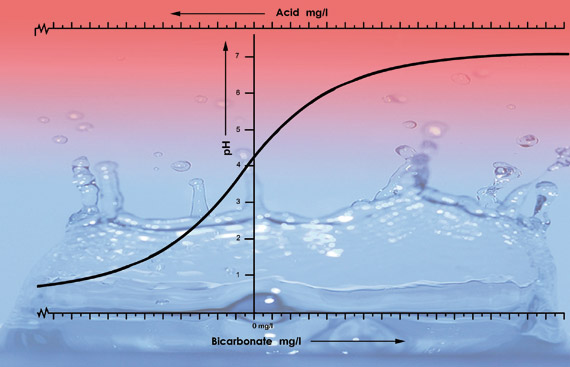
Illustrazione dei valori di pH dell’acqua di rubinetto di varie zone con diversi livelli di bicarbonato. Abbiamo aggiunto 33 ml di acido nitrico (38%) ad ogni campione di 100 litri di ogni tipo di acqua. La curva del pH scende più velocemente dopo il pH 5.3 perché per questo tipo di acqua l’acido neutralizza tutto il bicarbonato. Al di sotto del pH 5,3 il livello di acidità accelera rapidamente.
Nei sistemi a ricircolo, il valore del pH può fluttuare più che nei sistemi “run-to-waste”. Lo stesso vale per il valore EC, ppm. Se volete saperne di più su EC, pH e ppm, vi consigliamo di leggere il nostro articolo Tutto su EC, pH e ppm usando AQUA.