Diabetes mellitus je nákladný, ale většina nákladů připadá na komplikace a nemocniční péči.1 Podle Americké diabetologické asociace (ADA) činily v roce 2012 celkové odhadované náklady na diabetes 245 miliard dolarů.1 Odhaduje se, že 43 % připadá na náklady na hospitalizaci a dalších 18 % na recepty na léčbu komplikací diabetu.1
Většině těchto komplikací lze předcházet cílenou kontrolou glykémie. Epidemiologické údaje ukazují, že na každý procentní bod poklesu hemoglobinu A1c (HbA1c) připadá 35% snížení rizika mikrovaskulárních komplikací.2 Dobrou zprávou je, že se podařilo snížit výskyt komplikací u diabetu,3 ale to bylo překonáno samotným nárůstem počtu lidí s diabetem, u kterých dochází k progresi komplikací.
Mnoho lidí s diabetem 2. typu může mít v době diagnózy komplikace související s diabetem. Jak u diabetu 1., tak u diabetu 2. typu jsou některé komplikace, například retinopatie a nefropatie, němé. To vyžaduje agresivní cílený přístup, protože čekat na příznaky bude pozdě. Dokonce i diabetická neuropatie bude až u 50 % lidí s měřitelnými abnormalitami asymptomatická.4
Tento článek se bude zabývat přehledem doporučení ze Standardů péče ADA 2017 pro mikrovaskulární komplikace a příslušných stanovisek a zdůrazní preventivní screening a klinické perly pro lékaře primární péče ošetřující pacienty s diabetem.
- Diabetická retinopatie
- Tabulka 1. Stupně retinopatie s popisem
- Klinické perly
- Diabetické onemocnění ledvin
- Tabulka 2. Vybrané přelomové studie prokazující kontrolu glykémie s A1c pod 7 %
- Tabulka 3. Odhadovaná GFR se stadiem a popisem
- Tabulka 4. Kategorie albuminurie u CKD
- Obr. 1. Navrhovaná četnost hodnocení (početkrát za rok) podle kategorie eGFR a albuminurie
- Tabulka 5. Červené příznaky nasvědčující nediabetickému glomerulárnímu onemocnění
- Tabulka 6. Úpravy dávek a doporučení pro látky snižující hladinu glukózy u pacientů s poruchou funkce ledvin
- Třída
- Léčba
- Klinické perly
- Diabetická periferní neuropatie
- Tabulka 7. Další příčiny neuropatie67
- Tabulka 8. Běžně používané farmakologické přípravky pro DPN4,69
- Klinické perly
- Gastroparéza
- Klinické perly
- Diabetická cheiroartropatie
- Závěr
Diabetická retinopatie
Diabetická retinopatie je častou mikrovaskulární komplikací diabetu 1. a 2. typu. Odhaduje se, že 3,7 milionu lidí na světě má kvůli diabetické retinopatii středně těžké až těžké poškození zraku a více než 800 000 lidí na světě je kvůli diabetické retinopatii slepých.5 Jedná se o nejčastější příčinu nově vzniklé slepoty u dospělých ve věku 20-74 let.6 Byla zjištěna silná závislost na kontrole glykémie, kontrole krevního tlaku a délce trvání onemocnění. Díky včasnému a pravidelnému screeningu a kontrole těchto rizikových faktorů lze diabetickou retinopatii odhalit a léčit a zabránit tak poškození zraku.
Délka trvání diabetu je největším rizikovým faktorem pro progresi diabetické retinopatie. U diabetu 1. typu je retinopatie vzácná v prvních 3-5 letech nebo před pubertou.7 V následujících 20 letech se diabetická retinopatie vyvine téměř u všech pacientů s diabetem 1. typu.7 U pacientů s diabetem 2. typu má v době diagnózy určitý stupeň retinopatie až 21 % pacientů.7 Chronická hyperglykémie, nefropatie, hypertenze a dyslipidémie jsou dalšími faktory, které zvyšují riziko vzniku diabetické retinopatie nebo jsou s ní spojeny.8 Až 50 % pacientů s albuminurií (bez ohledu na odhadovanou úroveň glomerulární filtrace) bude mít retinopatii.9 Tabulka 1 popisuje jednotlivá stadia retinopatie.
Tabulka 1. Stupně retinopatie s popisem |
|
|
Stupeň |
Popis |
|
Mírný Ne-.Proliferativní diabetická retinopatie |
Mikroaneuryzmata přítomna |
|
Středně těžká neproliferativní diabetická retinopatie |
Mikroaneuryzmata, tečkovité nebo skvrnité krvácení do sítnice, tvrdé exsudáty, nebo vatové skvrny mohou být přítomny |
|
Těžká neproliferativní diabetická retinopatie |
Intraretinální krvácení, žilní korálky, nebo intraretinální mikrovaskulární abnormality mohou být přítomny |
|
Proliferativní diabetická retinopatie |
Neovaskularizace, přítomno sklivcové nebo preretinální krvácení |
Patofyziologie. Mírné neproliferativní abnormality charakterizované zvýšenou cévní propustností mohou progredovat do středně závažné až závažné neproliferativní diabetické retinopatie (NPDR).7 Proliferativní diabetická retinopatie je charakterizována proliferací nových retinálních cév.7 Makulární edém, což je centrální ztluštění sítnice s exsudací a edémem, se může objevit v kterémkoli stadiu retinopatie.7 Diabetickou retinopatii může urychlit těhotenství, puberta, nedostatečná kontrola glykémie, hypertenze a operace katarakty.7
Prevence diabetické retinopatie. Kontrola glykémie je klíčem k prevenci diabetické retinopatie. Ve studii DCCT (Diabetes Control and Complications Trial) vědci hodnotili vliv přísné kontroly glykémie a progrese od žádné nebo minimální retinopatie na počátku až po středně těžkou NPDR.10 U pacientů ve skupině s intenzivní léčbou bez retinopatie na počátku se průměrné riziko retinopatie snížilo o 76 % za 36 měsíců.10 U pacientů ve skupině s intenzivní léčbou, kteří již měli minimální až středně těžkou NPDR, bylo riziko progrese sníženo o 54 % oproti pacientům užívajícím konvenční léčbu.10 V původní studii Action to Control Cardiovascular Risk in Diabetes (ACCORD) byli účastníci s diabetem 2. typu po dobu 10 let a známým kardiovaskulárním onemocněním randomizováni k intenzivní nebo standardní léčbě glykémie, systolického krevního tlaku a dyslipidémie. Po čtyřech letech se progrese retinopatie snížila u osob s předchozí intenzivní kontrolou glykémie bez ohledu na podobné aktuální hladiny HbA1c.11 Podobný efekt dědictví nebyl pozorován u skupin s intenzivní kontrolou krevního tlaku nebo na fenofibrátu pro dyslipidémii.11
Vyšetření. Vzhledem k tomu, že makulární edém a proliferativní diabetická retinopatie mohou být asymptomatické, je screening nezbytný pro včasné odhalení a léčbu. U pacientů s diabetem 1. typu by měl být screening zahájen pět let po stanovení diagnózy.8 U pacientů s diabetem 2. typu by měl být screening zahájen při stanovení diagnózy.8 Screening by měl provádět oftalmolog nebo optometrista, který má zkušenosti s diabetickou retinopatií. Screening by měl být prováděn s rozšířenýma očima. Pokud je již retinopatie přítomna, doporučuje se odeslání k oftalmologovi.8 Opakované hodnocení by mělo být prováděno každoročně, pokud je zjištěno minimální nebo žádné onemocnění.8
Těhotenství je vysoce rizikovým obdobím pro proliferativní retinopatii. U těhotných žen s preexistujícím diabetem 1. nebo 2. typu by mělo být oční vyšetření provedeno před početím nebo v prvním trimestru. Vyšetření by se měla opakovat každý trimestr a po dobu jednoho roku po porodu.8 U osob s gestačním diabetem nejsou po porodu nutná žádná další oční vyšetření.
Těhotenství u pacientek s preexistujícím diabetem 1. nebo 2. typu může vést k rychlé progresi diabetické retinopatie. To platí zejména v případě špatné kontroly glykémie v době početí.14 Ženy s diabetem, které jsou těhotné nebo plánují otěhotnět, by měly být poučeny o riziku vzniku nebo progrese diabetické retinopatie a o nutnosti kontroly glykémie před početím.8 Při rychlém zavedení intenzivní glykemické léčby však může dojít k časnému zhoršení retinopatie, pokud je již retinopatie přítomna.8 Gestační diabetes zřejmě nepřináší stejné riziko vzniku diabetické retinopatie během těhotenství.8
Léčba. Bylo prokázáno, že kromě kontroly glykémie snižuje progresi diabetické retinopatie také kontrola krevního tlaku (< 140 mmHg systolického), avšak přísná kontrola systolického krevního tlaku < 120 mmHg nepřináší žádný další benefit.12 Fenofibrát může rovněž zpomalit progresi diabetické retinopatie, zejména při velmi mírné NPDR, u pacientů s dyslipidémií.13 Bylo prokázáno, že aspirin nemá žádný vliv na progresi retinopatie, rozvoj sklivcového krvácení ani na délku trvání sklivcového krvácení a lze jej bezpečně používat i v jiných léčebných indikacích, aniž by došlo k ohrožení očí.7
Léčba pacientů s diabetem by měla zahrnovat doporučení pro cvičení. Osoby s mírnou neproliferativní retinopatií mohou bezpečně zahájit fyzickou aktivitu. Pacienti se středně těžkou neproliferativní retinopatií by se však měli vyvarovat aktivit, které výrazně zvyšují krevní tlak, jako je například posilování.15 Pacienti s těžkou neproliferativní nebo nestabilní retinopatií by se měli vyvarovat jakékoli fyzické aktivity, která je energická (skákání, otřesy), jakýchkoli aktivit se skloněnou hlavou a zadržování dechu.15
V případě krvácení do sklivce by se nemělo cvičit.15
Včasné odhalení diabetické retinopatie je důležité, protože léčba může zabránit nebo zvrátit ztrátu zraku. Ve studii Diabetic Retinopathy Study (DRS) vědci zjistili, že účinnou léčbou diabetické retinopatie je fotokoagulační operace. Studie Early Treatment Diabetic Retinopathy a DRS ukázaly, že fotokoagulace snižuje riziko ztráty zraku, přičemž největší přínos měla u pacientů, kteří měli pokročilejší základní onemocnění.16,17 Současné údaje poskytují důkazy, že intravitreální přípravky s antivaskulárním endoteliálním růstovým faktorem (anti-VEGF) jsou v léčbě makulárního edému účinnější než monoterapie nebo kombinovaná léčba s laserovou koagulací.8 Anti-VEGF navíc může zlepšit vidění, zatímco fotokoagulace pouze zabraňuje další ztrátě zraku.18,19 Jednou z nevýhod anti-VEGF je, že vyžaduje měsíční intravitreální léčbu během prvních 12 měsíců.
Klinické perly
- Neexistují žádné specifické známky nebo příznaky časné diabetické retinopatie.
- Screening diabetické retinopatie by měl probíhat u pacientů:
– s diabetem 1. typu pět let po stanovení diagnózy.
– u pacientů s diabetem 2. typu při stanovení diagnózy.
- Poradenství a zvýšená vyšetření by měla být poskytnuta diabetičkám, které plánují otěhotnět nebo otěhotní, protože diabetická retinopatie se může během těhotenství rychle urychlit.
- Přísná kontrola glykémie a kontrola krevního tlaku (< 140 mmHg systolického) může zabránit rozvoji diabetické retinopatie.
- Až 50 % pacientů s albuminurií (bez ohledu na úroveň eGFR) bude mít retinopatii.9
- Léčba fotokoagulací může zabránit progresi onemocnění a léčba anti-VEGF může zvrátit ztrátu zraku způsobenou makulárním edémem.
Diabetické onemocnění ledvin
Diabetické onemocnění ledvin (DKD), preferovaná terminologie ADA, je hlavní příčinou chronického onemocnění ledvin (CKD) ve Spojených státech.20,21 DKD má významné dlouhodobé dopady na kvalitu života pacientů s diabetem a je zodpovědná až za 40 % případů konečného stadia onemocnění ledvin (ESRD).20 Na základě iniciativy National Kidney Foundation’s Kidney Disease Outcomes Quality Initiative (KDOQI) a standardů péče ADA z roku 2017 poskytne tato část pokyny týkající se cílových hladin HbA1c, medikace a terapeutické léčby pacientů s DKD.
KDOQI stratifikuje cílové hladiny HbA1c podle rizika hypoglykémie a komorbidit pacienta. Tato iniciativa vychází ze tří publikací, které prokazují, že kontrola glykémie s HbA1c pod 7 % zabrání nebo sníží progresi onemocnění ledvin u pacientů s diabetem 2. typu.22,23,24 Tyto studie jsou shrnuty v tabulce 2. ADA doporučuje u pacientů s vyšším rizikem hypoglykémie zvýšit cílový HbA1c nad 7 %.8 KDOQI doporučuje pacientům s CKD 4. a 5. stupně, kteří mají omezenou očekávanou délku života, udržovat HbA1c vyšší než 7 %.25
Tabulka 2. Vybrané přelomové studie prokazující kontrolu glykémie s A1c pod 7 % |
|
|
Trial |
Results |
|
Action in Diabetes and Vascular Disease: Preterax and Diamicron Modified Release Controlled Evaluation (ADVANCE) Trial22 |
21% snížení nové makroalbuminurie a náhradní léčby ledvin při A1c pod 7% |
|
Veterans Affairs Diabetes Trial (VADT)23 |
37% snížení makroalbuminurie a 32% snížení mikroalbuminurie při A1c pod 7% |
|
Studie ACCORD (Action to Control Cardiovascular Risk in Diabetes)24 |
2% snížení makroalbuminurie a 21% snížení mikroalbuminurie při A1c pod 7% |
Epidemiologie. Muži a ženy jsou DKD postiženi stejně.20 Vrchol výskytu rozvoje DKD je 15 let po stanovení diagnózy.21 Afroameričané mají třikrát až pětkrát vyšší pravděpodobnost rozvoje diabetické nefropatie než běloši.20 Vyšší riziko rozvoje DKD mají také Mexičané a indiáni kmene Pima.20
Proteinurie je prediktorem kardiovaskulární morbidity a mortality ze všech příčin u diabetu.21 Přítomnost DKD je faktorem zvýšeného rizika kardiovaskulárních onemocnění. Pacienti s DKD se trvale potýkají s vyšší úmrtností na kardiovaskulární onemocnění.26 Kromě toho je u pacientů s DKD vyšší úmrtnost ze všech příčin.21
U diabetu 1. typu se mikrovaskulární komplikace, jako je DKD, začínají rozvíjet přibližně 10-20 let po stanovení diagnózy; u diabetu 2. typu často není znám přesný začátek, a proto je nutné provést screening dříve.27
Patofyziologie a patogeneze. Předpokládá se, že hyperglykémie vyvolává tři hlavní histologické změny na glomerulech, které vedou k DKD: 1) expanzi mezangia, 2) ztluštění glomerulární bazální membrány a 3) glomerulární sklerózu.28 Ačkoli přesná patogeneze, proč k DKD dochází, není známa, předpokládá se, že hyperglykémie zpočátku způsobuje hyperfiltraci a poškození ledvin v důsledku histologických změn a aktivace cytokinů.20 Typicky může být prvním příznakem DKD albuminurie.29
To se dále zhoršuje v důsledku komorbidních stavů hyperlipidemie, arteriosklerózy, hypertenze a obezity, které přispívají k poškození ledvin a následnému zhoršení funkce. Centrální obezita vede k hypertenzi prostřednictvím hyperaktivace systému renin-angiotenzin-aldosteron a sympatického nervového systému.20 Dále s arteriosklerotickým postižením renálního cévního řečiště dochází ke zvýšené progresi diabetické nefropatie. Důležitým rozlišovacím znakem diabetické nefropatie ve srovnání s jinými formami CKD je, že glomeruly a ledviny jsou obvykle zpočátku normální nebo zvětšené.20
Klasifikace. Ke stanovení stadia CKD se používá jak eGFR, tak přítomnost albuminurie.30,31 eGFR vychází z rasy, věku, pohlaví, hmotnosti a hladiny sérového kreatininu. (Viz tabulka 3.) Historicky se pro definici mírně zvýšené hladiny albuminu používal termín mikroalbuminurie. National Kidney Foundation nyní doporučuje používat termíny „mírná“, „středně zvýšená“ nebo „silně zvýšená“ k popisu úrovně albuminurie na základě hodnot znázorněných v tabulce 4.31 Poměr albuminu ke kreatininu je výchozím testem používaným ke zjištění albuminurie.
Tabulka 3. Odhadovaná GFR se stadiem a popisem |
|||
|
Stadium |
GFR (ml/min na 1.73 m2) |
Popis |
|
|
90+ |
Glomerulární hyperfiltrace |
||
|
Mírně snížená funkce ledvin |
|||
|
3A |
Středně snížená funkce ledvin |
||
|
3B |
|||
|
Silně snížená funkce ledvin |
|||
|
< 15 nebo na dialýze |
Konec-stádium selhání ledvin |
||
Tabulka 4. Kategorie albuminurie u CKD |
||
|
Kategorie |
Albumin-to-Hladina kreatininu |
Popis |
|
A1 |
< 30 |
Normální až mírně zvýšené |
|
A2 |
Mírně zvýšená |
|
|
A3 |
> 300 |
Silně zvýšená |
Dvě klasifikační schémata představují dvojí cestu k rozvoji CKD. Jedna vede přes zvýšení kreatininu a zhoršení GFR. Druhá je prostřednictvím rozvoje albuminurie. Zvyšující se albuminurii často následuje pokles eGFR;32 tomu však lze předejít užíváním inhibitorů angiotenzin konvertujícího enzymu (ACE) nebo blokátorů angiotenzinových receptorů (ARB) a kontrolou glykémie. (Viz obrázek 1.)
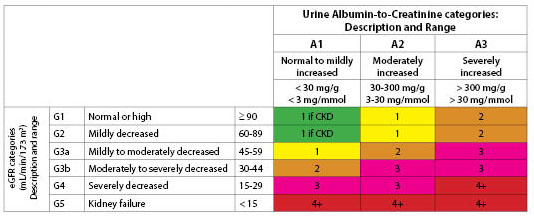
Přetištěno se souhlasem Kidney Disease: Improving Global Outcomes (KDIGO).
Obvyklé příznaky. Většina lidí nemá žádné příznaky diabetické nefropatie. Často mohou mít pacienti známky nebo diagnózu jiných mikrovaskulárních komplikací.20 Časná DKD je obvykle asymptomatická. Pozdním nálezem DKD je zpěněná moč. Pokud má pacient závažnou hypoalbuminémii, může se navíc projevovat otoky nohou a únavou.20 Pacienti s DKD mají obvykle systémovou hypertenzi. U pacientů s diabetickou nefropatií se obvykle vyskytuje také retinopatie a neuropatie.8
Diagnostické možnosti. Vzhledem k tomu, že se nevyskytují žádné příznaky, je rutinní screening kriticky důležitý. ADA doporučuje každoroční screeningové vyšetření poměru albuminu ke kreatininu v moči.8 Kromě toho by měla být alespoň jednou ročně vyšetřena eGFR u pacientů s diabetem 1. typu trvajícím pět let a u všech pacientů s diabetem 2. typu nebo u pacientů s komorbidní hypertenzí a diabetem.8 Neexistuje žádné jasné doporučení pro získání zobrazovacích vyšetření, jako je ultrazvuk, pro diagnostiku DKD.
Diferenciální diagnostika. Některé červené příznaky mohou naznačovat, že diabetes není jedinou příčinou CKD. Pokud má osoba pokročilou CKD bez průkazu jiných mikrovaskulárních komplikací, je to varování. Overtní proteinurie s náhlým výskytem (méně než pět let po začátku diabetu) močového sedimentu s dysmorfními červenými krvinkami a odlitky nebo náhlý pokles GFR naznačují onemocnění ledvin nediabetické etiologie.20 Pokud existuje obava z mnohočetného myelomu, lze provést elektroforézu séra nebo moči. Nepřítomnost albuminurie při snížené eGFR a diabetu vyžaduje vyšetření na jiné příčiny CKD než DKD.21 V tabulce 5 jsou uvedeny červené vlajky, které naznačují nediabetické onemocnění glomerulů.
Tabulka 5. Červené příznaky nasvědčující nediabetickému glomerulárnímu onemocnění
- Přítomnost proteinurie <5 let od dokumentovaného začátku diabetu 1. typu nebo akutního začátku onemocnění ledvin
- Akutní pokles eGFR; diabetická nefropatie
- Močový sediment obsahující dysmorfní červené krvinky nebo buněčné odlitky
- Přítomnost dalších mikrovaskulárních komplikací, jako je neuropatie nebo retinopatie
- Známky a/nebo příznaky jiného systémového onemocnění
Léčba. Charakteristickým znakem diabetické nefropatie je léčba glukózy, snížení soli, krevního tlaku a dyslipidemie. Dále by se pacienti měli vyvarovat nefrotoxických léků a doplňků stravy, jako jsou aminoglykosidy a nesteroidní protizánětlivé léky. Pacienti by měli být odesláni k nefrologovi ve stadiu IV onemocnění ledvin nebo v případě, že dojde k rychlému poklesu funkce ledvin. Další indikace k odeslání závisí na složitosti případu. Novější perorální léky na diabetes mohou pomoci zabránit progresi selhání ledvin.
Kontrola glykémie. U pacientů s diabetickou nefropatií jsou ovlivněny výběr léků, monitorování a farmakologie. S poklesem eGFR pacienta budou některé perorální přípravky vyžadovat úpravu dávky. Hlavní terapií pro kontrolu glykémie u pacientů s diabetem a pokročilým CKD zůstává inzulin.31 Tabulka 6 uvádí doporučené úpravy dávek antiglykemických léků u pacientů s onemocněním ledvin. V roce 2016 bylo prokázáno, že empagliflozin i kanagliflozin snižují progresi CKD a mikroalbuminurii.33,34 Empagliflozin snížil míru progrese nefropatie a snížil riziko závažných nežádoucích kardiovaskulárních příhod ve srovnání s placebem, když byl přidán ke standardní péči o diabetiky 2. typu ve stěžejní výsledkové studii Empagliflozin Cardiovascular Outcome Event Trial in Type 2 Diabetes Mellitus Patients (EMPA-REG).33
Tabulka 6. Úpravy dávek a doporučení pro látky snižující hladinu glukózy u pacientů s poruchou funkce ledvin |
||
|
Glukózo-.snižující hladinu glukózy |
Úprava dávkování u pacientů s poruchou funkce ledvin |
|
Třída |
Léčba |
|
|
Biguanidy |
Metformin |
eGFR 30 až 45 ml/min/1.73 m2: Nedoporučuje se zahájit léčbu. Pokud je po zahájení léčby nutné posoudit přínosy/rizika pokračování léčby. eGFR < 30 ml/min/1,73 m2: Použití je kontraindikováno |
|
Sulfonylurey |
Glimepirid |
Mírné až středně těžké postižení: Těžká porucha: Zahajte léčbu dávkou 1 mg jednou denně Těžká porucha: Užití je kontraindikováno |
|
Glipizid |
Prodloužené uvolňování: Zahájení: 2,5 mg jednou denně |
|
|
Glyburid |
eGFR < 60 ml/min/1,73 m2: Použití se nedoporučuje |
|
|
Meglitinidy |
Nateglinid |
Ne nutná úprava dávkování |
|
Repaglinid |
CrCl 20 až 40 ml/min: Zahájení při 0.5 mg při jídle CrCl < 20 ml/min: Žádné informace |
|
|
Tiazolidindiony |
Pioglitazon |
Není třeba upravovat dávkování nutné |
|
Rosiglitazon |
Není nutná úprava dávkování |
|
|
α-Inhibitory glukosidázy |
Akarbóza |
SCr > 2.0 mg/dl: Použití se nedoporučuje |
|
Miglitol |
CrCl < 25 ml/min nebo SCr >2.0 mg/dl: Použití se nedoporučuje |
|
|
Inhibitory DPP-4 |
Alogliptin |
CrCl 30 až 60 mL/min: 12.5 mg jednou denně CrCl < 30 ml/min: 6,25 mg jednou denně ESRD vyžadující hemodialýzu: 6.25 mg jednou denně a podávat bez ohledu na načasování hemodialýzy |
|
Linagliptin |
Není nutná úprava dávkování |
|
|
Saxagliptin |
CrCl ≤ 50 ml/min: 2.5 mg jednou denně ESRD vyžadující hemodialýzu: 2.5 mg jednou denně a podávat po hemodialýze |
|
|
Sitagliptin |
CrCl 30 až 50 ml/min: 50 mg jednou denně CrCl < 30 ml/min: ESRD vyžadující hemodialýzu nebo peritoneální dialýzu: 25 mg jednou denně a podávat bez ohledu na načasování hemodialýzy |
|
|
Vildagliptin |
CrCl < 50 ml/min: 50 mg jednou denně |
|
|
Sekvestranty žlučových kyselin |
Kolesevelam |
Není nutné upravovat dávkování |
|
Dopamin.2 agonisté |
Bromokriptin |
Žádné informace |
|
Inhibitory SGLT-2 |
Kanagliflozin |
eGFR 45 až 60 ml/min/1.73 m2: Nepřekračujte dávku 100 mg jednou denně eGFR < 45 ml/min/1,73 m2: Nedoporučuje se zahajovat léčbu. Pokud po zahájení léčby přetrvává eGFR < 45 ml/min/1,73 m2, léčbu přerušte. eGFR < 30 ml/min/1,73 m2/ESRD/Hemodialýza: Použití je kontraindikováno |
|
Dapagliflozin |
eGFR < 60 ml/min/1,73 m2: Nedoporučuje se zahájit léčbu. Pokud po zahájení léčby přetrvává eGFR mezi 30 a < 60 ml/min/1,73 m2, léčbu přerušte. eGFR < 30 ml/min/1,73 m2/ESRD/Hemodialýza: Použití je kontraindikováno |
|
|
Empagliflozin |
eGFR < 45 ml/min/1,73 m2: Nedoporučuje se zahájit léčbu. Pokud po zahájení léčby přetrvává eGFR < 45 ml/min/1,73 m2 eGFR < 30 ml/min/1,73 m2 ESRD/hemodialýza, léčbu přerušte: Použití je kontraindikováno |
|
|
GLP-1 receptorových agonistů |
Albiglutid |
Není nutná úprava dávkování |
|
Dulaglutid |
Není nutná úprava dávkování |
|
|
Exenatid |
CrCl 30 až 50 ml/min: Žádné informace. Používejte s opatrností. CrCl < 30 ml/min/ ESRD: CrCl < 30 ml/min/ ESRD: Použití se nedoporučuje |
|
|
Liraglutid |
Žádné informace |
|
|
Lixisenatid |
eGFR 15 až 29 ml/min/1.73 m2: Žádné informace. Sledujte zvýšené nežádoucí gastrointestinální účinky, které mohou vést k dehydrataci a zhoršení funkce ledvin. eGFR <15 ml/min/1.73 m2/ ESRD: Použití se nedoporučuje |
|
|
Amylinová mimetika |
Pramlintid |
CrCl ≥15 ml/min: Není nutná úprava dávkování ESRD: Žádné informace |
|
Insuliny |
Rapid-působící analogy
Krátkodobě působící
Intermediární-působící
Základní inzulínová analoga
|
Potřeba inzulínu může být snížena v důsledku změn v jeho clearance nebo metabolismu. Pečlivě sledujte hladinu glukózy v krvi. |
Krevní tlak. Léčba krevního tlaku by měla u pacientů s diabetem a diabetickým onemocněním ledvin začít při hodnotě 140/90 mmHg.37 Studie UKPDS (United Kingdom Prospective Diabetes Study) zjistila 12% snížení rizika diabetických komplikací s každým poklesem systolického tlaku o 10 mmHg až do hodnoty tlaku 120 mmHg.38 Léky volby zůstávají inhibitory ACE nebo ARB pro osoby s hypertenzí a diabetem, DKD a CKD. Bylo prokázáno, že inhibice ACE oddaluje rozvoj DKD, pokud je zahájena u pacientů s mírně zvýšenou albuminurií. Kreatinin může při zahájení léčby inhibitorem ACE nebo ARB stoupnout až o 30 %.39 Pokud kreatinin stoupne více, je třeba zvážit posouzení dalších základních onemocnění ledvin.
KDOQI nedoporučuje podávat ACE/ARB pacientům s diabetem 2. typu, kteří jsou normotenzní a mají normoalbuminurii.40,41,42 Inhibitory ACE nebo ARB se doporučují pacientům s diabetem, kteří jsou normotenzní s mikroalbuminurií.31,37 Pro tyto osoby neexistuje žádná specifická dávka nebo titrace. Duální blokáda renin-angiotenzinového systému pomocí ACE i ARB se nedoporučuje z důvodu zvýšeného rizika hyperkalémie, poruchy funkce ledvin a hypotenze.43
Snížení obsahu soli. Studie 2012 Reduction of Endpoints in Non-insulin-dependent diabetes mellitus with the Angiotensin II Antagonist Losartan (RENAAL) Trial a Irbesartan Diabetic Nephropathy Trial (IDNT) prokázaly, že dieta s nízkým obsahem sodíku zvyšuje nefroprotektivní a kardioprotektivní účinky ARB u pacientů s diabetem 2. typu a diabetickou nefropatií.44,45
Dialýza a transplantace ledvin. Pacienti s ESRD by měli být odesláni na nefrologii. Možnosti léčby zahrnují peritoneální dialýzu nebo hemodialýzu, transport ledvin nebo možnost přerušení léčby a zahájení paliativní nebo hospicové péče. Jedna observační studie zjistila, že pacienti, kteří zahájili dialýzu v mladším věku (< 60 let), měli horší přežití.46
Předání. Obrázek 1 zahrnuje indikace k odeslání na základě klasifikace GFR a albuminurie. Zvažte i jiné příčiny onemocnění ledvin nesouvisející s diabetem, zejména u pacientů s diabetem 1. typu, kde nástup retinopatie nepředchází rozvoji nefropatie.21 Nefrologové mohou pomoci objasnit diagnózu, kontrolovat rezistentní hypertenzi a hyperkalémii a připravit pacienty na dialýzu.8
Je třeba také vzít v úvahu, že rozvoj nefropatie nemusí souviset se samotným diabetem. U pacientů s diabetem 1. typu výskyt retinopatie obvykle předchází rozvoji nefropatie.47 U jedince, který má nefropatii, ale nemá retinopatii, by mělo být provedeno vyšetření jiných příčin. Ke stanovení příčiny nefropatie by měl být odeslán nefrolog v případě nejistoty nebo obtížně zvládnutelných problémů souvisejících s DKD, včetně anémie, hyperparatyreózy a postupujícího onemocnění ledvin s eGFR < 30 ml/min/1,73 m2.8 Konzultace s nefrologem při vzniku 4. stadia CKD (eGFR < 30 ml/min/1,73 m2) je spojena se snížením morbidity, snížením nákladů na zdravotní péči a oddálením dialýzy.48 Zvažte doporučení ve stadiu 3B, aby byli pacienti připraveni dříve a aby nefrolog mohl maximálně medikamentózně léčit.
Klinické perly
- Každoroční screening DKD by měl probíhat prostřednictvím vyšetření močového albuminu a měření eGFR.
- Kontrola krevního tlaku a glykemie může zajistit prevenci progrese nefropatie. U pacientů s diabetem a CKD udržujte krevní tlak < 140/90 mmHg. Léčbou volby by měly být inhibitory ACE nebo ARB.
- Inhibitory ACE a ARB by se neměly používat k prevenci nefropatie, pokud jsou krevní tlak a vylučování bílkovin normální. Inhibitory ACE a ARB by se neměly používat v kombinaci.
- Pacienti s CKD ve stádiu 3-5 mají zvýšené riziko hypoglykémie. Opatrně je třeba používat perorální přípravky, jako jsou sulfonylurey.
- U některých pacientů s CKD je vhodné stanovit cílovou hodnotu HbA1c > 7 %, zejména pokud je riziko hypoglykémie velké.
Diabetická periferní neuropatie
V klinické praxi obecně přijímaná definice diabetické periferní neuropatie (DPN) zní: „Přítomnost symptomů a/nebo známek dysfunkce periferních nervů u osob s diabetem po vyloučení jiných příčin.“49 Klasifikace distální symetrické polyneuropatie podle ADA je: 1) primárně neuropatie malých vláken, 2) primárně neuropatie velkých vláken a 3) smíšená neuropatie malých a velkých vláken (nejčastější).
Patofyziologie a patogeneze. Vývoj a progrese DPN vyplývají ze složitých vztahů mezi nervy a okolními buňkami.50 Ke všem stadiím DPN přispívají jak vaskulární faktory, tak metabolické interakce.51 Obecně přijímaným poznatkem u lidského diabetu vedoucím k rozvoji DPN je komplexní interakce mezi hyperglykémií, délkou trvání diabetu, poškozením neuronů souvisejícím s věkem, stupněm kontroly krevního tlaku a krevních lipidů a hmotností.52,53,54,55 Hyperglykémie aktivuje četné biochemické dráhy, které určují metabolický stav nervové buňky a v kombinaci se zhoršenou perfuzí nervu přispívají k progresi neuropatie. Přelomová studie DCCT podporuje význam hyperglykémie v patogenezi neuropatie.10,56,57 Dalším mechanismem souvisejícím s hyperglykémií, který vede k DPN, je hyperglykémií vyvolaný oxidativní a nitrosativní stres se zvýšenou produkcí volných radikálů.58,59
Kromě hyperglykémie se v poslední době předpokládá, že v patogenezi diabetických neuropatií může hrát důležitou roli i nízkostupňový zánět, který vede k deficitu periferních a autonomních nervových vláken.51,60 Komplexní soubor metabolických a cévních faktorů vyvolává nerovnováhu mezi poškozením a opravou nervových vláken, specificky postihuje distální senzorická vlákna a přispívá k postupné ztrátě citlivosti, která se projevuje klinickými příznaky diabetické polyneuropatie.58,61
Běžné příznaky. Při dotazování na prožívané příznaky DPN si všímejte lokalizace (nejčastěji pociťované na rukou a nohou), precipitujících faktorů, charakteristiky potíží a také nástupu a frekvence nočních exacerbací, protože příznaky jsou specifické pro každého pacienta.4 Zvýšenou hladinou glukózy v krvi jsou postižena jak malá, tak velká vlákna a prožívané příznaky se liší v závislosti na třídě postižených senzorických vláken. Pokud jsou postižena převážně malá nervová vlákna, vyvolanými příznaky jsou obvykle bolest (bodavá, lancinující, pichlavá, pálivá, bolestivá, nudná a nadměrně citlivá), dysestezie (nepříjemné pocity pálení, brnění, píchání a bodání) a necitlivost.4
Intenzita nepříjemných pocitů se může pohybovat od pocitu drobných abnormálních vjemů až po postižení bolestí, která se může zhoršovat v noci a narušovat spánek, což prokazatelně souvisí s depresí v důsledku vnímání snížené kvality života.4
Při postižení převážně velkých vláken mohou pacienti naopak pociťovat necitlivost a brnění v končetinách, nejistou chůzi a ztrátu rovnováhy (vedoucí k možným pádům).4 U některých pacientů může dojít ke zhoršení příznaků při poklesu hladiny glukózy v krvi v důsledku zintenzivnění terapeutické léčby diabetu. Pacienti mohou být asymptomatičtí, ale s různým stupněm ztráty citlivosti; nežádoucím důsledkem závažné ztráty citlivosti v důsledku diabetické neuropatie může být bezbolestné poranění, které vede ke zvýšenému riziku ulcerace nohy nebo v závažných případech k amputaci.62
Nejčastější formou diabetické periferní neuropatie je distální symetrická polyneuropatie s postupnou ztrátou senzorických nervových vláken.4 Typický „punčochovitý“ vzor oboustranně vzniká poškozením, ke kterému dochází na nejdistálnějších částech nejdelších nervů (jsou postiženy jako první).63,64,65 S postupem času vzniká z proximálního postupu nervových deficitů „punčochovitý“ vzor, který podporuje ztrátu citlivosti a typické příznaky DNP.4
Klinická diagnóza. Klinickou diagnózu DPN lze stanovit na základě neuropatických příznaků a symptomů pacienta s diabetem po vyloučení jiných příčin neuropatie.66 Asymptomatická diabetická periferní neuropatie se může vyskytnout až u 50 % osob, které mají tuto komplikaci; proto je nezbytné provádět preventivní péči o nohy, zejména u těch, kteří jsou vystaveni vysokému riziku úrazů v důsledku necitlivých nohou.4 Každoroční screening DPN by měl být prováděn u všech pacientů s diabetem pomocí pinpricku, teploty, vnímání vibrací (pomocí 128-Hz ladičky), pocitu tlaku 10-g monofilament a hlubokých šlachových reflexů kotníku; potenciální vředy na nohou lze předpovědět podle ztráty pocitu 10-g monofilament (ztráta ochranného pocitu) a sníženého vnímání vibrací.63 Standardy lékařské péče o diabetiky ADA-2017 nadále doporučují každoroční test 10-g monofilament za účelem identifikace pacientů s rizikem vzniku ulcerace a amputace.8 Kromě toho doporučují pokyny ADA z roku 2017 screening DPN při diagnóze diabetu 2. typu a pět let po diagnóze diabetu 1. typu.8
V roce 2009 aktualizoval Torontský konsenzuální panel pro diabetické neuropatie diagnostická kritéria a poskytl diagnostické kategorie. Kromě toho mohou poskytovatelé zdravotní péče do diagnostického procesu zahrnout několik dobře ověřených screeningových nástrojů, včetně Michigan Neuropathy Screening Instrument (MNSI), Toronto Clinical Neuropathy Score a Utah Neuropathy Scale. V tabulce 7 jsou popsány další příčiny neuropatie, které by měly být vyloučeny.
Tabulka 7. Další příčiny neuropatie67
- Alkohol nebo jiné toxiny
- Neurotoxické léky, zejména chemoterapie
- Deficit vitaminu B12
- Hypothyreóza
- Onemocnění ledvin
- Zhoubné nádory (mnohočetný myelom, bronchogenní karcinom)
- Virus lidské imunodeficience (HIV)
- Chronická zánětlivá demyelinizační neuropatie, dědičné neuropatie a vaskulitida
Diagnostické studie. K potvrzení přítomnosti DPN existuje několik diagnostických testů. Studie nervového vedení jsou již léta považovány za zlatý standard diagnostických testů DPN, protože jejich objektivní měření bez reakcí pacientů vede k vysoké spolehlivosti.4 Kvantitativní senzorické testování hodnotí schopnost pacientů detekovat lehký dotyk, vibrace a rozlišovat teplotu, což zahrnuje určitou míru subjektivity.4 Další metody, včetně kožní biopsie a intraepidermální hustoty nervových vláken a rohovkové konfokální mikroskopie, se v klinické praxi rutinně nepoužívají, ale lze je použít v klinických studiích.4
Možnosti léčby: Farmakologická léčba. Farmakologická léčba DPN slouží k symptomatickému zlepšení, takže používané léky nejsou určeny k prevenci progrese. Tabulka 8 shrnuje léky ze tří nejčastěji používaných skupin (antikonvulziva, antidepresiva a opioidy) ke kontrole neuropatických příznaků. Ačkoli se jako počáteční přístup k léčbě DPN běžně používá několik látek, pouze pregabalin a duloxetin byly schváleny FDA pro léčbu tohoto stavu; proto se jako počáteční volba pro symptomatickou neuropatickou bolest doporučuje některá z těchto látek.4 Gabapentin, ačkoli není schválen FDA pro použití v léčbě DPN, se často používá jako počáteční přístup, který má srovnatelnou účinnost s látkami schválenými FDA. Tricyklická antidepresiva (např. amitriptylin) – přípravky neschválené agenturou FDA – jsou při léčbě DPN účinná, ale měla by se používat s opatrností kvůli vyššímu riziku nežádoucích účinků.
Tabulka 8. Běžně používané farmakologické přípravky pro DPN4,69 |
|||||
|
Farmaceutický přípravek (rozsah NNT 30.50% zlepšení*) |
Max. denní dávka pro DNP (mg/den) |
Časté nežádoucí účinky |
Potřeba úpravy dávky? |
Kontraindikace |
Předpisování |
|
Antikonvulziva
|
|||||
|
Pregabalin (3.3-8,3) |
Závratě Somnolence Přibývání na váze Periferní otoky Rozmazané vidění Zácpa |
Renální: Ano Jaterní: Ne |
Přecitlivělost na pregabalin |
Silné důkazy; schváleno FDA; kontrolovaná látka |
|
|
Gabapentin (3.3-7.2) |
3,600 |
Závratě Ataxie Somnolence Bolesti hlavy Nausea Průjem Přibývání na váze |
Renal: Ano Hepatic: Ne |
Přecitlivělost na gabapentin |
Mírné důkazy; neschváleno FDA |
|
Antidepresiva
|
|||||
|
Amitriptylin (2.1-4.2) |
Těžká sedace; konfúze; anticholinergní účinky (zácpa, rozmazané vidění) |
Renální: Ne Jaterní: Ne U starších pacientů se doporučují nižší dávky |
Přecitlivělost na amitriptylin; současné podávání s MAO nebo během 14 dnů; současné podávání s cisapridem; akutní fáze zotavení po infarktu myokardu |
Mírné důkazy; neschváleno FDA; používat s opatrností u osob s kardiovaskulárním onemocněním v anamnéze |
|
|
Duloxetin (3.8-11) |
(USA) |
Nausea; sedace; generalizovaná ospalost |
Renální: Ano Jaterní: Vyhnout se použití při poruše funkce jater |
Přecitlivělost; současné podávání s MAO nebo během 14 dnů; zahájení podávání u osob, které dostávají linezolid nebo intravenózně methylenovou modř |
Střední důkazy; Schváleno FDA; může být přidáno k pregabalinu nebo gabapentinu |
|
Venlafaxin (5.2-8.4) |
Nausea; sedace; generalizovaná ospalost |
Renální: Ano Hepatické: Ano |
Slabé důkazy; není schváleno FDA; lze přidat ke gabapentinu |
||
|
Opioidy
|
|||||
|
Tramadol (2.1-6.4) |
Somnolence Nausea Zvracení Zácpa Světloplachost Závratě Bolesti hlavy |
Renální: Ano Hepatický: Ne |
Přecitlivělost na tramadol, opioidy nebo jakoukoli složku přípravku; ER přípravek: významná respirační deprese a akutní nebo těžké astma; IR přípravek: akutní intoxikace alkoholem, hypnotiky, narkotiky, centrálně působícími analgetiky, opioidy nebo psychotropními látkami |
Snížený potenciál pro zneužití (kontrolovaná látka seznamu IV); nedoporučuje se používat jako lék první nebo druhé volby |
|
|
Tapentadol (N/A) |
Přípravek s okamžitým uvolňováním: Prodloužené uvolňování: |
Somnolence Nevolnost Zvracení Zácpa Závratě |
Renální: Užívání se nedoporučuje, pokud Jaterní: Ne |
Při přecitlivělosti na tapentadol; výrazné respirační depresi; akutním nebo těžkém astmatu; paralytickém ileu; při 14denním užívání inhibitorů MAO |
Schváleno FDA; kontrolovaná látka seznamu II; nedoporučuje se používat jako prostředek první nebo druhé volby |
|
Informace se týkají léčivých přípravků získaných z příslušných příbalových letáků (odkazováno na obchodní názvy) |
|||||
Směrnice Americké neurologické akademie (AAN) doporučuje následující lokální přípravky: Kapsaicin a isosorbid dinitrát ve spreji (středně silné důkazy) a náplast Lidoderm (slabé důkazy).69 Oxkarbazepin, lamotrigin, lakosamid, klonidin, pentoxifylin a mexiletin nejsou ve směrnicích AAN při léčbě DPN doporučeny.69
Někteří navíc doporučují při refrakterní DPN používat opioidy. Mezi opioidy doporučované ve směrnici AAN patří dextrometorfan (400 mg/den), morfin sulfát (titrovaný na 120 mg/den) a oxykodon (průměrně 37 mg/den, maximálně 120 mg/den); neexistují však dostatečné údaje, které by doporučovaly použití jednoho přípravku místo druhého.69 Autoři tohoto článku doporučují použití opioidů pouze v těžkých refrakterních případech s pečlivým sledováním pacientů, kteří díky opioidům získají skutečné funkční zlepšení. Autoři se řídí stanoviskem Centra pro kontrolu a prevenci nemocí (Centers for Disease Control and Prevention) z roku 2016, podle něhož mají opioidy u bolestí nenádorového typu omezené dlouhodobé použití.70
Jedním z problémů farmakologické léčby DPN je nedostatečný počet head-to-head studií zahrnujících výsledky týkající se kvality života.4 Nedávná studie srovnávající osmitýdenní léčbu mezi vysokými dávkami pregabalinu, vysokými dávkami duloxetinu nebo v kombinaci nezjistila žádné významné rozdíly v průměrné změně bolesti mezi monoterapií a kombinovanou léčbou.71 Je zapotřebí více studií srovnávajících dvě účinné látky, které by poskytly náhled na zlepšení péče o osoby trpící diabetickou periferní neuropatií.
Nefarmakologická léčba. Postupy. Směrnice ANN navrhuje zvážit perkutánní elektrickou nervovou stimulaci po dobu tří až čtyř týdnů pro léčbu DPN.69 Pilotní, dvoustupňová akupunkturní, randomizovaná, kontrolovaná studie72 a jednoslepá, placebem kontrolovaná, randomizovaná studie73 hodnotící účinnost akupunktury u DPN prokázaly zlepšení výsledných ukazatelů souvisejících s bolestí. K potvrzení role akupunktury v léčbě DPN jsou však zapotřebí další studie.
Kyselina alfa-lipoová. Některé důkazy naznačují, že užívání antioxidační kyseliny alfa-lipoové by mohlo pomoci snížit oxidační stres zprostředkovaný volnými radikály a poskytnout následující výhody: zaměření na patogenezi, zpomalení vývoje a zlepšení příznaků DPN.74,75
Prevence. Bylo prokázáno, že úprava životního stylu se zaměřením na zdravou stravu a fyzickou aktivitu průběžně snižuje prevalenci diabetu a jeho komplikací, včetně diabetické periferní neuropatie.68 Bylo prokázáno, že intenzivní kontrola glykémie pomáhá snižovat riziko diabetické neuropatie u pacientů s diabetem prostřednictvím zlepšení funkce nervů.61,76,77 DCCT stanovila roli kontroly glykémie v prevenci a zastavení progrese diabetické neuropatie u diabetu 1. typu.10,56
Klinické perly
- Až 50 % pacientů může mít nebolestivou nebo asymptomatickou periferní neuropatii.
- Pacientům s neuropatií se doporučuje edukace v oblasti péče o nohy (každodenní samokontrola nohou) a u vybraných pacientů pravidelná podiatrická péče.
- Pacientům s DPN, kteří vykazují známky ztráty ochranného čití s deformitou nebo bez ní, by měla být doporučena preventivní kontrola u lékaře každé tři až šest měsíců.64
- Pro účinné zvládnutí příznaků DPN se stává nezbytným multidisciplinární přístup; tento komplexní přístup může zahrnovat farmakologickou, psychologickou a/nebo fyzikální terapii.
- Nové stanovisko k diabetické neuropatii vydané ADA doporučuje screening DPN u pacientů s prediabetem vykazujících příznaky periferní neuropatie.4
- Specializovanou péči potřebují osoby s periferním onemocněním, nesenzorickou neuropatií nebo Charcotovou nohou.
Gastroparéza
Další formou diabetické neuropatie je gastroparéza. Tento stav je spojen s příznaky horní části gastrointestinálního traktu včetně nevolnosti, zvracení, časné sytosti nebo postprandiální plnosti, bolesti břicha a nadýmání, avšak při absenci obstrukce vývodu. Ačkoli existuje řada příčin gastroparézy, odhaduje se, že přibližně třetina všech případů připadá na diabetes.78
Patofyziologie. Navrhované patofyziologické mechanismy diabetické gastroparézy zahrnují poruchu glykemické kontroly, vagovou nebo prevertebrální neuropatii sympatických ganglií, abnormality intersticiálních Cajalových buněk, ztrátu syntázy oxidu dusnatého a případně myopatii.79,80
Klinický obraz. Na počátku tohoto onemocnění jsou pacienti obvykle asymptomatičtí. Mezi příznaky a závažností neuropatie není lineární vztah. Široká škála příznaků ztěžuje diagnostiku tohoto onemocnění. Mezi další klinické projevy patří anorexie, malnutrice, úbytek hmotnosti a hypoglykémie z nesouladu vstřebávání potravy a inzulínu. Bolest může být ve skutečnosti nedostatečně hlášená, ale pro mnoho lidí významná. V konsorciu financovaném NIH mělo 72 % pacientů s gastroparézou bolesti břicha.81 U 18 % těchto pacientů to byl dominantní příznak. Bolest byla u těchto pacientů vyvolána jídlem (72 %), byla noční (74 %) a narušovala spánek (66 %).81
Jak častá je gastroparéza při diabetu? Kumulativní desetiletý výskyt gastroparézy byl odhadnut na 5,2 % u diabetu 1. typu a 1 % u diabetu 2. typu mezi pacienty s diabetem v komunitě.82 Podle jiných studií se výskyt pohybuje mezi 5-12 %.83,84 Výskyt je však mnohem vyšší, pokud je diagnóza stanovena na základě příznaků, nikoliv na základě studie vyprazdňování žaludku.
Gastroparéza je častější u diabetu 1. typu než u diabetu 2. typu a nejčastěji se objevuje poté, co osoba trpí diabetem déle než 10 let a rozvinuly se u ní další mikrovaskulární komplikace – retinopatie, nefropatie a periferní neuropatie. Pokud se u pacienta objeví gastroparéza dříve, než se očekávalo, je třeba pátrat po jiné etiologii, nejčastěji po perioperačním poškození vagového nervu nebo po farmakologických účincích léků na bázi inkretinů – agonistů receptoru pro glukagonu podobný peptid 1 (GLP-1RA) a inhibitorů dipeptidyl-peptidázy 4 (inhibitory DPP-4).
Jakmile se u pacienta objeví příznaky gastroparézy, příznaky obvykle přetrvávají a jsou stabilní po dobu 12-25 let. To platí i v případě, že dojde ke zlepšení kontroly glykémie,85 s výjimkou případu transplantace slinivky břišní a ledviny.86 Ačkoli neexistují jasné důkazy, že gastroparéza sama o sobě zvyšuje úmrtnost, podstatně snižuje všechny aspekty kvality života.87
Diagnostika. S diagnózou může pomoci řada testů. Zlatým standardem pro tuto diagnózu je gastroezofageální scintigrafie. Je neinvazivní, testuje fyziologii a poskytuje kvantitativní výsledky. Gastroparézu lze diagnostikovat, pokud dojde k zadržení alespoň 35 % standardního nízkotučného jídla čtyři hodiny po požití.80
Pro zajištění co nejpřesnějších výsledků testu by měl předtestový protokol zahrnovat vysazení všech léků ovlivňujících motilitu alespoň na dva až tři dny před testováním, včetně prokinetik, opiátů a anticholinergik. Inkretinové přípravky, jako jsou agonisté GLP-1 a inhibitory DPP-4, by měly být rovněž vysazeny, protože je o nich známo, že zpomalují vyprazdňování žaludku. Bylo prokázáno, že hyperglykémie rovněž zpomaluje vyprazdňování žaludku, a proto by glykémie měla být před zahájením studie nižší než 275 mg/dl.79,88
Pacienti by se měli zdržet kouření a konzumace alkoholu v den testu, protože obojí může zpomalit vyprazdňování žaludku.89 GLP-1RA navíc mohou gastroparézu zhoršit, protože zpomalují vyprazdňování žaludku. Dále mohou mít někteří lidé subklinickou gastroparézu, která se při nasazení GLP-1RA odhalí.
Léčba. Léčba gastroparézy závisí do značné míry na závažnosti příznaků. Obecné zásady léčby zahrnují podpůrnou léčbu (tekutiny, elektrolyty, kontrola glykémie a výživa), medikamentózní léčbu (prokinetika, antiemetika a úleva od bolesti) a invazivní léčbu (chirurgický zákrok, injekce botoxu, stimulace žaludku nebo elektrická stimulace).79
Podpůrná léčba se obvykle zahajuje v nemocnici a je zaměřena na normalizaci poruch tekutin, elektrolytů a výživy. Při poskytování nutriční podpory se upřednostňuje enterální výživa před parenterální, protože je fyziologičtější a může pomoci udržet střevní flóru. Dále mohou být u gastroparézy velmi užitečné změny stravy. U pacientů s gastroparézou se doporučuje dieta s nízkým obsahem vlákniny a tuků a s nízkým obsahem zbytků.85 Dieta s vysokým obsahem vlákniny může zvýšit příznaky, protože vyžaduje více trávení.
Léky. Prokinetika: Ve Spojených státech jsou nejčastěji používanými léky k léčbě gastroparézy metoklopramid a erytromycin. Metoklopramid má však varování na černém rámečku kvůli riziku tardivní dyskineze. Rozvoj tohoto stavu přímo souvisí s délkou užívání metoklopramidu a počtem užívaných dávek. Při užívání tohoto léku je nejlepší užívat jej pouze u symptomatických pacientů a začít s nejnižší účinnou dávkou 15 minut před jídlem. Lékové prázdniny mohou někdy pomoci prodloužit trvání účinku.90
Domperidon je selektivnější agonista dopaminu, který je stejně účinný jako metoklopramid, ale má méně nežádoucích účinků na centrální nervový systém.91
Antiemetika: Antiemetika mohou být použita na pomoc s příznaky. Riziko lékových interakcí je však značné a mělo by být pečlivě sledováno.
Zvládání bolesti může být u pacientů s gastroparézou problémem. Tricyklická antidepresiva se často používají jako léčba první volby bolesti u gastroparézy. Přístupy druhé volby jsou slabý agonista mu-opioidních receptorů tramadol, který rovněž uvolňuje serotonin a inhibuje zpětné vychytávání noradrenalinu, a analog kyseliny gama-aminomáselné gabapentin. Užívání narkotik u gastroparézy se však nedoporučuje, protože může přispět k zácpě a zhoršení příznaků.
Invazivní léčba: Botoxové injekce se při léčbě gastroparézy běžně používají, jejich použití však není podloženo klinickými studiemi.92,93
Zařízení pro elektrickou stimulaci žaludku bylo schváleno FDA na základě výjimky pro humanitární zařízení v roce 2000.94 Zařízení pro elektrickou stimulaci žaludku poskytuje žaludku vysokofrekvenční elektrickou stimulaci s nízkou energií. Je užitečnější u diabetické gastroparézy než u idiopatické gastroparézy. Metaanalýza prokázala značný přínos pro symptomy pacientů. Přesný mechanismus jejího přínosu není dosud znám.95 Předpokládá se, že elektrická stimulace žaludku vede ke změnám v centrálních mechanismech, které kontrolují nevolnost a zvracení, zvyšuje vagovou funkci a vede ke snížení citlivosti na distenzi.97 Pacienti, kteří dobře reagují, obvykle reagují rychle. To vedlo některé k tomu, že před dlouhodobým zavedením doporučují nejprve vyzkoušet dočasné umístění elektrod.
Klinické perly
- Diabetická gastroparéza je častější u osob s dlouhodobým diabetem a u osob s jinými mikrovaskulárními komplikacemi.
- Zlatým standardem diagnostiky gastroparézy je gastroezofageální scintigrafie.
- U diabetické gastroparézy se doporučuje dieta s nízkým obsahem vlákniny a tuků a nízkým obsahem zbytků.
- Farmakologická a intervenční léčba má omezený přínos a významné dlouhodobé riziko.
Diabetická cheiroartropatie
Jednou z méně známých komplikací diabetu je cheiroartropatie. Tento stav je charakterizován omezenou pohyblivostí kloubů v důsledku ztluštění kůže u osob s dlouhodobým diabetem. Pravděpodobně se jedná o první komplikaci zjištěnou u diabetu 1. typu. Míra výskytu se pohybuje v širokém rozmezí 8-50 %.98
Předpokládá se, že příčinou cheiroartropatie je glykosylace a zesíťování kolagenu. Může postihovat kůži a šlachy a může mít za následek omezenou pohyblivost kloubů, nejčastěji extenzi prstů, ztuhlost a bolest. Klasickým příznakem fyzikálního vyšetření diabetické cheiropatie je „modlitební znamení“. Při tomto stavu není člověk schopen zcela srovnat ruce, aby se „modlil“, a mezi prsty levé a pravé ruky tak zůstává mezera. Existují důkazy, že ti, u nichž se cheiropatie rozvine, mají třikrát vyšší riziko mikrovaskulárních komplikací.99
Diabetická cheiropatie se obvykle zhoršuje u osob s dlouhodobou nebo špatně kontrolovanou glykémií. Naštěstí u mnoha lidí dochází po zlepšení kontroly glykémie ke zmírnění příznaků a zlepšení pohyblivosti.100
Závěr
Léčba komplikací diabetu vyžaduje multidisciplinární tým. Vzhledem k asymptomatické povaze onemocnění je zásadní včasný screening retinopatie, nefropatie a neuropatie. Charakteristickým znakem léčby všech komplikací diabetu zůstává kontrola glykémie a krevního tlaku.
- American Diabetes Association. Náklady na diabetes. Dostupné na: http://www.diabetes.org/advocacy/news-events/cost-of-diabetes.html?referrer=https://www.google.com/. Aktualizováno 22. června 2015. Dostupné 8. února 2017.
- UK Prospective Diabetes Study Group. Intenzivní kontrola glykémie pomocí sulfonylurey nebo inzulínu ve srovnání s konvenční léčbou a riziko komplikací u pacientů s diabetem 2. typu. Lancet 1998;352:837-853.
- Gregg EW, Yanfed L, Wang J. Changes in diabetes-related complications in the United States, 1990-2010. N Engl J Med 2014;370:1514-1523.
- Pop-Busui R, Boulton A, Feldman E, et al. Diabetes neuropathy: Stanovisko Americké diabetologické asociace. Diabetes Care 2017;40:136-154.
- Leasher JL, Bourne RR, Flaxman SR, et al. Global estimates on the number of people blind or visually impaired by diabetic retinopathy: A meta-analysis from 1990 to 2010. Diabetes Care 2016;39:1643-1649.
- National Eye Institute. Fakta o diabetickém očním onemocnění. Dostupné na: https://nei.nih.gov/health/diabetic/retinopathy. Aktualizováno v září 2015. Přístup 8. února 2017.
- Fong, DS, Aiello L, Gardner TW, et al. Retinopathy in diabetes. Diabetes Care 2004;27(Suppl 1):S84-S87.
- American Diabetes Association. Standardy lékařské péče u diabetu-2017. Diabetes Care 2017;40:(Suppl 1):S4-S5.
- Doggen K, Nobels F, Scheen AJ, et al. Cardiovascular risk factors and complications associated with albuminuria and impaired renal function in insulin-treated diabetes. J Diabetes Complications 2013;27:370-375.
- The Diabetes Control and Complications Trial Research Group. The effect of intensive treatment of diabetes on the development and progression of long-term complications in insulin-dependent diabetes mellitus [Vliv intenzivní léčby diabetu na rozvoj a progresi dlouhodobých komplikací u diabetes mellitus závislého na inzulínu]. N Engl J Med 1993;329:977-986.
- Action to Control Cardiovascular Risk in Diabetes Follow-On (ACCORDION) Eye Study Group and the Action to Control Cardiovascular Risk in Diabetes Follow-On (ACCORDION) Study Group. Přetrvávající účinky intenzivní kontroly glykémie na retinopatii u diabetu 2. typu v následné studii Action to Control Cardiovascular Risk in Diabetes (ACCORDION). Diabetes Care 2016;39:1089-1100.
- ACCORD Study Group, ACCORD Eye Study Group, Chew EY, et al. Effects of medical therapies on retinopathy progression in type 2 diabetes. N Engl J Med 2010;363:233-244.
- Chew EY, Davis MD, Danis RP, et al. The effects of medical management on progression of diabetic retinopathy in persons with type 2 diabetes: Oční studie ACCORD (The Action to Control Cardiovascular Risk in Diabetes). Ophthalmology 2014;121:2443-2451.
- Diabetes Control and Complications Trial Research Group. Vliv těhotenství na mikrovaskulární komplikace ve studii Diabetes Control and Complications Trial. Diabetes Care 2000;23:1084-1091.
- Colberg SR, Sigal RJ, Yardley JE, et al. Physical activity/exercise and diabetes: A position statement of the American Diabetes Association. Diabetes Care 2016;39:2065-2079.
- The Diabetic Retinopathy Study Research Group. Předběžná zpráva o účincích fotokoagulační léčby. Am J Ophthalmol 1976;81:383-396.
- Early Treatment Diabetic Retinopathy Study Research Group. Photocoagulation for diabetic macular edema (Fotokoagulace u diabetického makulárního edému): Early Treatment Diabetic Retinopathy Study report number 1. Arch Ophthalmol 1985;103:1796-1806.
- Nguyen QD, Brown DM, Marcus DM, et al. Ranibizumab for diabetic macular edema: Výsledky 2 randomizovaných studií fáze III: RISE a RIDE. Ophthalmology 2012;119:789-801.
- Wong TY, Cheung CMG, Larsen M, et al. Diabetická retinopatie. Nat Rev Disease Prim doi:10.1038/nrdp.2016.12; publikováno online 17. března 2016.
- Batuman V, Soman AS, Schmidt RJ, Soman SS. Diabetická nefropatie. Medscape Dostupné na: Medscape: http://emedicine.medscape.com/article/238946-overview. Aktualizováno 30. září 2016. Dostupné 12. února 2017.
- Tuttle KR, Bakris GL, Bilous RW, et al. Diabetic kidney disease: Zpráva z konsensuální konference ADA. Diabetes Care 2014;37:2864-2883. https://doi.org/10.2337/dc14-1296
- Patel A, MacMahon S, Chalmers J, et al. Intensive blood glucose control and vascular outcomes in patients with type 2 diabetes. N Engl J Med 2008;358:2560-2572.
- Duckworth W, Abraira C, Moritz T, et al. Glucose control and vascular complications in veterans with type 2 diabetes. N Engl J Med 2009;360:129-139.
- Ismail-Beigi F, Craven T, Banerji MA, et al. Effect of intensive treatment of hyperglycaemia on microvascular outcomes in type 2 diabetes: Provedená analýza randomizované studie ACCORD. Lancet 2010;376:419-430.
- National Kidney Foundation. KDOQI clinical practice guideline for diabetes and CKD: 2012 update [Pokyny pro klinickou praxi pro diabetes a CKD: aktualizace 2012]. Am J Kidney Dis 2012;60:850-886.
- Fox CS, Matsushita K, Woodward M, et al. Chronic Kidney Disease Prognosis Consortium. Associations of kidney disease measures with mortality and end-stage renal disease in individuals with and without diabetes: A meta-analysis. Lancet 2012;380:1662-1673.
- Hahr AJ, Molitch ME. Management diabetes mellitus u pacientů s chronickým onemocněním ledvin. Clin Diabetes Endocrinol 2015. doi: 10.1186/s40842-015-0001-9.
- Alsaad KO, Herzenberg AM. Odlišení diabetické nefropatie od jiných případů glomerulosklerózy: An update. J Clin Pathol 2007;60:18-26.
- Narva AS, Bilous RW. Laboratorní hodnocení diabetického onemocnění ledvin. Diabetes Spectr 2015;28:162-166.
- Levey AS, Stevens LA, Schmid CH, et al. A new equation to estimate glomerular filtration rate. Ann Intern Med 2009;150:604-612.
- National Kidney Foundation. KDOQI clinical practice guidelines for chronic kidney disease (Pokyny pro klinickou praxi pro chronické onemocnění ledvin): Hodnocení, klasifikace a stratifikace. Am J Kidney Dis 2002;39(2 Suppl 1):S1-S266.
- de Boer IH, Rue TC, Cleary PA, et al. Long-term renal outcomes of patients with type 1 diabetes mellitus and microalbuminuria: Diabetes Control and Complications Trial/Epidemiology of Diabetes Interventions and Complications kohorta. Arch Intern Med 2011;171:412-420.
- Wanner C, Inzucchi SE, Lachin JM, et al. Empagliflozin and progression of kidney disease in type 2 diabetes. N Engl J Med 2016;375:323-334.
- Heerspink HJL, Desai M, Jardine M, et al. Canagliflozin zpomaluje progresi poklesu renálních funkcí nezávisle na glykemických účincích. J Am Soc Nephrol 2016;28:1-8.
- Lexi-Drugs. Lexicomp. Wolters Kluwer Health, Inc. Riverwoods, IL. Dostupné na adrese: http://online.lexi.com. Přístup 31. října 2016.
- Micromedex Solutions. Truven Health Analytics, Inc. Ann Arbor, MI. Dostupné na adrese: http://www.micromedexsolutions.com. Přístup 31. 10. 2016.
- James PA, Oparil S, Carter BL, et al. 2014 evidence-based guideline for the management of high blood pressure in adults. JAMA 2014;311:507-520.
- King P, Peacock I, Donnelly R. The United Kingdom Prospective Diabetes Study (UKPDS): Klinické a terapeutické důsledky pro diabetes 2. typu. Br J Clin Pharmacol 1999;48:643-648.
- Jackevicius CA, Wong J, Aroustamian I, et al. Rates and predictors of ACE inhibitor disontinuation following to elevated serum creatinine: A retrospective cohort study. BMJ Open 2014;4:e005181.
- Mauer M, Zinman B, Gardiner R, et al. Renal and retinal effects of enalapril and losartan in type 1 diabetes. N Engl J Med 2009;361:40-51.
- Bilous R, Chaturvedi N, Sjølie AK, et al. Effect of candesartan on microalbuminuria and albumin excretion rate in diabetes: Tři randomizované studie. Ann Intern Med 2009;151:11-20.
- Haller H, Ito S, Izzo JL Jr, et al. Olmesartan for delay or prevention of microalbuminuria in type 2 diabetes. N Engl J Med 2011;364:907-917.
- Makani H, Bangalore S, Desouza KA, et al. Účinnost a bezpečnost duální blokády systému renin-angiotenzin: Metaanalýza randomizovaných studií. BMJ 2013;346:f360.
- Miao Y, Ottenbros SA, Laverman GD, et al. Effect of a reduction of a uric acid on renal outcomes during losartan treatment: Angiotenzin II Antagonist Losartan Trial: post-hoc analýza snížení koncových ukazatelů u diabetu mellitu nezávislého na inzulínu. Hypertension 2011;58:2-7.
- Lewis EJ, Hunsicker LG, Clarke WR, et al. Renoprotective effect of the angiotensin-receptor antagonist irbesartan in patients with nehropathy due to type 2 diabetes. N Eng J Med 2001;354:851-860.
- Adler A, Casula A, Steenkamp R, et al. Association between glycemia and mortality in diabetic individuals on renal replacement therapy in the U.K. Diabetes Care 2014;37:1304-1311.
- Sharma SG, Bomback AS, Radhakrishnan J, et al. The modern spectrum of renal biopsy findings in patients with diabetes. Clin J Am Soc Nephrol 2013;8:1718-1724.
- Smart NA, Dieberg G, Ladhani M, Titus T. Early referral to specialist nefrology services for preventing the progression to end-stage kidney disease. Cochrane Database Syst Rev 2014;6:CD007333.
- Boulton AJM, Gries FA, Jervell JA. Pokyny pro diagnostiku a ambulantní léčbu diabetické periferní neuropatie. Diabet Med 1998;15:508-514.
- O’Brien PD, Hinder LM, Sakowski SA, Feldman EL. ER stres u diabetické periferní neuropatie: A new therapeutic target. Antioxid Redox Signal 2014;21:621-633.
- Cameron NE, Cotter MA. Prozánětlivé mechanismy u diabetické neuropatie: Dráha nukleárního faktoru kappa B: zaměření na dráhu nukleárního faktoru kappa B. Curr Drug Targets 2008;9:60-67.
- Tesfaye S, Chaturvedi N, Eaton SE, et al. Vascular risk factors and diabetic neuropathy. N Engl J Med 2005;352:341-350.
- Wiggin TD, Sullivan KA, Pop-Busui R, et al. Elevated triglycerides correlated with progression of diabetic neuropathy. Diabetes 2009;58:1634-1640.
- Stella P, Ellis D, Maser RE, Orchard TJ. Kardiovaskulární autonomní neuropatie (poměr výdechu a nádechu) u diabetu 1. typu. Incidence a prediktory. J Diabetes Complications 2000;14:1-6.
- Witten DR, Tesfaye S, Chaturvedi N, et al. Risk factors for cardiac autonomic neuropathy in type 1 diabetes mellitus. Diabetologia 2005;48:164-171.
- Výzkumná skupina DCCT (Diabetes Control and Complication Trial). Vliv intenzivní léčby diabetu na nervové vedení ve studii Diabetes Control and Complications Trial. Ann Neurol 1995;38:869-880.
- Diabetes Control and Complication Trial (DCCT) Research Group. The effect of intensive diabetes therapy on measures of autonomic nervous system function in the Diabetes Control and Complications Trial (DCCT). Diabetologia 1998;41:416-423.
- Edwards JL, Vincent AM, Cheng HT, Feldman EL. Diabetická neuropatie: Mechanismy k léčbě. Pharmacol Ther 2008;120:1-34.
- Vincent AM, Callaghan BC, Smith AL, Feldman EL. Diabetická neuropatie: Cellular mechanisms a therapeutic target (Buněčné mechanismy terapeutickým cílem). Nat Rev Neurol 2011;7:573-583.
- Kellogg AP, Wiggin T, Larkin D, et al. Protective effects of cyclooxygenase-2 gene inactivation against peripheral nerve dysfunction and intraepidermal nerve fibers loss in experimental diabetes. Diabetes 2007;56:2997-3005.
- Callaghan BC, Cheng HT, Stables CL, et al. Diabetic neuropathy: Klinické projevy a současná léčba. Lancet Neurol 2012;11:521-534.
- Boulton AJM, Kirsner RS, Vileikyte L. Klinická praxe: Neuropatické diabetické vředy na nohou. N Eng J Med 2004;351:48-55.
- Boulton AJM, Vinik AI, Arezzo JC, et al. Diabetic neuropathies: Prohlášení Americké diabetologické asociace. Diabetes Care 2005;28:956-962.
- Boulton AJM, Armstrong DG, Albert SF, et al. Comprehensive foot examination and risk assessment: A report of the task force of the foot care interest group of the American Diabetes Association, with the endorsement by the American Association of Clinical Endocrinologists. Diabetes Care 2008;31:1679-1685.
- Tesfaye S, Boulton AJ, Dyck PJ, et al. Diabetic neuropathies: Update on definitions, diagnostic criteria, estimation of severity, and treatments. Diabetes Care 2010;33:2285-2293.
- Dyke PJ, Albers JW, Andersen H, et al. Diabetic polyneuropathies: Aktuální informace o definici výzkumu, diagnostických kritériích a odhadu závažnosti. Diabetes Metab Res Rev 2011;27:620-628.
- Freeman R. Not all neuropathy is diabetes is of diabetic etiology: Diferenciální diagnostika diabetické neuropatie. Curr Diabe Rep 2009;9:423-431.
- Balducci S, Iacobellis G, Parisi L, et al. Exercise training can modify the natural history of diabetic peripheral neuropathy. J Diabetes Complications 2006;20:216-223.
- Bril V, England J, Franklin GM, et al. Evidence-based guideline: Gestorské doporučení: Léčba bolestivé diabetické neuropatie (Treatment of painful diabetic neuropathy). Zpráva Americké neurologické akademie, Americké asociace neuromuskulární a elektrodiagnostické medicíny a Americké akademie fyzikální medicíny a rehabilitace. Neurology 2011;76:1758-1765.
- Dowell D, Haegerich TM, Chou R. CDC Guideline for prescribing opioids for chronic pain – United States 2016. MMWR Recomm Rep 2016;65:1-49.
- Tesfaye S, Wilhelm S, Lledo A, et al. Duloxetine and pregabalin: High-dose monotherapy or their combination? Studie „COMBO-DN“ – mezinárodní, randomizovaná, dvojitě zaslepená studie s paralelními skupinami u pacientů s diabetickou periferní neuropatickou bolestí. Pain 2013;154:2616-2625.
- Ahn AC, Bennani T, Freeman R, et al. Two styles of acupuncture for treating painful diabetic neuropathy – a pilot randomized control trial. Acupunct Med 2007;25:11-17.
- Garrow A, Xing M, Vere J, et al. Role akupunktury v léčbě diabetické bolestivé neuropatie (DPN): A pilot RCT. Acupunct Med 2014;32:242-249.
- Ziegler D, Nowak H, Kempler P, et al. Léčba symptomatické diabetické polyneuropatie pomocí antioxidantu kyseliny alfa-lipoové: A meta-analysis. Diabet Med 2004;21:114-121.
- Ziegler D, Low PA, Litchy WJ, et al. Efficacy and safety of antioxidant treatment with alpha-lipoic acid over 4 years in diabetic polyneuropathy: The NATHAN 1 trial. Diabetes Care 2011;34:2054-2060.
- Kuwabara S, Ogawara K, Harrori T, et al. The acute effects of glycemic control on axonal excitability in human diabetic neres. Intern Med 2002;41:360-365.
- Peltier A, Goutman SA, Callaghan BC. Bolestivá diabetická neuropatie. BMJ 2014;348:g1799.
- Soykan I, Sivri B, Sarosiek I, et al. Demografie, klinické charakteristiky, psychologické profily a profily zneužívání, léčba a dlouhodobé sledování pacientů s gastroparézou. Dig Dis Sci 1998;43:2398-2404.
- Camilleri M, Bharucha AE, Farrugia G. Epidemiologie, mechanismy a léčba diabetické gastroparézy. Clin Gastroenterol Hepatol 2011;9:5-12.
- Shin AS, Camilleri M. Diagnostické hodnocení diabetické gastroparézy. Diabetes 2013;62:2667-2673.
- Hasler WL, Wilson L, Parkman HP, Lee L. Importance of abdominal pain as a symptom in gastroparesis: Vztah ke klinickým faktorům, závažnosti onemocnění, kvalitě života, retenci žaludku a užívání léků. Gastroenterology 2010;138. doi: 10.1016/S0016-5085(10)62131-2.
- Choung RS, Locke GR 3rd, Schleck CD, et al. Risk of gastroparesis in subjects with type 1 and 2 diabetes in the general population. Am J Gastroenterol 2012;107:82-88.
- Maleki D, Locke GR III, Camilleri M, et al. Gastrointestinal tract symptoms among persons with diabetes mellitus in the community. Arch Intern Med 2000;160:2808-2816.
- Bytzer P, Talley NJ, Leemon M, et al. Prevalence gastrointestinálních symptomů spojených s diabetes mellitus: Průzkum v populaci 15 000 dospělých. Arch Intern Med 2001;161:1989-1996.
- Jones KL, Russo A, Berry MK, et al. A longitudinal study of gastric emptying and upper gastrointestinal symptoms in patients with diabetes mellitus. Am J Med 2002;113:449-455.
- Gaber AO, Hathaway DK, Abell T, et al. Improved autonomic and gastric function in pancreas-kidney vs kidney-alone transplantation contributes to quality of life. Transplant Proc 1994;26:515-516.
- Punkkinen J, Färkkilä M, Mätzke S, et al. Upper abdominal symptoms in patients with Type 1 diabetes: S poruchou vyprazdňování žaludku způsobenou autonomní neuropatií nesouvisí. Diabet Med 2008;25:570-577.
- Schvarcz E, Palmer M, Aman J, et al. Physiological hyperglycemia slows gastric emptying in normal subjects and patients with insulin-dependent diabetes mellitus. Gastroenterology 1997;113:60-66.
- Miller G, Palmer KR, Smith B, et al. Smoking delays gastric emptying of solids. Gut 1989;30:50-53.
- Rao AS, Camilleri M. Přehledový článek: Metoclopramide and tardive dyskinesia. Aliment Pharmacol Ther 2010;31:11-19.
- Patterson D, Abell T, Rothstein R, et al. A double-blind multicenter comparison of domperidone and metoclopramide in the treatment of diabetic patients with symptoms of gastroparesis. Am J Gastroenterol 1999;94:1230-1234.
- Arts J, Holvoet L, Caenepeel P, et al. klinická studie: Randomizovaná zkřížená studie intrapylorické injekce botulotoxinu u gastroparézy. Aliment Pharmacol Ther 2007;26:1251-1258.
- Friedenberg FK, Palit A, Parkman HP, et al. Botulinum toxin A for the treatment of delayed gastric emptying. Am J Gastroenterol 2008;103:416-423.
- Humanitární výjimka pro zařízení Enterra. Fed Reg 2000;65:78495-78496.
- O’Grady G, Egbuji JU, Du P, et al. High-frequency gastric electrical stimulation for the treatment of gastroparesis: A meta-analysis: A meta-analysis: A meta-analysis: A meta-analysis. World J Surg 2009;33:1693-1701.
- Reddymasu SC, Sarosiek I, McCallum RW. Těžká gastroparéza: Léčebná terapie nebo elektrická stimulace žaludku. Clin Gastroenterol Hepatol 2010;8:117-124.
- McCallum RW, Dusing RW, Sarosiek I, et al. Mechanisms of symptomatic improvement after gastric electrical stimulation in gastroparetic patients. Neurogastroenterol Motil 2010;22:161-167.
- Douloumpakas I, Pyrpasopoulou A, Triantafyllou A, et al. Prevalence muskuloskeletálních poruch u pacientů s diabetes mellitus 2. typu: A pilot study. Hippokratia 2007;11:216-218.
- Rosenbloom AL, Silverstein JH, Lezotte DC. Omezená pohyblivost kloubů u dětského diabetes mellitus ukazuje na zvýšené riziko mikrovaskulárního onemocnění. N Engl J Med 1981;305;191-194.
- Lister DM, Graham-Brown RAC, Burden AC. Řešení diabetické cheiroartropatie. Br Med J 1986;293:1537.
.