- Mitä happamuus on?
- Mikä on pH?
- Miksi happamuus on tärkeää?
- Oireita liian alhaisesta pH:sta (kasvualusta on liian hapan)
- Oireita liian korkeasta pH:sta (kasvualusta on liian emäksinen)
- Mikä määrittää pH:n?
- PH-arvon mittaaminen
- Näytteiden ottaminen
- Oikeita pH-arvoja jokaiselle kasvualustalle
- PH-arvon korjaaminen
Mitä happamuus on?
Happamuus on välttämätöntä elämälle maapallolla. Happamuus määrää usein monien aineiden ominaisuudet, laadun, imeytyvyyden ja liukoisuuden. Näin toimivat entsyymit, jotka vastaavat lähes kaikista eliöiden biologisista prosesseista, mutta vain oikean happamuuden vallitessa. Pienikin vaihtelu veren happamuudessa on tappavaa.
Mikä on pH?
PH (pondus Hydrogenii) osoittaa s liuoksen happamuuden tai emäksisyyden. pH-arvo vaihtelee yleensä välillä 0-14. Liuos, jonka pH-arvo on välillä 0-7, on hapan ja liuos, jonka pH-arvo on välillä 7-14, on emäksinen. Etikan ja kolan pH-arvo on alle 3. Soodan ja saippuan pH-arvo on yli 8. pH-arvoa 7 pidetään neutraalina. Puhtaan veden pH-arvo huoneenlämmössä on 7. Vesijohtoveden pH-arvo on yleensä hieman korkeampi kalsiumin vuoksi.
Monet luonnolliset ympäristöt, kuten ihomme, kasvien kasvualustat ja ravintoalustat, ovat lievästi happamia, ja niiden pH-arvo on 5 ja 6,5 välillä. Jos tarkastelemme asioita, joista ihmiset pitävät, huomaamme, että ne ovat yleensä lievästi happamia tai neutraaleja aineita, kuten vettä. Myös kasvit suosivat lievästi happamia aineita. Noin 5,5:n pH-arvo esiintyy luonnossa niin usein, että jotkut kasviasiantuntijat pitävät tätä arvoa ”neutraalina”.
Miksi happamuus on tärkeää?
Happamuus vaikuttaa merkittävästi useiden ravintoaineiden imeytyvyyteen ja liukoisuuteen (ks. kuvio 1).
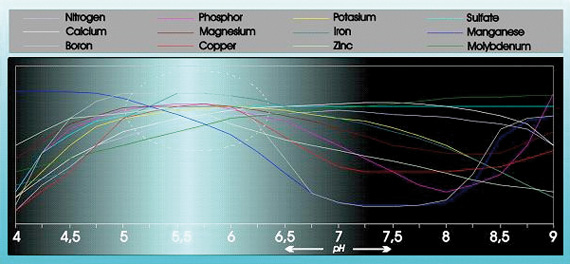
Kuvio 1
Happamuus vaikuttaa lisäksi merkittävästi orgaanisten aineiden rakenteeseen, hajoamiseen ja maaperässä olevaan pieneliöstöön. pH vaikuttaa myös siihen, miten kasvualustassa olevat ruoka-aineet, raskasmetallit, torjunta-aineet ja muut mikro-organismit huuhtoutuvat pois maasta.
Liian matala tai liian korkea pH-arvo voi olla haitallinen kasveille, joten on tärkeää, että se on oikea. Mutta mistä tiedät, milloin pH on väärä? Kokemuksen perusteella! Siksi olemme esittäneet avuksesi joitakin oireita, joita saatat havaita:
Oireita liian alhaisesta pH:sta (kasvualusta on liian hapan)
- Useimmat ravinteet liukenevat helposti, mikä voi aiheuttaa liikaa mangaania, alumiinia ja rautaa;
- Fosforin, kaliumin, magnesiumin ja molybdeenin puute voi johtua liiallisesta huuhtelusta;
- Magnesiumin puute, erityisesti kylmissä kasvualustoissa;
- Multa on yleisesti ottaen huono;
- Mullan elinvoimaisuus on estynyt.
Oireita liian korkeasta pH:sta (kasvualusta on liian emäksinen)
- Useimmat ravinteet liukenevat huonommin, jolloin kalsium-, rauta- ja fosfaattiyhdisteet saostuvat;
- Vähentynyt erityisesti mangaanin, fosfaatin ja raudan, mutta myös kuparin, sinkin ja boorin imeytyminen. Tämä aiheuttaa puutostiloja erityisesti kosteissa ja kylmissä kasvualustoissa.
- Hiekkamailla orgaanisten aineiden hajoaminen lisääntyy huomattavasti, jos pH on korkea.
Mikä määrittää pH:n?
Yksi tärkeimmistä tekijöistä, jotka määräävät pH-arvon liuoksessa tai kasvualustassa, on puskurikyky. Puskurikapasiteetti tarkoittaa tässä tapauksessa sitä, että läsnä on jonkinlainen tasapaino, joka palautuu jatkuvasti. Jos esimerkiksi laitetaan tippa happoa 1 litraan vesijohtovettä, jonka pH on 7, sillä ei ole juurikaan vaikutusta happamuuteen. Jos kuitenkin laitetaan tippa happoa yhteen litraan de-mineralisoitua vettä (akkuvettä), pH laskee välittömästi dramaattisesti. Tämä johtuu siitä, että vesijohtovesi sisältää bikarbonaattia, kun taas de-mineralisoitu vesi ei sisällä. Bikarbonaatti on tärkein puskuriaine veden pH-arvojen ollessa välillä 5,5-7,5.
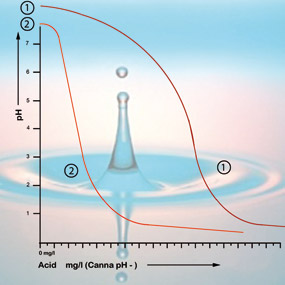 Bikarbonaatti sitoutuu liuoksessa olevaan happoon, joka vapauttaa hiilidioksidia ilmakehään. Näin happo neutraloituu, ja muutokset happamuudessa ovat vain vähäisiä niin kauan kuin bikarbonaattia on vielä läsnä.
Bikarbonaatti sitoutuu liuoksessa olevaan happoon, joka vapauttaa hiilidioksidia ilmakehään. Näin happo neutraloituu, ja muutokset happamuudessa ovat vain vähäisiä niin kauan kuin bikarbonaattia on vielä läsnä.
PH-arvon ollessa 5,3 kaikki bikarbonaatti on käytetty loppuun, eikä liuoksessa ole enää puskuria. pH on nyt epävakaa ja se muuttuu välittömästi, jos siihen lisätään happoa (ks. kuva 2). Bikarbonaattipitoisuuden perusteella voidaan siis laskea happomäärä, joka tarvitaan, jotta syöttöliuoksen happamuus saadaan oikeaksi. Vesijohtoveden bikarbonaattipitoisuuden ilmoittaa yleensä vesilaitos milligrammoina litrassa.
Puskurikapasiteetti ja substraatin happamuus riippuvat sen koostumuksesta ja tuoreudesta. Orgaanisen aineksen, kalsiumin ja bikarbonaatin läsnäolo määrää yleensä pH:n. Savi sisältää aina kalsiumkarbonaattia ja sillä on suhteellisen korkea pH-arvo, jota on vaikea muuttaa, kun taas turve- ja hiekkamaat ovat happamia.
Kasvi itsessään vaikuttaa myös suuresti happamuuteen. Juuret erittävät joko happamia tai emäksisiä aluskasvustoja riippuen kasvin kehitysvaiheesta, saatavilla olevasta ravinnosta, juurten lämpötilaeroista ja valon voimakkuudesta. Ymmärrät siis, miksi juuriympäristön pH voi jatkuvasti vaihdella. Hienostunut ravintotasapaino eri kehitysvaiheiden aikana pitää juuriympäristön pH:n hyväksyttävissä rajoissa.
Mikrobit, hiilidioksidipitoisuus ja leväkasvusto voivat myös vaikuttaa juuriympäristön ja ravinnesäiliön happamuuteen.
PH-arvon mittaaminen

PH-arvon mittaaminen on melko helppoa – tarvitset pH-indikaattoreita, kuten lakmuspaperia tai pH-testauslaitteen. Nämä ovat suhteellisen halpoja, mutta ne eivät ole aina tarkkoja ja voivat joskus poiketa 1-2 pH-yksikköä. Kaikki pH-mittarit ovat yleensä kalliimpia, ja tarkkuus riippuu mittarin tyypistä ja säännöllisestä kalibroinnista kalibrointinesteellä.
Näytteiden ottaminen

Kasvien kasteluun käytettävän veden pH on tärkeä, mutta juurten ympärillä oleva happamuus on olennainen. pH:ta mitattaessa on siis erittäin tärkeää ottaa näyte oikealla tavalla hyvien tulosten saamiseksi. Näytteessä on ikähappoisuus juuren ympäristössä.
Kiertovesijärjestelmässä näytteiden ottaminen ja pH:n mittaaminen on helppoa, yksinkertaisesti mitataan kierrätetty syöttöliuos.
Substraattijärjestelmissä, joissa ei ole kiertovesijärjestelmää, syöttöliuos vedetään substraatista (kivivilla, agrofoam jne.) useista kohdista. Asiantuntijat ovat keskustelleet vuoden ja päivän ajan siitä, mistä näytteet otetaan. Suosittelemme, kuten useat hyvämaineiset laboratoriot tekevät, että näytteet otetaan juurten kohdalta, joka on tippa- persin alta ja ympäriltä. Ottakaa pieniä näytteitä mahdollisimman monesta paikasta. Ota kaikki näytteet aina samaan aikaan ja mieluiten toisen tiputuksen jälkeen valo – päivä – jakson aikana.
 Multa-, kookos- ja turvesubstraateista ota vain pieni määrä substraattia useasta eri paikasta.
Multa-, kookos- ja turvesubstraateista ota vain pieni määrä substraattia useasta eri paikasta.
Voit mitata näytteesi happamuuden parhaiten ”1:1,5 tilavuusuutteen” menetelmällä. Voit tehdä tämän helposti itse tekemällä kasvualustan niin märäksi, että vesi valuu sormien läpi, kun sitä vaivataan ja puristetaan melko voimakkaasti (kuva 1). Käytä esimerkiksi 250 ml:n mittalasia. Täytä mittalasi 150 ml:ksi mineralisoimattomalla vedellä. Lisää kasvualustaa, kunnes tilavuus on 250 ml (kuva 2). Ravista hyvin ja anna seistä muutaman tunnin ajan. Suodata se sitten ja mittaa pH.

Oikeita pH-arvoja jokaiselle kasvualustalle
Kasvattaessasi kasvualustassa pH-arvot välillä 5,0-6,4 ovat juurisympäristön kannalta hyviä. Ei ole haitallisia vaikutuksia, jos arvot ovat hieman korkeammat tai matalammat. Välittömiä haittavaikutuksia ilmenee vain arvoilla, jotka ovat alle 4 ja yli 8. pH-arvo, joka on alle 4, aiheuttaa usein välittömiä vaurioita juurille. Lisäksi raskasmetallit, kuten mangaani ja rauta, imeytyvät niin hyvin, että ne voivat myrkyttää kasvin (nekroosi). Arvot välillä 7 ja 8 eivät ole välittömästi haitallisia kasville. Ravinteita, kuten rautaa, fosfaattia ja mangaania, on silloin vähemmän saatavilla, mikä johtaa pitkällä aikavälillä puutostiloihin (kloroosi ja kehitysongelmat).
PH-arvon korjaaminen
 Jos juuristoympäristön happamuus vaihtelee välillä 5 ja 6,4, niin kasvuympäristösi pH-arvo on kunnossa, eikä sinun tarvitse ryhtyä mihinkään korjaaviin toimenpiteisiin. Yritä välttää pH:n korjaamista, ellei se ole todella välttämätöntä. Siitä on todennäköisesti enemmän haittaa kuin hyötyä; kasvi pitää rauhasta ja hiljaisuudesta. Tärkeämpää on seurata, miten happamuus muuttuu pidemmän ajan kuluessa. Jos arvo laskee alle pH 5:n tai nousee yli pH 6,4:n, on suositeltavaa alkaa vähitellen tehdä säätöjä.
Jos juuristoympäristön happamuus vaihtelee välillä 5 ja 6,4, niin kasvuympäristösi pH-arvo on kunnossa, eikä sinun tarvitse ryhtyä mihinkään korjaaviin toimenpiteisiin. Yritä välttää pH:n korjaamista, ellei se ole todella välttämätöntä. Siitä on todennäköisesti enemmän haittaa kuin hyötyä; kasvi pitää rauhasta ja hiljaisuudesta. Tärkeämpää on seurata, miten happamuus muuttuu pidemmän ajan kuluessa. Jos arvo laskee alle pH 5:n tai nousee yli pH 6,4:n, on suositeltavaa alkaa vähitellen tehdä säätöjä.
Happamuuden korjaaminen onnistuu helpoimmin laskemalla ruokintaliuoksen happamuutta typpihapolla kasvuvaiheessa ja fosforihapolla kukintavaiheessa tai tarvittaessa nostamalla sitä kaustisella kaliumkalvolla, kaliumbikarbonaatilla ja CANNA RHIZOTONICilla. Varmista, että käytettävän liuoksen pH ei laske liian alas alle 5,0:n. Kivivillassa kasvatettaessa kuidut vahingoittuvat, jolloin hyvin alhaisilla pH-arvoilla vapautuu paljon emäksistä ainetta. Lisäksi pH:ta on vaikeampi hallita bikarbonaatin puuttumisen vuoksi
Juuriympäristön korkea pH voi johtua myös kertyneestä bikarbonaatista. Tämän korjaamiseksi ylläpidä 20 %:n salaojitusta tai huuhtele läpi happamammalla liuoksella.
On hyödyllistä merkitä muistiin pH-mittaukset sekä lisätystä liuoksesta että kasvualustassa olevasta ruokintaliuoksesta. Saat hyvän käsityksen pH:n etenemisestä ja tehtyjen toimenpiteiden vaikutuksesta.
- Valkuaista pilkkovat entsyymit tarvitsevat happaman ympäristön (mahanesteet) ja hiilihydraatteja pilkkovat entsyymit emäksisen ympäristön (sylki).
- Liuoksen happamuus määräytyy vetyionien (=happo) ja hydroksidi-ionien (=emäksinen) suhteen perusteella.
- Vajeita voi esiintyä, koska kasvin on eritettävä protoneja voidakseen imeä näitä molekyylejä. Kasvualustassa, jonka pH on alhainen, on jo hyvin paljon protoneja. Nämä alkuaineet myös huuhtoutuvat pois, koska protonit hylkivät molekyylejä kasvualustassa olevasta väliaineesta.
- Bikarbonaatti on aine, joka yhdessä kalsiumin kanssa on vastuussa kalkin muodostumisesta. Yhdessä natriumin kanssa bikarbonaattia käytetään lääkkeissä liiallista mahahappoa vastaan (Alka-seltzer).
- Jotkut laboratoriot työskentelevät myös bikarbonaattikovuuden kanssa. Jotta tämä voidaan muuntaa mg/l bikarbonaatiksi, on bikarbonaattikovuus kerrottava luvulla 21,8.
Esimerkiksi: bikarbonaattikovuus on 11, jolloin 1 litra vettä sisältää (11 x 21.8=) 240 mg/litra bikarbonaattia. -
Hiekkainen maa: Ruohovaltainen maa pH 4.6 … 5.2 Rakennusmaa pH 5.0 … 5.6 Savi: Merensavi pH 6.0 … 7.2 Jokisavi pH 6.2 … 6.4 Savi: Käsittelemätön pH 6.4.0 - Jos levät kasvavat merkittävästi, pH nousee, koska liuoksesta poistuu hiilidioksidia. Bakteerit voivat muuntaa tiettyjä typen muotoja niin, että niillä on happamoittava vaikutus. Suuret hiilidioksidimäärät ilmassa tuottavat enemmän hiilidioksidia ruokintaliuokseen ja päinvastoin.
- Käytä soodaa vain pieniä määriä, koska se sisältää natriumia, ja kasvit tarvitsevat vain hyvin pienen määrän natriumia. Muista, että suuret natriumpitoisuudet vahingoittavat kasveja.
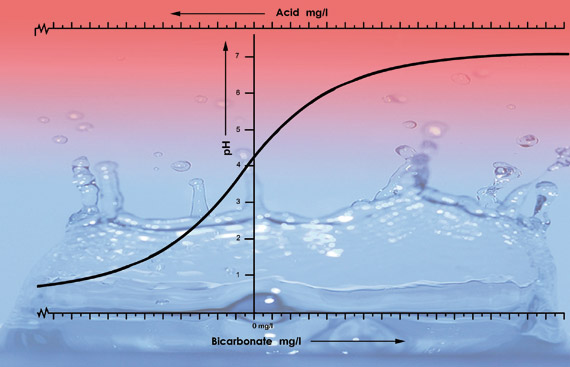
Kuvio eri alueilta peräisin olevan vesijohtoveden pH-arvoista eri bikarbonaattipitoisuuksilla. Kunkin vesityypin 100 litran näytteeseen lisättiin 33 ml typpihappoa (38 %). pH-käyrä laskee nopeammin pH 5,3:n jälkeen, koska tämäntyyppisessä vedessä happo neutraloi kaiken bikarbonaatin. Alle pH 5,3:n happamuus kiihtyy nopeasti.
Kiertovesijärjestelmissä pH-arvo voi vaihdella enemmän kuin run-to-waste-järjestelmissä. Sama pätee myös EC, ppm-arvoon. Jos haluat lisätietoja EC:stä, pH:sta ja ppm:stä, suosittelemme lukemaan artikkelin Kaikki EC:stä, pH:sta ja ppm:stä AQUA:n avulla.