Proces izobaryczny to zmiana stanu pewnej ilości materii w procesie termodynamicznym, w którym ciśnienie pozostaje stałe. To, co może się zmienić, to jedna lub więcej zmiennych stanu. Jeśli do układu przekazywane jest ciepło, wykonywana jest praca i zmienia się również energia wewnętrzna układu.
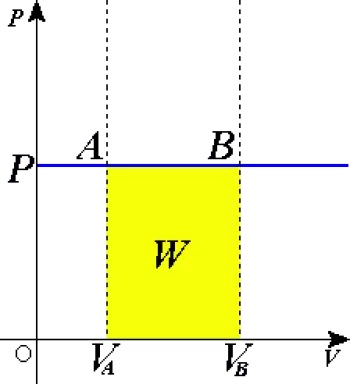
Na wykresie ciśnienie-objętość prowadzi linię poziomą zgodnie z prawem gazu idealnego.
Procesem izobarycznym rządzi prawo Charlesa. Zgodnie z prawem Charlesa, dla stałej masy gazu idealnego przy stałym ciśnieniu, objętość jest wprost proporcjonalna do temperatury Kelvintemperatury.
Procesy izobaryczne są regulowane przez pierwsze prawo termodynamiki. W procesach tych przyrost energii jest równy przyrostowi entalpii pomniejszonej o ciśnienie pomnożonej przez przyrost objętości:ΔE = ΔH – P – ΔV.
Nie należy mylić z procesami izotermicznymi, które przebiegają przy stałym ciśnieniu, ani z procesami adiabatycznymi, w których nie następuje wymiana ciepła. W tych procesach może nastąpić zmiana ciśnienia. Gdy proces przebiega w stałej objętości, nazywa się procesem izochorycznym.
Przykłady procesów izobarycznych
Aby lepiej zrozumieć ten proces termodynamiczny, pomoże nam obejrzenie kilku przykładów.
-
Faza rozprężania cylindra silnika.
-
Przygotowanie wody w otwartym naczyniu.
-
Ogrzewanie się kuli ziemskiej wskutek działania promieniowania słonecznego.
-
Balony na ogrzane powietrze eksperymentują z procesem izobarycznym i izochronicznym.
Ogrzewanie się powietrza w balonie
Zmiana objętości, jakiej doświadcza balon w miarę uderzania w niego promieni słonecznych, jest przykładem procesu izobarycznego. Podczas gdy słońce zwiększa temperaturę, objętość gazu (powietrza) doświadcza izobarycznej ekspansji.
Na początku poranka prezentuje ona pewne ciśnienie, objętość i temperaturę, w miarę jak powietrze w niej się ogrzewa, ciśnienie wzrasta, ale nie zmienia się ono z powodu wzrostu jej objętości.
Faza rozprężania cylindra w silniku cieplnym
Cylinder w silniku cieplnym może być rozszerzany lub kurczony w zależności od fazy cyklu. Rozszerzanie powietrza w cylindrze z ruchomym tłokiem, do którego dostarczane jest ciepło, odbywa się w procesie izobarycznym. W ten sam sposób, podczas sprężania, objętość zmniejsza się izobarycznie.
Objętość będzie wzrastać proporcjonalnie do jego temperatury, a ciśnienie pozostanie stałe. Jest to zgodne z prawem Charlesa.
Wrząca woda w otwartym pojemniku
Powszechnym przykładem procesu izobarycznego jest wrząca woda w otwartym pojemniku. Poprzez dostarczenie energii cieplnej do wody, jej temperatura wzrasta i zamienia się w parę wodną.
Uzyskana para wodna ma wyższą temperaturę i zajmuje większą objętość, jednak ciśnienie pozostaje stałe. Od początku ciśnienie jest równe ciśnieniu atmosferycznemu.
Podgrzewanie balonu na gorące powietrze
Podgrzewanie balonu na gorące powietrze jest przykładem procesu izobarycznego.
Balony na gorące powietrze działają, ponieważ gorące powietrze unosi się do góry. Poprzez ogrzewanie powietrza wewnątrz balonu za pomocą palnika, staje się ono lżejsze niż chłodniejsze powietrze na zewnątrz. Powoduje to unoszenie się balonu do góry, tak jakby znajdował się w wodzie.
Ciśnienie wewnątrz balonu jest takie samo jak ciśnienie atmosferyczne. Kiedy pilot wstrzykuje ciepło do powietrza, jego temperatura wzrasta. Powoduje to zmniejszenie gęstości powietrza i z powodu różnicy między gęstością powietrza a jego gęstością balon unosi się w górę.
Termodynamicznie, część ciepła jest zamieniana na pracę, dzięki czemu balon na gorące powietrze unosi się w górę. Część tego ciepła jest uwalniana na zewnątrz układu z powodu termodynamicznego kontaktu powietrza zewnętrznego oraz z powodu utraty gorącego powietrza podczas jego rozprężania.
W 1-2 = P ( V 2 – V 1 ) W 1-2 = n R ( T 2 – T 1 ) Q 1-2 = m c p ( T 2 – T 1 ) Q 1-2 = ( k / ( k -1)) P ( V 2 – V 1 )
Where,
-
W 1-2 ilość pracy wykonanej w wyniku zmiany stanu
-
Q 1-.2 ilość ciepła dostarczonego lub usuniętego
-
P ciśnienie
-
V objętość
-
T temperatura bezwzględna
-
n ilość pyłu (zwykle wyrażana w molach)
-
m3.
-
m masa substancji
-
cp ciepło właściwe substancji przy stałym ciśnieniu
-
k to stosunek równy ilorazowi ciepła właściwego przy stałym ciśnieniu i stałej objętości, odpowiednio
Z pierwszego równania wynika, że jeżeli układ rozszerza się (ΔV jest dodatnie), to układ wykonuje dodatnią pracę. Przeciwnie, jeśli przyrost objętości jest ujemny, układ kurczy się i praca jest ujemna.
Równanie stanu gazu idealnego
Równanie stanu gazu idealnego (czasami równanie Mendelejewa – Clapeyrona lub równanie Clapeyrona) jest wzorem, który określa związek między ciśnieniem, objętością molową i temperaturą bezwzględną gazu idealnego. Równanie ma postać:
pV = nRT
gdzie,
p – ciśnienie,
V- objętość gazu,
n- ilość gazu,
R – uniwersalna stała gazowa , R ≈ 8,314 J / (mol⋅K),
T – temperatura termodynamiczna, K kelwinów.