A diabetes mellitus költséges, de a legtöbb költséget a szövődmények és a kórházi ellátás okozza.1 Az Amerikai Diabétesz Szövetség (ADA) szerint 2012-ben a cukorbetegség becsült összköltsége 245 milliárd dollár volt.1 Ennek 43%-át a kórházi fekvőbeteg-ellátás költségei tették ki, további 18%-át pedig a cukorbetegség szövődményeinek kezelésére szolgáló receptek.1
A legtöbb ilyen szövődmény megelőzhető célzott glükózszabályozással. Az epidemiológiai adatok azt mutatják, hogy a hemoglobin A1c (HbA1c) minden egyes százalékpontos csökkenése esetén 35%-kal csökken a mikrovaszkuláris szövődmények kockázata.2 Jó hír, hogy a cukorbetegség szövődményeinek aránya csökkent,3 de ezt felülmúlta a szövődményekkel előrehaladó cukorbetegek számának puszta növekedése.
Sok 2-es típusú cukorbetegnél a diagnózis felállításakor már jelentkezhet cukorbetegséggel kapcsolatos szövődmény. Mind az 1-es, mind a 2-es típusú cukorbetegségben a szövődmények egy része, mint például a retinopátia és a nefropátia, néma. Ez agresszív célzott megközelítést igényel, mert a tünetekre várva már túl késő lesz. Még a diabéteszes neuropátia is tünetmentes lesz a mérhető eltérésekkel rendelkező emberek akár 50%-ánál.4
Ez a cikk áttekinti az ADA 2017-es ellátási standardjainak a mikrovaszkuláris szövődményekre vonatkozó ajánlásait és a vonatkozó állásfoglalásokat, valamint kiemeli a megelőző szűrővizsgálatokat és a klinikai gyöngyszemeket a cukorbetegeket kezelő alapellátó orvos számára.
- Diabéteszes retinopátia
- 1. táblázat. Retinopátia stádiumai leírással
- Klinikai gyöngyszemek
- Diabeteses vesebetegség
- 2. táblázat. Válogatott mérföldkőnek számító tanulmányok, amelyek 7% alatti A1c értékkel bizonyítják a glikémiás kontrollt
- 3. táblázat. Becsült GFR stádiummal és leírással
- 4. táblázat. Albuminuria-kategóriák CKD-ben
- 1. ábra. A kiértékelés javasolt gyakorisága (évenkénti gyakoriság) eGFR és albuminuria kategória szerint
- 5. táblázat. Nem diabéteszes glomeruláris betegségre utaló vörös zászlók
- 6. táblázat. A glükózcsökkentő szerek dózismódosításai és ajánlásai veseelégtelenségben szenvedő betegeknél
- Class
- Medicina
- Klinikai gyöngyszemek
- Diabéteszes perifériás neuropátia
- 7. táblázat. A neuropátia egyéb okai67
- 8. táblázat. Gyakran alkalmazott farmakológiai szerek a DPN kezelésére4,69
- Klinikai gyöngyszemek
- Gasztroparézis
- Klinikai gyöngyszemek
- Diabéteszes cheiroarthropathia
- Következtetés
Diabéteszes retinopátia
A diabéteszes retinopátia az 1-es és 2-es típusú cukorbetegség gyakori mikrovaszkuláris szövődménye. Becslések szerint világszerte 3,7 millió ember látása mérsékelten vagy súlyosan károsodott a diabéteszes retinopátia miatt, és világszerte több mint 800 000 ember vak a diabéteszes retinopátia miatt.5 Ez a leggyakoribb oka az újonnan jelentkező vakságnak a 20-74 év közötti felnőttek körében.6 Erős összefüggéseket állapítottak meg a glikémiás kontrollal, a vérnyomás-szabályozással és a betegség időtartamával. Korai, rendszeres szűréssel és e kockázati tényezők ellenőrzésével a diabéteszes retinopátia felismerhető és kezelhető a látáskárosodás megelőzése érdekében.
A diabétesz időtartama a diabéteszes retinopátia progressziójának legnagyobb kockázati tényezője. Az 1-es típusú cukorbetegségben a retinopátia az első 3-5 évben vagy a pubertás előtt ritka.7 A következő 20 évben majdnem minden 1-es típusú cukorbetegségben szenvedő betegnél kialakul a diabéteszes retinopátia.7 A 2-es típusú cukorbetegségben szenvedő betegek 21%-ánál a diagnózis felállításakor valamilyen fokú retinopátia alakul ki.7 A krónikus hiperglikémia, a nefropátia, a magas vérnyomás és a diszlipidémia olyan további tényezők, amelyek növelik a diabéteszes retinopátia kockázatát, vagy összefüggésbe hozhatók vele.8 Az albuminuriás betegek akár 50%-ánál (függetlenül a becsült glomeruláris filtrációs ráta szintjétől) retinopátia alakul ki.9 Az 1. táblázat a retinopátia különböző stádiumait ismerteti.
1. táblázat. Retinopátia stádiumai leírással |
|
|
Stádium |
leírás |
|
Enyhe Nem…Proliferatív diabéteszes retinopátia |
Mikroaneurizmák jelenléte |
|
Mérsékelt nem proliferatív diabéteszes retinopátia |
Mikroaneurizmák, retinalis pont- vagy foltos vérzések, kemény exsudátumok, vagy vattás foltok lehetnek jelen |
|
Súlyos nem proliferatív diabéteszes retinopátia |
Hálóhártyán belüli vérzések, vénás gyöngyözés, vagy intraretinalis mikrovaszkuláris eltérések lehetnek jelen |
|
Proliferatív diabéteszes retinopátia |
Neovaszkularizáció, üvegtesti vagy preretinalis vérzések jelenléte |
Patofiziológia. A fokozott éráteresztőképességgel jellemezhető enyhe, nem proliferatív eltérések közepes vagy súlyos nem proliferatív diabéteszes retinopátiává (NPDR) fejlődhetnek.7 A proliferatív diabéteszes retinopátiát új retinális erek proliferációja jellemzi.7 A makulaödéma, amely a retina központi megvastagodása exsudációval és ödémával, a retinopátia bármely stádiumában jelentkezhet.7 A diabéteszes retinopátiát felgyorsíthatja a terhesség, a pubertás, a glikémiás kontroll hiánya, a magas vérnyomás és a szürkehályogműtét.7
A diabéteszes retinopátia megelőzése. A diabéteszes retinopátia megelőzésének kulcsa a glikémiás kontroll. A Diabetes Control and Complications Trial (DCCT) vizsgálatban a kutatók értékelték a szoros glikémiás kontroll és a kiinduláskori retinopátia hiányától vagy minimális retinopátiától a mérsékelt NPDR-ig terjedő progresszió hatását.10 Az intenzív terápiás csoportba tartozó, kiinduláskor retinopátiával nem rendelkező betegek esetében a retinopátia átlagos kockázata 36 hónap alatt 76%-kal csökkent.10 Az intenzív terápiás csoportban azoknál a betegeknél, akiknél már minimális vagy közepes mértékű NPDR jelentkezett, a progresszió kockázata 54%-kal csökkent a hagyományos kezelést alkalmazókhoz képest.10 Az eredeti Action to Control Cardiovascular Risk in Diabetes (ACCORD) vizsgálatban a 10 éve 2-es típusú cukorbetegségben szenvedő, ismert kardiovaszkuláris betegségben szenvedő résztvevőket a glikémia, a szisztolés vérnyomás és a diszlipidémia tekintetében intenzív vagy standard terápiára randomizálták. Négy évvel később a retinopátia progressziója csökkent azoknál, akik korábban intenzív glikémiás kontrollt kaptak, függetlenül a hasonló aktuális HbA1c-szintektől.11 Hasonló örökségi hatást nem tapasztaltak azokban a csoportokban, amelyek intenzív vérnyomáskontrollt vagy fenofibrátot kaptak a diszlipidémia kezelésére.11
Szűrés. Mivel a makulaödéma és a proliferatív diabéteszes retinopátia tünetmentes lehet, a szűrés létfontosságú a korai felismerés és kezelés szempontjából. Az 1-es típusú cukorbetegek esetében a szűrést a diagnózis felállítása után öt évvel kell elkezdeni.8 A 2-es típusú cukorbetegek esetében a szűrést a diagnózis felállításakor kell elkezdeni.8 A szűrést a diabéteszes retinopátiában jártas szemésznek vagy optometristának kell elvégeznie. A szűrést tágított szemmel kell elvégezni. Ha a retinopátia már jelen van, ajánlott szemészorvoshoz irányítani.8 Az ismételt vizsgálatot évente el kell végezni, ha minimális vagy semmilyen betegséget nem találnak.8
A terhesség a proliferatív retinopátia nagy kockázatú időszaka. Az 1-es vagy 2-es típusú cukorbetegségben szenvedő terhes nőknél a szemvizsgálatot a fogamzás előtt vagy az első trimeszterben kell elvégezni. A vizsgálatokat minden trimeszterben és a szülés után egy éven át meg kell ismételni.8 A terhességi cukorbetegek esetében a szülés után nincs szükség további szemészeti vizsgálatokra.
A terhesség a már meglévő 1-es vagy 2-es típusú cukorbetegségben szenvedő betegeknél a diabéteszes retinopátia gyors progresszióját eredményezheti. Ez különösen akkor igaz, ha a fogantatás idején rossz a glikémiás kontroll.14 Azokat a cukorbeteg nőket, akik terhesek vagy tervezik a teherbeesést, fel kell világosítani a diabéteszes retinopátia kialakulásának vagy progressziójának kockázatáról és a glikémiás kontroll szükségességéről a fogantatás előtt.8 A retinopátia korai romlása azonban az intenzív glikémiás kezelés gyors bevezetésével is bekövetkezhet, ha a retinopátia már jelen van.8 Úgy tűnik, hogy a terhességi cukorbetegség nem jár a diabéteszes retinopátia terhesség alatti kialakulásának azonos kockázatával.8
Kezelés. A glikémiás kontroll mellett a vérnyomás kontrollja (< 140 mmHg szisztolés vérnyomás) is csökkenti a diabéteszes retinopátia progresszióját, de a < 120 mmHg szisztolés vérnyomás szoros kontrollja nem jelent további előnyt.12 A fenofibrát szintén lassíthatja a diabéteszes retinopátia progresszióját, különösen nagyon enyhe NPDR esetén, diszlipidémiás betegeknél.13 Az aszpirinről kimutatták, hogy nincs hatással a retinopátia progressziójára, az üvegtestvérzés kialakulására vagy az üvegtestvérzés időtartamára, és biztonságosan alkalmazható más orvosi indikációkban, szemészeti veszélyeztetés nélkül.7
A cukorbetegek kezelésének tartalmaznia kell a testmozgásra vonatkozó ajánlásokat. Az enyhe, nem proliferatív retinopátiában szenvedők biztonságosan elkezdhetik a fizikai aktivitást. A közepesen súlyos, nem proliferatív retinopátiában szenvedő betegeknek azonban kerülniük kell a vérnyomást nagymértékben megemelő tevékenységeket, például az erőemelést.15 A súlyos, nem proliferatív vagy instabil retinopátiában szenvedő betegeknek kerülniük kell minden erőteljes fizikai tevékenységet (ugrás, rázkódás), minden fejjel lefelé irányuló tevékenységet és a légzés visszatartását.15 Üvegtestvérzés esetén nem szabad sportolni.15
A diabéteszes retinopátia korai felismerése azért fontos, mert a kezeléssel megelőzhető vagy visszafordítható a látásromlás. A Diabetic Retinopathy Study (DRS) során a kutatók megállapították, hogy a fotokoagulációs műtét a diabéteszes retinopátia hatékony kezelése. Az Early Treatment Diabetic Retinopathy Study és a DRS azt mutatta, hogy a fotokoaguláció csökkentette a látásvesztés kockázatát, a legnagyobb előnnyel azoknál a betegeknél, akiknél a kiindulási betegség előrehaladottabb volt.16,17 A jelenlegi adatok azt bizonyítják, hogy az intravitreális antivaszkuláris endoteliális növekedési faktor (anti-VEGF) szerek hatékonyabbak a makulaödéma kezelésében, mint a monoterápia vagy a lézeres koagulációval kombinált kezelés.8 Emellett az anti-VEGF javíthatja a látást, míg a fotokoaguláció csak a további látásvesztést akadályozza meg.18,19 Az anti-VEGF egyik hátránya, hogy az első 12 hónapban havi intravitreális terápiát igényel.
Klinikai gyöngyszemek
- A korai diabéteszes retinopátiának nincsenek specifikus jelei vagy tünetei.
- A diabéteszes retinopátia szűrésére a következő betegeknél kell sort keríteni:
– 1. típusú cukorbetegségben szenvedő betegeknél öt évvel a diagnózis után.
– 2. típusú cukorbetegségben szenvedő betegeknél a diagnózis felállításakor.
- Tanácsadást és fokozott vizsgálatot kell biztosítani azoknak a cukorbeteg nőknek, akik terhességet terveznek vagy teherbe esnek, mert a diabéteszes retinopátia a terhesség alatt gyorsan felgyorsulhat.
- A diabéteszes retinopátia kialakulását szoros glikémiás és vérnyomás-szabályozás (< 140 mmHg szisztolés) megelőzheti.
- Az albuminuriás betegek akár 50%-ánál (függetlenül az eGFR szintjétől) retinopátia alakul ki.9
- A fotokoagulációs kezelés megakadályozhatja a betegség progresszióját, és az anti-VEGF kezelés visszafordíthatja a makulaödéma okozta látásvesztést.
Diabeteses vesebetegség
A diabéteszes vesebetegség (DKD), az ADA által preferált terminológia, a krónikus vesebetegség (CKD) vezető oka az Egyesült Államokban.20,21. A DKD jelentős hosszú távú hatással van a cukorbetegek életminőségére, és a végstádiumú vesebetegségek (ESRD) akár 40%-áért is felelős.20 A National Kidney Foundation’s Kidney Disease Outcomes Quality Initiative (KDOQI) és az ADA 2017-es ellátási standardjai alapján ez a szakasz a DKD-s betegek HbA1c-célszintjére, gyógyszeres kezelésére és terápiás kezelésére vonatkozó útmutatást nyújt.
A KDOQI a HbA1c-célszintet a beteg hipoglikémia kockázata és a társbetegségek alapján rétegzi. Ez a kezdeményezés három olyan publikáción alapul, amelyek bizonyítják, hogy a 7% alatti HbA1c-értékkel történő glikémiás kontroll megelőzi vagy csökkenti a vesebetegség progresszióját 2-es típusú cukorbetegségben szenvedő betegeknél.22,23,24 Ezeket a tanulmányokat a 2. táblázat foglalja össze. Az ADA azt ajánlja, hogy a hipoglikémia szempontjából fokozottan veszélyeztetett betegeknél a cél HbA1c-t 7% fölé kell emelni.8 A KDOQI azt javasolja, hogy a 4. és 5. stádiumú CKD-ben szenvedő, korlátozott életkilátásokkal rendelkező betegek tartsák a 7% feletti HbA1c-t.25
2. táblázat. Válogatott mérföldkőnek számító tanulmányok, amelyek 7% alatti A1c értékkel bizonyítják a glikémiás kontrollt |
|
|
Kísérlet |
Eredmények |
|
A diabétesz és érbetegségek kezelésében: Preterax and Diamicron Modified Release Controlled Evaluation (ADVANCE) Trial22 |
21%-os csökkenés az új makroalbuminuria és a vesepótló terápia 7% alatti A1c-vel |
|
Veterans Affairs Diabetes Trial (VADT)23 |
37%-os csökkenés a makroalbuminúria és a 32%-os csökkenés a mikroalbuminuriában 7% alatti A1c-vel |
|
Az ACCORD (Action to Control Cardiovascular Risk in Diabetes) vizsgálat24 |
2%-os csökkenés a makroalbuminuriában és 21%-os csökkenés a mikroalbuminuriában 7% alatti A1c-vel |
Epidemiológia. A férfiak és a nők egyformán érintettek a DKD-ben.20 A DKD kialakulásának csúcseseménye 15 évvel a diagnózis felállítása után következik be.21 Az afroamerikaiaknál háromszor-ötször nagyobb valószínűséggel alakul ki diabéteszes nefropátia, mint a kaukázusiaknál.20 A mexikói amerikaiak és a Pima indiánok esetében szintén nagyobb a DKD kialakulásának kockázata.20
A proteinuria a kardiovaszkuláris morbiditás és a teljes halálozás előrejelzője cukorbetegségben.21 A DKD megléte a kardiovaszkuláris betegségek fokozott kockázatának tényezője. A DKD-ben szenvedő betegeknél következetesen magasabb a szív- és érrendszeri betegségek okozta halálozás.26 Emellett a DKD-ben szenvedő betegeknél magasabb a teljes halálozás.21
Az 1-es típusú cukorbetegségben a mikrovaszkuláris szövődmények, mint például a DKD, körülbelül 10-20 évvel a diagnózis után kezdenek kialakulni; a 2-es típusú cukorbetegségben a pontos kezdet gyakran ismeretlen, ezért korábbi szűrést indokol.27
Patofiziológia és patogenezis. Úgy gondolják, hogy a hiperglikémia három fő szövettani változást idéz elő a glomerulusokban, amelyek DKD-hez vezetnek: 1) mesangialis expanzió, 2) a glomeruláris bazális membrán megvastagodása és 3) glomeruláris szklerózis.28 Bár a DKD kialakulásának pontos patogenezise ismeretlen, úgy gondolják, hogy a hiperglikémia kezdetben a szövettani változások és a citokinek aktivációja következtében hiperszűrődést és vesekárosodást okoz.20 Jellemzően az albuminuria lehet a DKD első jele.29
Ez tovább súlyosbodik a hyperlipidaemia, az arterioszklerózis, a magas vérnyomás és az elhízás komorbid állapotai következtében, amelyek mind hozzájárulnak a vesekárosodáshoz és az azt követő funkciócsökkenéshez. A centrális elhízás a renin-angiotenzin-aldoszteron rendszer és a szimpatikus idegrendszer hiperaktiválása révén magas vérnyomáshoz vezet.20 Továbbá, ahogy a veseérrendszer arterioszklerotikussá válik, a diabéteszes nefropátia fokozott progressziója következik be. A diabéteszes nefropátia fontos megkülönböztető jegye a CKD más formáihoz képest, hogy a glomerulusok és a vesék kezdetben általában normálisak vagy megnövekedett méretűek.20
Klasszifikáció. Mind az eGFR-t, mind az albuminuria jelenlétét használják a CKD stádiumának meghatározására.30,31 Az eGFR a faj, az életkor, a nem, a testsúly és a szérum kreatininszintek alapján kerül meghatározásra. (Lásd a 3. táblázatot.) Történelmileg a mikroalbuminuria kifejezést használták a mérsékelten emelkedett albuminszintek meghatározására. A National Kidney Foundation ma már az “enyhe”, “mérsékelten” vagy “súlyosan emelkedett” kifejezések használatát ajánlja az albuminuria szintjének leírására a 4. táblázatban ábrázolt szintek alapján.31 Az albumin-kreatinin arány az albuminuria kimutatására használt kezdeti vizsgálat.
3. táblázat. Becsült GFR stádiummal és leírással |
||||
|
Stádium |
GFR (ml/perc per 1.73 m2) |
leírás |
||
|
90+ |
Glomeruláris hyperfiltráció |
|||
|
Enyhén csökkent vesefunkció |
||||
|
3A |
Mértékesen csökkent vesefunkció |
|||
|
3B |
||||
|
Súlyosan csökkent vesefunkció |
||||
|
< 15 vagy dialízisre szorul |
vég-stádiumú veseelégtelenség |
|||
4. táblázat. Albuminuria-kategóriák CKD-ben |
|||
|
Kategória |
Albumin-to-Kreatinin szint |
leírás |
|
|
A1 |
< 30 |
Normális vagy enyhén emelkedett |
|
|
A2 |
Mértékletesen fokozott |
||
|
A3 |
> 300 |
Súlyosan fokozott |
|
A két osztályozási séma a CKD kialakulásának kettős útját mutatja be. Az egyik a kreatinin emelkedésén és a GFR romlásán keresztül. A másik az albuminuria kialakulásán keresztül. A növekvő albuminuriát gyakran követi az eGFR csökkenése;32 ez azonban angiotenzin-konvertáló enzim (ACE) gátlók vagy angiotenzinreceptor-blokkolók (ARB) alkalmazásával és glikémiás kontrollal megelőzhető. (Lásd az 1. ábrát.)
1. ábra. A kiértékelés javasolt gyakorisága (évenkénti gyakoriság) eGFR és albuminuria kategória szerint
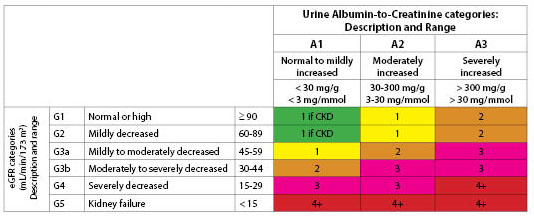
Reprinted with permissioned from Kidney Disease: Improving Global Outcomes (KDIGO).
Common Symptoms. A legtöbb embernek nincsenek tünetei a diabéteszes nefropátiától. Gyakran előfordul, hogy a betegeknél más mikrovaszkuláris szövődményekre utaló jelek vannak, vagy azokat diagnosztizálják.20 A korai DKD jellemzően tünetmentes. A DKD késői lelete a habos vizelet. Továbbá, ha a beteg súlyosan hypoalbuminémiás, pedális ödéma és fáradékonyság jelentkezhet nála.20 A DKD-s betegeknek jellemzően szisztémás hipertóniájuk van. A diabéteszes nefropátiában szenvedő betegeknél jellemzően retinopátia és neuropátia is jelentkezik.8
Diagnosztikai lehetőségek. Mivel nincsenek tünetek, a rutinszerű szűrés kritikus. Az ADA a vizelet albumin-kreatinin arányának éves szűrését ajánlja.8 Ezen kívül legalább évente vizsgálni kell az eGFR-t az öt éve fennálló 1-es típusú cukorbetegségben szenvedő betegeknél, valamint minden 2-es típusú cukorbetegségben szenvedő vagy komorbid magas vérnyomásban és cukorbetegségben szenvedő betegnél.8 Nincs egyértelmű ajánlás a képalkotó eljárások, például ultrahangvizsgálat elvégzésére a DKD diagnózisához.
Differenciáldiagnózis. Néhány vörös zászlós jel arra utalhat, hogy nem a cukorbetegség az egyetlen oka a CKD-nek. Ha egy személynek előrehaladott CKD-je van más mikrovaszkuláris szövődményekre utaló jelek nélkül, ez figyelmeztető jel. A hirtelen (kevesebb mint öt évvel a cukorbetegség kialakulása után) jelentkező, diszmorf vörösvértesteket és gipszeket tartalmazó vizeletüledék vagy a GFR hirtelen csökkenése nem diabeteses etiológiájú vesebetegségre utal.20 Szérum- vagy vizeletelektroforézist lehet végezni, ha fennáll a myeloma multiplexre való gyanú. Az albuminuria hiánya csökkent eGFR és cukorbetegség mellett a CKD DKD-től eltérő egyéb okok kivizsgálását igényli.21 Az 5. táblázat felsorolja a nem diabeteses glomeruláris betegségre utaló vörös zászlókat.
5. táblázat. Nem diabéteszes glomeruláris betegségre utaló vörös zászlók
- A proteinuria kezdete < 5 évvel az 1-es típusú cukorbetegség dokumentált kezdetétől vagy a vesebetegség akut kezdetétől
- Az eGFR akut csökkenése; diabéteszes nefropátia
- Diszmorf vörösvérsejteket vagy sejtes gipszeket tartalmazó vizeletüledék
- Más mikrovaszkuláris szövődmények, például neuropátia vagy retinopátia hiánya
- Más szisztémás betegség jelei és/vagy tünetei
Kezelés. A diabetes nephropathia jellemzője a glükóz, a sócsökkentés, a vérnyomás és a diszlipidémia kezelése. Továbbá a betegeknek kerülniük kell a nefrotoxikus gyógyszereket és táplálékkiegészítőket, például az aminoglikozidokat és a nem szteroid gyulladáscsökkentőket. A betegeket IV. stádiumú vesebetegség esetén vagy a vesefunkció gyors csökkenése esetén nefrológushoz kell irányítani. A beutalás egyéb indikációi az eset összetettségétől függnek. A cukorbetegség újabb orális gyógyszerei segíthetnek megelőzni a veseelégtelenség progresszióját.
Glikémiás kontroll. A gyógyszerek kiválasztása, ellenőrzése és a farmakológia mind befolyásolják a diabéteszes nefropátiában szenvedő betegeket. Ahogy a beteg eGFR-je csökken, egyes orális szerek dózismódosításra szorulnak. A cukorbetegségben és előrehaladott CKD-ben szenvedő betegek glükózszabályozásának központi terápiája továbbra is az inzulin marad.31 A 6. táblázat mutatja az antiglikémiás gyógyszerek ajánlott dózismódosításait vesebetegségben szenvedő betegeknél. 2016-ban mind az empagliflozinról, mind a canagliflozinról kimutatták, hogy csökkenti a CKD progresszióját és a mikroalbuminuriát.33,34 Az empagliflozin csökkentette a nefropátia progressziójának arányát és a súlyos nemkívánatos kardiovaszkuláris események kockázatát a placebóval összehasonlítva, amikor a standard 2-es típusú diabéteszes kezeléshez adták hozzá a mérföldkőnek számító Empagliflozin Cardiovascular Outcome Event Trial in Type 2 Diabetes Mellitus Patients (EMPA-REG) eredményvizsgálatban.33
6. táblázat. A glükózcsökkentő szerek dózismódosításai és ajánlásai veseelégtelenségben szenvedő betegeknél |
||
|
Glükóz-…csökkentő szerek |
Adagolás beállítása veseelégtelenség esetén |
|
Class |
Medicina |
|
|
Biguanidok |
Metformin |
eGFR 30-45 ml/min/1.73 m2: Nem ajánlott a terápia megkezdése. Ha a terápia megkezdése után, értékelje a terápia folytatásának előnyeit/kockázatait. eGFR < 30 mL/min/1,73 m2: Használata ellenjavallt |
|
Szulfonylureák |
Glimepirid |
Enyhe vagy közepes mértékű károsodás: Kezdje napi egyszeri 1 mg-os adagolással Súlyos károsodás: Használata ellenjavallt |
|
Glipizid |
Extended-release: Kezdje napi egyszeri 2,5 mg-os adagolással |
|
|
Gliburid |
eGFR < 60 ml/min/1,73 m2: Használata nem ajánlott |
|
|
Meglitinidek |
Nateglinid |
Nem. dózisbeállítás szükséges |
|
Repaglinid |
CrCl 20-40 ml/perc: Kezdetben 0.5 mg étkezés közben CrCl < 20 mL/min: Nincs információ |
|
|
Tiazolidindionok |
Pioglitazon |
Nincs dózisbeállítás. szükséges |
|
Roziglitazon |
Nem szükséges az adagolás módosítása |
|
|
α-Glükozidáz gátlók |
Akarbóz |
SCr > 2.0 mg/dl: alkalmazása nem ajánlott |
|
Miglitol |
CrCl < 25 ml/perc vagy SCr >2.0 mg/dl: alkalmazása nem ajánlott |
|
|
DPP-4-gátlók |
Alogliptin |
CrCl 30-60 ml/min: 12.5 mg naponta egyszer CrCl < 30 mL/min: 6,25 mg naponta egyszer Hemodialízist igénylő RESRD: 6.25 mg naponta egyszer, és a hemodialízis időzítésére való tekintet nélkül adandó |
|
Linagliptin |
Nincs szükség az adagolás módosítására |
|
|
Saxagliptin |
CrCl ≤ 50 ml/min: 2.5 mg naponta egyszer Hemodialízist igénylő ESRD: 2.5 mg naponta egyszer és hemodialízist követően adandó |
|
|
Sitagliptin |
CrCl 30-50 mL/min: 50 mg naponta egyszer CrCl < 30 mL/min: 25 mg naponta egyszer ESRD, amely hemodialízist vagy peritoneális dialízist igényel: 25 mg naponta egyszer és a hemodialízis időzítésére való tekintet nélkül adható |
|
|
Vildagliptin |
CrCl < 50 mL/min: 50 mg naponta egyszer |
|
|
Éjsav-szekvenstriensek |
Colesevelam |
Nem szükséges az adagolás módosítása |
|
Dopamin-2 agonisták |
Bromokriptin |
Nincs információ |
|
SGLT-2 gátlók |
Canagliflozin |
eGFR 45-60 ml/min/1.73 m2: Ne lépje túl a napi egyszeri 100 mg-ot eGFR < 45 mL/min/1,73 m2: Nem ajánlott a terápia megkezdése. Ha a kezdés után a terápia abbahagyása olyan betegeknél, akiknél az eGFR tartósan < 45 ml/perc/1,73 m2. eGFR < 30 ml/perc/1,73 m2/ESRD/Hemodialízis: Használata ellenjavallt |
|
Dapagliflozin |
eGFR < 60 ml/perc/1,73 m2: Nem ajánlott a terápia megkezdése. Ha a kezelés megkezdése után a terápia abbahagyása olyan betegeknél, akiknek eGFR-je tartósan 30 és < 60 mL/min/1,73 m2 között van. eGFR < 30 mL/min/1,73 m2/ESRD/Hemodialízis: Használata ellenjavallt |
|
|
Empagliflozin |
eGFR < 45 ml/perc/1,73 m2: Nem ajánlott a terápia megkezdése. Ha a terápia megkezdése után tartósan < 45 ml/perc/1,73 m2 eGFR-rel rendelkező betegeknél a terápia abbahagyása. eGFR < 30 ml/perc/1,73 m2. ESRD/ Hemodialízis: Használata ellenjavallt |
|
|
GLP.1 receptor agonisták |
Albiglutid |
Nincs szükség az adagolás módosítására |
|
Dulaglutid |
Nincs szükség dózisbeállításra |
|
|
Exenatid |
CrCl 30-50 ml/min: Nincs információ. Óvatosan alkalmazható. CrCl < 30 ml/min/ESRD: Használata nem ajánlott |
|
|
Liraglutid |
Nincs információ |
|
|
Lixisenatid |
eGFR 15-29 ml/min/1.73 m2: Nincs információ. Figyelni kell a fokozott gyomor- és bélrendszeri mellékhatásokra, amelyek kiszáradáshoz és a vesefunkció romlásához vezethetnek. eGFR <15 ml/perc/1.73 m2/ESRD: alkalmazása nem ajánlott |
|
|
Amylin mimetikumok |
Pramlintid |
CrCl ≥15 ml/min: Nincs szükség az adagolás módosítására ESRD: Nincs információ |
|
Insulinok |
Rapid-ható analógok
Rövid hatású
Intermediate-hatású
Bázis inzulin analógok
|
Az inzulinszükséglet csökkenhet az inzulin clearance vagy az anyagcsere változásai miatt. Figyelmesen ellenőrizze a vércukorszintet. |
Vérnyomás. A vérnyomás kezelését 140/90 mmHg-nál kell kezdeni a cukorbetegségben és diabéteszes vesebetegségben szenvedő betegeknél.37 A United Kingdom Prospective Diabetes Study (UKPDS) 12%-os csökkenést talált a diabéteszes szövődmények kockázatában minden 10 mmHg szisztolés nyomáscsökkenéssel, amíg a nyomás 120 mmHg nem volt.38 A választandó gyógyszerek továbbra is az ACE-gátlók vagy ARB-k a magas vérnyomásban és cukorbetegségben, DKD-ben és CKD-ben szenvedő egyének számára. Az ACE-gátlásról kimutatták, hogy késlelteti a DKD kialakulását, ha enyhén emelkedett albuminuriával rendelkező betegeknél kezdik. A kreatinin akár 30%-kal is emelkedhet az ACE-gátló vagy ARB megkezdésekor.39 Ha a kreatinin ennél nagyobb mértékben emelkedik, fontolóra kell venni más vesebetegségek kivizsgálását.
A KDOQI nem ajánlja ACE/ARB adását normotenzív és normoalbuminuriás 2-es típusú diabeteses betegeknek.40,41,42 ACE-gátlók vagy ARB-k adása javasolt normotenzív, mikroalbuminuriás cukorbetegek számára.31,37 Nincs specifikus dózis vagy titrálás ezekre az egyénekre. A renin-angiotenzin rendszer kettős blokkolása ACE-vel és ARB-vel egyaránt nem ajánlott a hiperkalémia, a károsodott vesefunkció és a hipotenzió fokozott kockázata miatt.43
Sócsökkentés. A 2012-es Reduction of Endpoints in Non-insulin-dependent diabetes mellitus with the Angiotensin II Antagonist Losartan (RENAAL) Trial és az Irbesartan Diabetic Nephropathy Trial (IDNT) vizsgálat kimutatta, hogy az alacsony nátriumtartalmú diéta fokozta az ARB nefroprotektív és kardioprotektív hatását 2-es típusú cukorbetegségben és diabéteszes nefropátiában szenvedő betegeknél.44,45
Vese dialízis és veseátültetés. Az ESRD-ben szenvedő betegeket a nefrológiára kell utalni. A kezelés lehetőségei közé tartozik a peritoneális dialízis vagy hemodialízis, a vesetranszport, vagy a kezelés leállításának és a palliatív vagy hospice ellátás megkezdésének lehetősége. Egy megfigyeléses vizsgálat szerint azoknál a betegeknél, akik fiatalabb korban (< 60 éves korban) kezdték meg a dialízist, rosszabb volt a túlélés.46
Elirányítás. Az 1. ábra tartalmazza a GFR és az albuminuria osztályozásán alapuló beutalási indikációkat. Figyelembe kell venni a cukorbetegségtől független vesebetegség egyéb okait, különösen az 1-es típusú cukorbetegségben szenvedő betegeknél, ahol a retinopátia kialakulása nem előzi meg a nefropátia kialakulását.21 A nefrológusok segíthetnek a diagnózis tisztázásában, a rezisztens hipertónia és a hiperkalémia szabályozásában, valamint a betegek dialízisre való felkészítésében.8
Azt is figyelembe kell venni, hogy a nefropátia kialakulása nem feltétlenül magával a cukorbetegséggel áll összefüggésben. Az 1-es típusú cukorbetegségben szenvedő betegeknél a retinopátia kialakulása általában megelőzi a nefropátia kialakulását.47 A nefropátiával, de retinopátia nélkül jelentkező egyénnél ki kell vizsgálni az egyéb okokat. Nefrológushoz kell fordulni a nefropátia okának megállapítása érdekében, ha az bizonytalan, vagy ha nehezen kezelhető, DKD-vel kapcsolatos problémák merülnek fel, beleértve a vérszegénységet, a hyperparathyreoidizmust és az eGFR < 30 ml/min/1,73 m2 eGFR mellett előrehaladott vesebetegséget.8 A 4. stádiumú CKD kialakulásakor (eGFR < 30 ml/min/1,73 m2) a konzultáló nefrológus bevonása csökkent megbetegedéssel, csökkent egészségügyi költségekkel és késleltetett dialízissel jár.48 Fontolja meg a beutalást a 3B stádiumban, hogy a betegeket korábban felkészítsék, és a nefrológus maximálisan orvosilag kezelje.
Klinikai gyöngyszemek
- A DKD éves szűrése a DKD-re a vizelet albumin vizsgálatával és az eGFR mérésével történjen.
- A vérnyomás és a glükóz ellenőrzése a nefropátia progressziójának megelőzését biztosíthatja. A vérnyomást < 140/90 mmHg értéken kell tartani cukorbetegségben és CKD-ben szenvedő betegeknél. Az ACE-gátlók vagy ARB-k legyenek a választandó kezelés.
- Az ACE-gátlók és ARB-k nem alkalmazhatók a nefropátia megelőzésére, ha a vérnyomás és a fehérjekiválasztás normális. ACE-gátlók és ARB-k nem alkalmazhatók kombinációban.
- A CKD 3-5. stádiumában lévő betegeknél fokozott a hipoglikémia kockázata. Óvatosan kell eljárni az orális szerekkel, például a szulfonilureákkal.
- Némely CKD-s betegnél célszerű a HbA1c célértékét > 7%-ra beállítani, különösen, ha a hipoglikémia kockázata nagy.
Diabéteszes perifériás neuropátia
A diabéteszes perifériás neuropátia (DPN) széles körben elfogadott definíciója a klinikai gyakorlatban “a perifériás idegműködési zavar tüneteinek és/vagy jeleinek jelenléte cukorbetegeknél, miután más okokat kizártak.”49 A disztális szimmetrikus polineuropátia ADA-osztályozása a következő: 1) elsősorban kisrostos neuropátia, 2) elsősorban nagyrostos neuropátia és 3) vegyes kis- és nagyrostos neuropátia (leggyakoribb).
Patofiziológia és patogenezis. A DPN kialakulása és progressziója az idegek és a környező sejtek közötti összetett kapcsolatokból ered.50 Mind a vaszkuláris tényezők, mind a metabolikus kölcsönhatások hozzájárulnak a DPN minden szakaszához.51 A DPN kialakulásához vezető humán cukorbetegségben általánosan elfogadott felfogás szerint a hiperglikémia, a cukorbetegség időtartama, az életkorral összefüggő neuronális károsodások, a vérnyomás- és vérzsír-szabályozás mértéke és a testsúly közötti komplex kölcsönhatás.52,53,54,55 A hiperglikémia számos biokémiai útvonalat aktivál, amelyek meghatározzák az idegsejt metabolikus állapotát, és a károsodott idegi perfúzióval kombinálva hozzájárulnak a neuropathia progressziójához. Egy mérföldkőnek számító vizsgálat, a DCCT alátámasztja a hiperglikémia jelentőségét a neuropathia patogenezisében.10,56,57 Egy másik hiperglikémiával kapcsolatos, DPN-hez vezető mechanizmus a hiperglikémia által kiváltott oxidatív és nitrozatív stressz, a szabadgyök-termelés növekedésével.58,59
A hyperglykaemia mellett a közelmúltban felmerült, hogy az alacsony fokú gyulladás valószínűleg fontos szerepet játszik a diabéteszes neuropathiák patogenezisében, ami a perifériás és autonóm idegrostok hiányosságaihoz vezet.51,60 A metabolikus és vaszkuláris tényezők összetett sorozata váltja ki az idegrostok károsodása és javulása közötti egyensúlyhiányt, amely különösen a disztális szenzoros rostokat érinti, és hozzájárul az érzés fokozatos elvesztéséhez, amely a diabéteszes polineuropátia klinikai tüneteit manifesztálja.58,61
Közös tünetek. Amikor a DPN tapasztalt tüneteiről érdeklődik, jegyezze fel a lokalizációt (leginkább a kezekben és a lábakban érezhető), a kiváltó tényezőket, a kellemetlenségek jellemzőit, valamint az éjszakai súlyosbodás kezdetét és gyakoriságát, mivel a tünetek betegspecifikusak.4 A kis és nagy rostokat egyaránt érinti az emelkedett vércukorszint, és a tapasztalt tünetek az érintett érzékelőrostok osztályától függően változnak. Ha az érintett idegrostok túlnyomórészt kis idegrostok, a kiváltott tünetek általában fájdalom (szúró, lángoló, szúró, égő, fájó, unalmas és túlzottan érzékeny), diszesztézia (égő, bizsergő, szúró és szúró kellemetlen érzés) és zsibbadás4.
A kellemetlenségek intenzitása a kisebb rendellenes érzésektől a fájdalom által okozott fogyatékosságig terjedhet, amely éjszaka súlyosbodhat és megzavarhatja az alvást, ami a csökkent életminőség érzékelése miatt bizonyítottan összefügg a depresszióval.4
Másrészt, ha túlnyomórészt a nagy rostok érintettek, a betegek zsibbadást és bizsergést érezhetnek a végtagjaikban, bizonytalan járást tapasztalhatnak, és elveszíthetik egyensúlyukat (ami potenciális esésekhez vezethet).4 Egyes betegeknél a tünetek súlyosbodása a vércukorszint csökkenésével járhat a cukorbetegség intenzívebb terápiás kezelése miatt. A betegek lehetnek tünetmentesek, de különböző mértékű érzékszervi veszteséggel; a diabéteszes neuropátia okozta súlyos érzékszervi veszteség nemkívánatos következménye lehet a fájdalommentes sérülés, ami a lábfekély vagy súlyos esetben az amputáció fokozott kockázatához vezet.62
A diabéteszes perifériás neuropátia leggyakoribb formája a distalis szimmetrikus polineuropátia az érzékelő idegrostok progresszív elvesztésével.4 A kétoldali jellegzetes “harisnyás” mintázatot a leghosszabb (először érintett) idegek legdisztálisabb szakaszain kialakuló károsodások hozzák létre.63,64,65 Az idő előrehaladtával az ideghiányok proximális továbbhaladásából “harisnyás-kesztyűs” mintázat alakul ki, amely elősegíti az érzékszervi veszteséget és a DNP jellegzetes tüneteit.4
Klinikai diagnózis. A DPN klinikai diagnózisa a diabéteszes beteg neuropátiás jelei és tünetei alapján állítható fel, miután a neuropátia egyéb okait kizárták.66 A tünetmentes diabéteszes perifériás neuropátia a szövődményben szenvedők akár 50%-ánál is előfordulhat, ezért a megelőző lábápolás végrehajtása alapvető fontosságú, különösen azoknál, akiknél az érzéketlen láb miatt magas a sérülésveszély.4 A DPN éves szűrését minden cukorbetegnél el kell végezni tűszúrás, hőmérséklet, rezgésérzékelés (128 Hz-es hangvillával), 10 g monofilamentum nyomásérzékelés és boka mély ínreflexek alapján; a potenciális lábfekélyeket a 10 g monofilamentum érzékelés elvesztése (a védőérzés elvesztése) és a csökkent rezgésérzékelés előre jelzi.63 Az ADA 2017-es orvosi ellátási standardjai a diabéteszben továbbra is az éves 10-g monofilamentum vizsgálatot ajánlják a fekély és amputáció kockázatának kitett betegek azonosítása céljából.8 Emellett az ADA 2017-es irányelvei a DPN szűrését ajánlják a 2. típusú cukorbetegség diagnózisakor és öt évvel az 1. típusú cukorbetegség diagnózisát követően.8
2009-ben a diabéteszes neuropátiákkal foglalkozó torontói konszenzusos testület frissítette a diagnosztikus kritériumokat, hogy diagnosztikus kategóriákat adjon meg. Ezenkívül az egészségügyi szolgáltatók számos jól validált szűrőeszközt vonhatnak be a diagnózis felállításába, köztük a Michigan Neuropathy Screening Instrument (MNSI), a Toronto Clinical Neuropathy Score és a Utah Neuropathy Scale. A 7. táblázat ismerteti a neuropátia egyéb okait, amelyeket ki kell zárni.
7. táblázat. A neuropátia egyéb okai67
- Alkohol vagy más toxinok
- Neurotoxikus gyógyszerek, különösen kemoterápia
- B12-vitamin hiánya
- Pajzsmirigy alulműködés
- Veseelégtelenség
- Malignus betegségek (myeloma multiplex, bronchogén karcinóma)
- Humán immunhiányos vírus (HIV)
- Krónikus gyulladásos demyelinizáló neuropathia, öröklött neuropathiák és vasculitis
Diagnosztikai vizsgálatok. Számos diagnosztikai vizsgálat létezik a DPN jelenlétének megerősítésére. Az idegvezetési vizsgálatokat évek óta a DPN arany standard diagnosztikai vizsgálatának tekintik, mivel objektív, a betegek válaszai nélküli mérésük nagy megbízhatóságot eredményez.4 A kvantitatív szenzoros vizsgálat a betegek könnyű érintés, rezgés és hőmérséklet megkülönböztetésének képességét értékeli, ami bizonyos fokú szubjektivitással jár.4 Más módszerek, beleértve a bőrbiopsziát és az intraepidermális idegrost-sűrűséget és a cornealis konfokális mikroszkópiát, a klinikai gyakorlatban rutinszerűen nem használatosak, de klinikai vizsgálatokban alkalmazhatók.4
Kezelési lehetőségek: Gyógyszeres kezelés. A DPN farmakológiai kezelése a tünetek javítására szolgál, így az alkalmazott gyógyszerek nem a progresszió megelőzésére szolgálnak. A 8. táblázat összefoglalja a neuropátiás tünetek kezelésére szolgáló gyógyszereket a három leggyakrabban használt osztályból (antikonvulzánsok, antidepresszánsok és opioidok). Bár a DPN kezelésében gyakran több hatóanyagot is alkalmaznak kezdeti megközelítésként, csak a pregabalint és a duloxetint engedélyezte az FDA ennek az állapotnak a kezelésére; így e szerek bármelyike ajánlott kezdeti választásként a tüneti neuropátiás fájdalom kezelésére.4 A gabapentint, bár az FDA nem engedélyezte a DPN kezelésében való alkalmazását, gyakran alkalmazzák kezdeti megközelítésként, amelynek hatékonysága összehasonlítható az FDA által engedélyezett szerekkel. A triciklikus antidepresszánsok (pl. amitriptilin) – az FDA által nem engedélyezett DPN-gyógyszerek – hatékonyak a DPN kezelésében, de a mellékhatások nagyobb kockázata miatt óvatosan kell alkalmazni őket.
8. táblázat. Gyakran alkalmazott farmakológiai szerek a DPN kezelésére4,69 |
|||||
|
Gyógyszeres szer (NNT-tartomány 30…50%-os javulás*) |
Napi maximális DNP adag (mg/nap) |
Szokásos mellékhatások |
Dózis módosítás szükséges? |
Ellenejavallatok |
Receptköteles szempontok |
|
Antikonvulzívumok
|
|||||
|
Pregabalin (3.3-8.3) |
Szédülés Szomnolencia Fogyás Perifériás ödéma Homályos látás Székrekedés |
Renális: Igen Hepatikus: Nem |
Pregabalinnal szembeni túlérzékenység |
Súlyos bizonyíték; FDA által jóváhagyott; ellenőrzött anyag |
|
|
Gabapentin (3.3-7.2) |
3,600 |
Szédülés Ataxia Somnolencia Főfájás Nausea Hasmenés Súlygyarapodás |
Renális: Hepatikus: Igen Hepatikus: Igen Hepatikus: Nem |
Gabapentinnel szembeni túlérzékenység |
Mérsékelt bizonyíték; nem FDA által jóváhagyott |
|
Antidepresszánsok
|
|||||
|
Amitriptilin (2.1-4.2) |
Súlyos szedáció; zavarodottság; antikolinerg hatások (székrekedés, homályos látás) |
Renális: Nem Hepatikus: Nem Időskorú betegeknél alacsonyabb adagok javasoltak |
Amitriptilinre való túlérzékenység; MAO-val való együttes alkalmazás vagy 14 napon belül; ciszapriddel való együttes alkalmazás; Myocardialis infarktust követő akut felépülési fázis |
Mérsékelt bizonyítékok; az FDA nem engedélyezte; kardiovaszkuláris betegségben szenvedőknél óvatosan alkalmazható |
|
|
Duloxetin (3.8-11) |
(USA) |
Nausea; szédülés; általános álmosság |
Renális: Igen Hepatikus: Kerülni kell az alkalmazást májkárosodás esetén |
Túlérzékenység; MAO-val való együttes vagy 14 napon belüli alkalmazás; linezolidot vagy intravénás metilénkéket kapóknál a kezelés megkezdése |
Mérsékelt bizonyíték; FDA által jóváhagyott; adható pregabalinhoz vagy gabapentinhez |
|
Venlafaxin (5.2-8.4) |
Nausea; szedáció; általános álmosság |
Renális: Igen Hepatikus: Igen |
gyenge bizonyíték; nem FDA által jóváhagyott; Gabapentinhez adható |
||
|
Opioidok
|
|||||
|
Tramadol (2.1-6.4) |
Somnolencia Émelygés Hányás Székrekedés Szédülés Szédülés Kopffájás |
Renal: Hepatikus: Igen Hepatikus: Igen Hepatikus: Nem |
Tramadollal, opioidokkal vagy a készítmény bármely összetevőjével szembeni túlérzékenység; ER készítmény: jelentős légzésdepresszió és akut vagy súlyos asztma; IR készítmény: Akut mérgezés alkohollal, hipnotikumokkal, narkotikumokkal, centrális hatású analgetikumokkal, opioidokkal vagy pszichotróp gyógyszerekkel |
Kisebb visszaélési potenciál (IV. jegyzékben szereplő ellenőrzött anyag); nem ajánlott első- vagy másodvonalbeli szerként |
|
|
Tapentadol (N/A) |
Imediate-release: Extended release: |
Somnolence Nausea Hányás Székrekedés Szédülés |
Ren: Nem ajánlott az alkalmazása, ha Hepatikus: Hepatikus: Nem |
Tapentadollal szembeni túlérzékenység; jelentős légzésdepresszió; akut vagy súlyos asztma; paralítikus ileusz; MAO-gátlók alkalmazását követő 14 napon belül |
FDA által jóváhagyott; II. jegyzékben szereplő ellenőrzött anyag; nem ajánlott első- vagy másodvonalbeli szerként |
|
Az információk a gyógyszerekre vonatkoznak, amelyeket a vonatkozó betegtájékoztatókból (a kereskedelmi nevekkel hivatkozva) |
|||||
Az American Academy of Neurology (AAN) irányelve a következő helyi szereket ajánlja: Kapszaicin és izoszorbiddinitrát spray (mérsékelt evidencia) és Lidoderm tapasz (gyenge evidencia).69 Az oxkarbazepint, a lamotrigint, a lacosamidot, a klonidint, a pentoxifyllint és a mexiletint az AAN-irányelv nem ajánlja a DPN kezelésében.69
Az opioidok alkalmazását refrakter DPN-ben egyesek ajánlják. Az AAN-irányelv által ajánlott opioidok közé tartozik a dextrometorfán (400 mg/nap), a morfin-szulfát (120 mg/napra titrálva) és az oxikodon (átlag 37 mg/nap, max. 120 mg/nap); azonban nincs elegendő adat arra, hogy az egyik szer alkalmazását javasoljuk a másik helyett.69 A tanulmány szerzői csak súlyos, refrakter esetekben javasolják az opioidok alkalmazását, szoros megfigyelés mellett azon betegek esetében, akik az opioidok hatására valódi funkcionális javulást érnek el. A szerzők követik a Centers for Disease Control and Prevention 2016-os állásfoglalását, amely szerint az opioidok hosszú távú alkalmazása korlátozott a nem daganatos típusú fájdalomban.70
A DPN farmakológiai kezelésének egyik kihívása az életminőségi eredményeket is magában foglaló head-to-head vizsgálatok elégtelensége4 . Egy nemrégiben végzett vizsgálat, amely a nagy dózisú pregabalin, nagy dózisú duloxetin vagy kombinációban alkalmazott nyolchetes terápiát hasonlította össze, nem talált jelentős különbséget az átlagos fájdalomváltozásban a monoterápia és a kombinált terápia között.71 Több, két hatóanyagot összehasonlító vizsgálatra van szükség ahhoz, hogy betekintést nyerjünk a diabéteszes perifériás neuropátiában szenvedők ellátásának javításába.
Nem farmakológiai kezelés. Eljárások. Az ANN-irányelv javasolja a perkután elektromos idegstimuláció megfontolását három-négy héten keresztül a DPN kezelésére.69 Egy kísérleti, kétféle akupunktúrás, randomizált, kontrollált vizsgálat72 és egy egy-vak, placebokontrollos, randomizált vizsgálat73 , amely az akupunktúra hatékonyságát értékelte a DPN-ben, egyaránt javulást mutatott a fájdalommal kapcsolatos kimeneti mérésekben. További vizsgálatokra van azonban szükség az akupunktúra szerepének megerősítéséhez a DPN kezelésében.
Alfa-liponsav. Bizonyos bizonyítékok arra utalnak, hogy az antioxidáns alfa-liponsav alkalmazása segíthet a szabad gyökök által közvetített oxidatív stressz csökkentésében, és a következő előnyökkel járhat: a DPN patogenezisének célzott kezelése, kialakulásának lassítása és tüneteinek javítása.74,75
Prevenció. Az egészséges táplálkozásra és a fizikai aktivitásra összpontosító életmódbeli módosítások folyamatosan csökkentik a cukorbetegség és szövődményei, köztük a diabéteszes perifériás neuropátia előfordulását.68 Az intenzív glikémiás kontroll bizonyítottan segít csökkenteni a diabéteszes neuropátia kockázatát a cukorbetegeknél az idegfunkciók javításán keresztül.61,76,77 A DCCT megállapította a glikémiás kontroll szerepét a diabéteszes neuropátia progressziójának megelőzésében és megállításában az 1-es típusú cukorbetegségben.10,56
Klinikai gyöngyszemek
- A betegek akár 50%-ának is lehet fájdalommentes vagy tünetmentes perifériás neuropathiája.
- A neuropathiás betegeknek lábápolási oktatás (a lábak napi önellenőrzése) és a kiválasztott betegek rendszeres podológiai ellátása ajánlott.
- A DPN-ben szenvedő betegeknek, akik a védőérzés elvesztésének jeleit mutatják deformitással vagy anélkül, azt kell tanácsolni, hogy három-hat havonta járjanak orvoshoz megelőző intézkedések céljából.64
- A DPN tüneteinek hatékony kezeléséhez elengedhetetlen a multidiszciplináris megközelítés; ez az átfogó megközelítés magában foglalhat farmakológiai, pszichológiai és/vagy fizikoterápiát.
- Az ADA által a diabéteszes neuropátiáról közzétett új állásfoglalás a DPN szűrését javasolja a perifériás neuropátia tüneteit mutató prediabéteszes betegeknél.4
- Speciális ellátásra van szükség a perifériás betegségben, nem szenzoros neuropátiában vagy Charcot-lábban szenvedők esetében.
Gasztroparézis
A diabéteszes neuropátia másik formája a gasztroparézis. Ez az állapot felső gasztrointesztinális tünetekkel jár, beleértve a hányingert, hányást, korai jóllakottságot vagy posztprandiális teltségérzetet, hasi fájdalmat és puffadást, de kivezető út elzáródás hiányában. Bár a gasztroparézisnek számos oka van, becslések szerint az esetek körülbelül egyharmadáért a cukorbetegség felelős.78
Patofiziológia. A diabéteszes gastroparesis javasolt patofiziológiai mechanizmusai közé tartozik a károsodott glikémiás kontroll, a vagus vagy a prevertebralis szimpatikus ganglionok neuropátiája, a Cajal interstitialis sejtek rendellenességei, a nitrogén-oxid-szintáz elvesztése és esetleg myopathia.79,80
Klinikai megjelenés. Az állapot korai szakaszában a betegek általában tünetmentesek. A tünetek és a neuropátia súlyossága között nincs lineáris kapcsolat. A tünetek széles skálája megnehezíti az állapot diagnosztizálását. Egyéb klinikai megjelenési formák közé tartozik az étvágytalanság, alultápláltság, fogyás és a táplálék és az inzulin felszívódásának eltéréséből eredő hipoglikémia. A fájdalom valójában aluljelentett, de sok ember számára jelentős lehet. Egy NIH által finanszírozott konzorciumban a gasztroparézisben szenvedő betegek 72%-ának volt hasi fájdalma.81 E betegek 18%-ánál ez volt a domináns tünet. A fájdalmat evés váltotta ki (72%), éjszakai volt (74%) és zavarta az alvást (66%) ezeknél a betegeknél.81
Hogyan gyakori a diabéteszes gasztroparézis? A gasztroparézis 10 éves kumulatív előfordulási gyakoriságát az 1. típusú cukorbetegségben 5,2%-ra, a 2. típusú cukorbetegségben 1%-ra becsülték a közösségi cukorbetegek körében.82 Más tanulmányok 5-12% közötti arányt találtak.83,84 Az arányok azonban sokkal magasabbak, ha a diagnózis a tüneteken és nem a gyomorürítési vizsgálaton alapul.
A gasztroparézis gyakoribb az 1-es típusú cukorbetegségben, mint a 2-es típusú cukorbetegségben, és leggyakrabban akkor jelentkezik, ha az illetőnek már több mint 10 éve cukorbetegsége van, és kialakult a többi mikrovaszkuláris szövődmény, a retinopátia, a nefropátia és a perifériás neuropátia. Ha egy betegnél a vártnál korábban jelentkezik a gasztroparézis, más etiológiát kell felderíteni, leggyakrabban a perioperatív vagusideg-sérülést vagy az inkretin alapú szerek – glükagonszerű peptid-1 receptor agonisták (GLP-1RA) és dipeptidil-peptidáz 4 gátlók (DPP-4 gátlók) – farmakológiai hatásait.
Amikor a betegnél a gasztroparézis tünetei jelentkeznek, a tünetek általában 12-25 éven keresztül fennállnak és stabilak. Ez még akkor is igaz, ha javul a glükózszabályozás,85 kivéve hasnyálmirigy- és veseátültetés esetén.86 Bár nincs egyértelmű bizonyíték arra, hogy a gasztroparézis önmagában növeli a mortalitást, jelentősen csökkenti az életminőség minden aspektusát.87
Diagnosztika. Számos vizsgálat segíthet a diagnózis felállításában. A diagnózis arany standardja a gastrooesophagealis szcintigráfia. Ez noninvazív, fiziológiai vizsgálatot végez, és kvantitatív eredményt ad. A gasztroparézist akkor lehet diagnosztizálni, ha négy órával az étkezés után egy standard, alacsony zsírtartalmú étel legalább 35%-át visszatartják.80
A legpontosabb vizsgálati eredmények érdekében a vizsgálat előtti protokollnak tartalmaznia kell, hogy a vizsgálat előtt legalább két-három napig abba kell hagyni minden motilitást befolyásoló gyógyszert, beleértve a prokinetikumokat, opiátokat és antikolinergikumokat. Az inkretin szereket, például a GLP-1 agonistákat és a DPP-4 gátlókat is abba kell hagyni, mivel ezekről ismert, hogy késleltetik a gyomorürülést. A hiperglikémia szintén késlelteti a gyomorürülést, és a glükózszintnek a vizsgálat megkezdése előtt 275 mg/dl alatt kell lennie.79,88
A betegeknek tartózkodniuk kell a dohányzástól és az alkoholfogyasztástól a vizsgálat napján, mivel mindkettő lassíthatja a gyomornyelőcső ürülését.89 Ezenkívül a GLP-1RA-k súlyosbíthatják a gasztroparézist, mivel lassítják a gyomorürülést. Továbbá egyeseknél előfordulhat szubklinikai gasztroparézis, amely a GLP-1RA elkezdésekor lepleződik le.
Kezelés. A gasztroparézis kezelése nagyban függ a tünetek súlyosságától. A kezelés általános elvei közé tartoznak a szupportív kezelések (folyadék-, elektrolit-, glükózszabályozás és táplálkozás), a gyógyszeres kezelések (prokinetikumok, antiemetikumok és fájdalomcsillapítás), valamint az invazív kezelések (műtét, Botox-injekciók, gyomor pacing vagy elektromos stimuláció).79
A szupportív kezelés általában a kórházban kezdődik, és a folyadék-, elektrolit- és táplálkozási zavarok normalizálására összpontosít. A táplálkozási támogatás biztosítása során az enterális táplálást előnyben részesítik a parenterális táplálással szemben, mivel ez fiziológiásabb és segíthet a bélflóra fenntartásában. Továbbá a diétás változtatások nagyon hasznosak lehetnek gasztroparézis esetén. A gasztroparézisben szenvedő betegek számára ajánlott az alacsony rost-, zsír- és maradéktartalmú étrend.85 A magas rosttartalmú étrend fokozhatja a tüneteket, mivel több emésztést igényel.
Medicinák. Prokinetikumok: Az Egyesült Államokban a metoklopramid és az eritromicin a leggyakrabban alkalmazott gyógyszerek a gasztroparézis kezelésére. A metoklopramidra azonban fekete dobozos figyelmeztetés van a tardív diszkinézia kockázata miatt. Ennek az állapotnak a kialakulása közvetlenül összefügg a metoklopramid alkalmazásának időtartamával és a bevett adagok számával. Ha ezt a gyógyszert használja, a legjobb, ha csak tüneteket mutató betegeknél alkalmazza, és a legalacsonyabb hatásos adaggal kezdi 15 perccel étkezés előtt. A gyógyszerszünet néha segíthet a hatás időtartamának meghosszabbításában.90
A domperidon egy szelektívebb dopamin agonista, amely ugyanolyan hatékony, mint a metoklopramid, de kevesebb központi idegrendszeri mellékhatása van.91
Antiemetikum: A tünetek enyhítésére antiemetikumokat lehet alkalmazni. A gyógyszerkölcsönhatások kockázata azonban jelentős, ezért gondosan figyelemmel kell kísérni.
A fájdalom kezelése kihívást jelenthet a gasztroparézises betegeknél. A triciklikus antidepresszánsokat gyakran alkalmazzák első vonalbeli terápiaként a fájdalom kezelésére gasztroparézisben. A másodvonalbeli megközelítés a gyenge mu-opioid receptor agonista, a tramadol, amely szerotonint is felszabadít és gátolja a noradrenalin visszavételét, valamint a gamma-aminovajsav analóg, a gabapentin. Narkotikumok alkalmazása gasztroparézisben azonban nem ajánlott, mivel hozzájárulhat a székrekedéshez és a tünetek súlyosbodásához.
Invazív kezelések: A botoxinjekciókat gyakran alkalmazzák a gasztroparézis kezelésében, de alkalmazásukat klinikai vizsgálatok nem támasztják alá.92,93
A gyomor elektromos stimulációs készüléket 2000-ben az FDA humanitárius eszközmentesség alapján engedélyezte.94 A gyomor elektromos stimulációs készülék nagyfrekvenciás, alacsony energiájú elektromos stimulációt juttat a gyomorba. A diabéteszes gasztroparézisben hasznosabb, mint az idiopátiás gasztroparézisben. Egy metaanalízis jelentős előnyöket mutatott ki a betegek tüneteiben. Az előnyök pontos mechanizmusa még mindig nem ismert.95 Azt javasolták, hogy a gyomor elektromos stimulációja változásokat eredményez a hányingert és hányást szabályozó központi mechanizmusokban, növeli a vagális funkciót, és a puffadásra való érzékenység csökkenését eredményezi.97 A jól reagáló betegek jellemzően gyorsan reagálnak. Ez arra késztetett egyeseket, hogy a hosszú távú alkalmazás előtt először ideiglenes elektródák elhelyezésével végzett kísérletet javasoljanak.
Klinikai gyöngyszemek
- A diabéteszes gasztroparézis gyakoribb a régóta fennálló cukorbetegeknél és az egyéb mikrovaszkuláris szövődményekkel küzdőknél.
- A gasztroparézis arany standard diagnózisa a gastrooesophagealis szcintigráfia.
- Diabéteszes gastroparesisben alacsony rost-, zsír- és maradékszegény diéta ajánlott.
- A farmakológiai és intervenciós kezeléseknek korlátozott előnyei és jelentős hosszú távú kockázata van.
Diabéteszes cheiroarthropathia
A cukorbetegség egyik kevésbé ismert szövődménye a cheiroarthropathia. Ezt az állapotot a régóta fennálló cukorbetegségben szenvedőknél a bőr megvastagodása miatt korlátozott ízületi mozgékonyság jellemzi. Valószínűleg ez volt az 1-es típusú cukorbetegségből azonosított első szövődmény. A gyakorisági arányok széles skálán mozognak, 8-50% között.98
A cheiroarthropathiát feltehetően a kollagén glikozilációja és keresztkötése okozza. A bőrt és az inakat is érintheti, és korlátozott ízületi mozgékonyságot, leggyakrabban az ujjak kinyúlását, merevséget és fájdalmat eredményezhet. A diabéteszes cheiropátia klasszikus fizikális vizsgálati jele az “ima jel”. Ebben az állapotban a személy képtelen a kezét teljesen szétterpeszteni, hogy “imádkozzon”, így a bal és a jobb kéz ujjai között rés marad. Bizonyított, hogy azoknál, akiknél cheiropátia alakul ki, háromszor nagyobb a mikrovaszkuláris szövődmények kockázata.99
A diabéteszes cheiropátia jellemzően a régóta fennálló vagy rosszul szabályozott glikémiában szenvedőknél rosszabb. Szerencsére sokan tapasztalják a tünetek enyhülését és a mozgásképesség javulását, amikor a glükózszabályozás javul.100
Következtetés
A cukorbetegség szövődményeinek kezelése multidiszciplináris csapatot igényel. A retinopátia, a nefropátia és a neuropátia korai szűrése alapvető fontosságú, tekintettel a betegség tünetmentes jellegére. A diabétesz kezelésének jellemzője minden szövődmény esetében továbbra is a glikémiás és vérnyomás-szabályozás.
- American Diabetes Association. A cukorbetegség költségei. Elérhető a következő címen: http://www.diabetes.org/advocacy/news-events/cost-of-diabetes.html?referrer=https://www.google.com/. Frissítve 2015. június 22-én. Hozzáférés: 2017. február 8.
- UK Prospective Diabetes Study Group. Intenzív vércukorszint-szabályozás szulfonilureákkal vagy inzulinnal a hagyományos kezeléssel összehasonlítva és a szövődmények kockázata 2-es típusú cukorbetegségben szenvedő betegeknél. Lancet 1998;352:837-853.
- Gregg EW, Yanfed L, Wang J. Changes in diabetes-related complications in the United States, 1990-2010. N Engl J Med 2014;370:1514-1523.
- Pop-Busui R, Boulton A, Feldman E, et al. Diabetes neuropathy: A position statement by the American Diabetes Association. Diabetes Care 2017;40:136-154.
- Leasher JL, Bourne RR, Flaxman SR, et al. Global estimates on the number of people blind or visually impaired by diabetic retinopathy: Egy metaanalízis 1990 és 2010 között. Diabetes Care 2016;39:1643-1649.
- National Eye Institute. Tények a diabéteszes szembetegségről. Elérhető a következő címen: https://nei.nih.gov/health/diabetic/retinopathy. Frissítve 2015. szeptember. Hozzáférés 2017. febr. 8.
- Fong, DS, Aiello L, Gardner TW, et al. Retinopathy in diabetes. Diabetes Care 2004;27(Suppl 1):S84-S87.
- American Diabetes Association. Az orvosi ellátás standardjai a cukorbetegségben-2017. Diabetes Care 2017;40:(Suppl 1):S4-S5.
- Doggen K, Nobels F, Scheen AJ, et al. Cardiovascular risk factors and complications associated with albuminuria and impaired renal function in insulin-treated diabetes. J Diabetes Complications 2013;27:370-375.
- The Diabetes Control and Complications Trial Research Group. A cukorbetegség intenzív kezelésének hatása a hosszú távú szövődmények kialakulására és progressziójára inzulinfüggő diabetes mellitusban. N Engl J Med 1993;329:977-986.
- Action to Control Cardiovascular Risk in Diabetes Follow-On (ACCORDION) Eye Study Group és az Action to Control Cardiovascular Risk in Diabetes Follow-On (ACCORDION) Study Group. Az intenzív glikémiás kontroll tartós hatása a retinopátiára 2-es típusú cukorbetegségben az Action to Control Cardiovascular Risk in Diabetes (ACCORDORD) follow-on tanulmányban. Diabetes Care 2016;39:1089-1100.
- ACCORD Study Group, ACCORD Eye Study Group, Chew EY, et al. Effects of medical therapies on retinopathy progression in type 2 diabetes. N Engl J Med 2010;363:233-244.
- Chew EY, Davis MD, Danis RP, et al. The effects of medical management on the progression of diabetic retinopathy in persons with type 2 diabetes: The Action to Control Cardiovascular Risk in Diabetes (ACCORD) Eye Study. Ophthalmology 2014;121:2443-2451.
- Diabetes Control and Complications Trial Research Group. A terhesség hatása a mikrovaszkuláris szövődményekre a Diabetes Control and Complications Trial-ban. Diabetes Care 2000;23:1084-1091.
- Colberg SR, Sigal RJ, Yardley JE, et al. Physical activity/exercise and diabetes: A position statement of the American Diabetes Association. Diabetes Care 2016;39:2065-2079.
- The Diabetic Retinopathy Study Research Group. Előzetes jelentés a fotokoagulációs terápia hatásairól. Am J Ophthalmol 1976;81:383-396.
- Early Treatment Diabetic Retinopathy Study Research Group. Fotokoaguláció diabéteszes makulaödéma esetén: Early Treatment Diabetic Retinopathy Study 1. számú jelentés. Arch Ophthalmol 1985;103:1796-1806.
- Nguyen QD, Brown DM, Marcus DM, et al. Ranibizumab for diabetic macular edema: Eredmények 2 fázis III randomizált vizsgálatból: RISE és RIDE. Ophthalmology 2012;119:789-801.
- Wong TY, Cheung CMG, Larsen M, et al. Diabetic retinopathy. Nat Rev Disease Prim doi:10.1038/nrdp.2016.12; published online March 17, 2016.
- Batuman V, Soman AS, Schmidt RJ, Soman SS. Diabetes nephropathia. Medscape Elérhető: Medscape: http://emedicine.medscape.com/article/238946-overview. Frissítve: 2016. szeptember 30. Hozzáférés: 2017. febr. 12.
- Tuttle KR, Bakris GL, Bilous RW, et al. Diabetic kidney disease: Egy ADA konszenzuskonferencia jelentése. Diabetes Care 2014;37:2864-2883. https://doi.org/10.2337/dc14-1296
- Patel A, MacMahon S, Chalmers J, et al. Intensive blood glucose control and vascular outcomes in patients with type 2 diabetes. N Engl J Med 2008;358:2560-2572.
- Duckworth W, Abraira C, Moritz T, et al. Glükózkontroll és érrendszeri szövődmények 2-es típusú cukorbeteg veteránoknál. N Engl J Med 2009;360:129-139.
- Ismail-Beigi F, Craven T, Banerji MA, et al. Effect of intensive treatment of hyperglycaemia on microvascular outcomes in type 2 diabetes: Az ACCORD randomizált vizsgálat elemzése. Lancet 2010;376:419-430.
- National Kidney Foundation. KDOQI klinikai gyakorlati útmutató a cukorbetegségről és a CKD-ről: 2012-es frissítés. Am J Kidney Dis 2012;60:850-886.
- Fox CS, Matsushita K, Woodward M, et al. Chronic Kidney Disease Prognosis Consortium. A vesebetegség mérőszámainak összefüggései a halálozással és a végstádiumú vesebetegséggel cukorbeteg és nem cukorbeteg egyéneknél: A meta-analysis. Lancet 2012;380:1662-1673.
- Hahr AJ, Molitch ME. A diabetes mellitus kezelése krónikus vesebetegségben szenvedő betegeknél. Clin Diabetes Endocrinol 2015. doi: 10.1186/s40842-015-0001-9.
- Alsaad KO, Herzenberg AM. A diabéteszes nefropátia megkülönböztetése a glomeruloszklerózis egyéb eseteitől: An update. J Clin Pathol 2007;60:18-26.
- Narva AS, Bilous RW. A diabéteszes vesebetegség laboratóriumi értékelése. Diabetes Spectr 2015;28:162-166.
- Levey AS, Stevens LA, Schmid CH, et al. A new equation to estimate glomerular filtration rate. Ann Intern Med 2009;150:604-612.
- National Kidney Foundation. KDOQI klinikai gyakorlati útmutató a krónikus vesebetegséghez: Evaluation, classification, and stratification. Am J Kidney Dis 2002;39(2 Suppl 1):S1-S266.
- de Boer IH, Rue TC, Cleary PA, et al. Long-term renal outcomes of patients with type 1 diabetes mellitus and microalbuminuria: An analysis of the Diabetes Control and Complications Trial/Epidemiology of Diabetes Interventions and Complications cohort. Arch Intern Med 2011;171:412-420.
- Wanner C, Inzucchi SE, Lachin JM, et al. Empagliflozin and progression of kidney disease in type 2 diabetes. N Engl J Med 2016;375:323-334.
- Heerspink HJL, Desai M, Jardine M, et al. Canagliflozin slows progression of renal function decline independently of glycemic effects. J Am Soc Nephrol 2016;28:1-8.
- Lexi-Drugs. Lexicomp. Wolters Kluwer Health, Inc. Riverwoods, IL. Elérhető a következő címen: http://online.lexi.com. Hozzáférés 2016. október 31.
- Micromedex Solutions. Truven Health Analytics, Inc. Ann Arbor, MI. Elérhető a következő címen: http://www.micromedexsolutions.com. Hozzáférés: 2016. okt. 31.
- James PA, Oparil S, Carter BL, et al. 2014 evidence-based guideline for the management of high blood pressure in adults. JAMA 2014;311:507-520.
- King P, Peacock I, Donnelly R. The United Kingdom Prospective Diabetes Study (UKPDS): Klinikai és terápiás vonatkozások a 2-es típusú cukorbetegségre. Br J Clin Pharmacol 1999;48:643-648.
- Jackevicius CA, Wong J, Aroustamian I, et al. Rates and predictors of ACE inhibitor discontinuation subsequent to elevated serum creatinine: A retrospective cohort study. BMJ Open 2014;4:e005181.
- Mauer M, Zinman B, Gardiner R, et al. Renal and retinal effects of enalapril and losartan in type 1 diabetes. N Engl J Med 2009;361:40-51.
- Bilous R, Chaturvedi N, Sjølie AK, et al. A kandezartán hatása a mikroalbuminuriára és az albumin kiválasztási sebességre cukorbetegségben: Három randomizált vizsgálat. Ann Intern Med 2009;151:11-20.
- Haller H, Ito S, Izzo JL Jr, et al. Olmesartan for the delay or prevention of microalbuminuria in type 2 diabetes. N Engl J Med 2011;364:907-917.
- Makani H, Bangalore S, Desouza KA, et al. A renin-angiotenzin rendszer kettős blokkolásának hatékonysága és biztonságossága: Randomizált vizsgálatok metaanalízise. BMJ 2013;346:f360.
- Miao Y, Ottenbros SA, Laverman GD, et al. A húgysavcsökkentés hatása a vese kimenetelére a lozartánkezelés során: A post-hoc elemzés a végpontok csökkentéséről nem inzulinfüggő diabetes mellitusban az Angiotensin II Antagonist Losartan Trial segítségével. Hypertension 2011;58:2-7.
- Lewis EJ, Hunsicker LG, Clarke WR, et al. Renoprotektív hatása az angiotenzin-receptor antagonistának, az irbesartánnak 2-es típusú cukorbetegség okozta nefropátiában szenvedő betegeknél. N Eng J Med 2001;354:851-860.
- Adler A, Casula A, Steenkamp R, et al. Association between glycemia and mortality in diabetes individuals on renal replacement therapy in the U.K. Diabetes Care 2014;37:1304-1311.
- Sharma SG, Bomback AS, Radhakrishnan J, et al. The modern spectrum of renal biopsy findings in patients with diabetes. Clin J Am Soc Nephrol 2013;8:1718-1724.
- Smart NA, Dieberg G, Ladhani M, Titus T. Early referral to specialist nephrology services for preventing the progression to end-stage kidney disease. Cochrane Database Syst Rev 2014;6:CD007333.
- Boulton AJM, Gries FA, Jervell JA. Irányelvek a diabéteszes perifériás neuropátia diagnózisához és ambuláns kezeléséhez. Diabet Med 1998;15:508-514.
- O’Brien PD, Hinder LM, Sakowski SA, Feldman EL. ER stressz a diabéteszes perifériás neuropátiában: Egy új terápiás célpont. Antioxid Redox Signal 2014;21:621-633.
- Cameron NE, Cotter MA. Pro-gyulladásos mechanizmusok a diabéteszes neuropátiában: Fókuszban a nukleáris faktor kappa B útvonal. Curr Drug Targets 2008;9:60-67.
- Tesfaye S, Chaturvedi N, Eaton SE, et al. Vascular risk factors and diabetic neuropathy. N Engl J Med 2005;352:341-350.
- Wiggin TD, Sullivan KA, Pop-Busui R, et al. Elevated triglycerides correlated with progression of diabetic neuropathy. Diabetes 2009;58:1634-1640.
- Stella P, Ellis D, Maser RE, Orchard TJ. Kardiovaszkuláris autonóm neuropátia (kilégzés és belégzés aránya) 1-es típusú cukorbetegségben. Előfordulás és prediktorok. J Diabetes Complications 2000;14:1-6.
- Witten DR, Tesfaye S, Chaturvedi N, et al. Risk factors for cardiac autonomic neuropathy in type 1 diabetes mellitus. Diabetologia 2005;48:164-171.
- Diabetes Control and Complication Trial (DCCT) Research Group. Az intenzív diabéteszkezelés hatása az idegvezetésre a Diabetes Control and Complications Trial-ban. Ann Neurol 1995;38:869-880.
- Diabetes Control and Complication Trial (DCCT) Research Group. Az intenzív diabéteszterápia hatása a vegetatív idegrendszeri funkciók mérésére a Diabetes Control and Complications Trial (DCCT) vizsgálatban. Diabetologia 1998;41:416-423.
- Edwards JL, Vincent AM, Cheng HT, Feldman EL. Diabéteszes neuropátia: Mechanizmusok a kezelésig. Pharmacol Ther 2008;120:1-34.
- Vincent AM, Callaghan BC, Smith AL, Feldman EL. Diabéteszes neuropátia: Sejtmechanizmusok egy terápiás célpont. Nat Rev Neurol 2011;7:573-583.
- Kellogg AP, Wiggin T, Larkin D, et al. Protective effects of cyclooxygenase-2 gene inactivation against peripheral nerve dysfunction and intraepidermal nerve fibers loss in experimental diabetes. Diabetes 2007;56:2997-3005.
- Callaghan BC, Cheng HT, Stables CL, et al. Diabetic neuropathy: Klinikai manifesztációk és jelenlegi kezelések. Lancet Neurol 2012;11:521-534.
- Boulton AJM, Kirsner RS, Vileikyte L. Klinikai gyakorlat: Neuropátiás diabéteszes lábfekélyek. N Eng J Med 2004;351:48-55.
- Boulton AJM, Vinik AI, Arezzo JC, et al. Diabetic neuropathies: A statement by the American Diabetes Association. Diabetes Care 2005;28:956-962.
- Boulton AJM, Armstrong DG, Albert SF, et al. Comprehensive foot examination and risk assessment: A report of the task force of the foot care interest group of the American Diabetes Association, with endorsement by the American Association of Clinical Endocrinologists. Diabetes Care 2008;31:1679-1685.
- Tesfaye S, Boulton AJ, Dyck PJ, et al. Diabetic neuropathies: Update on definitions, diagnostic criteria, estimation of severity, and treatments. Diabetes Care 2010;33:2285-2293.
- Dyke PJ, Albers JW, Andersen H, et al. Diabetic polyneuropathies: Update on research definition, diagnostic criteria and estimation of severity. Diabetes Metab Res Rev 2011;27:620-628.
- Freeman R. Not all neuropathy is diabetes is of diabetes etiology: A diabéteszes neuropátia differenciáldiagnosztikája. Curr Diabe Rep 2009;9:423-431.
- Balducci S, Iacobellis G, Parisi L, et al. Exercise training can modify the natural history of diabetic peripheral neuropathy. J Diabetes Complications 2006;20:216-223.
- Bril V, England J, Franklin GM, et al. Evidencia alapú iránymutatás: A fájdalmas diabéteszes neuropátia kezelése. Az Amerikai Neurológiai Akadémia, az Amerikai Neuromuszkuláris és Elektrodiagnosztikai Orvosi Társaság és az Amerikai Fizikai Orvosi és Rehabilitációs Akadémia jelentése. Neurology 2011;76:1758-1765.
- Dowell D, Haegerich TM, Chou R. CDC Guideline for prescribing opioids for chronic pain – United States 2016. MMWR Recomm Rep 2016;65:1-49.
- Tesfaye S, Wilhelm S, Lledo A, et al. Duloxetine and pregabalin: High-dose monotherapy or their combination? A “COMBO-DN tanulmány” – multinacionális, randomizált, kettős vak, párhuzamos csoportos vizsgálat diabéteszes perifériás neuropátiás fájdalomban szenvedő betegeken. Pain 2013;154:2616-2625.
- Ahn AC, Bennani T, Freeman R, et al. Two styles of acupuncture for treating painful diabetic neuropathy – a pilot randomized control trial. Acupunct Med 2007;25:11-17.
- Garrow A, Xing M, Vere J, et al. Az akupunktúra szerepe a diabéteszes fájdalmas neuropátia (DPN) kezelésében: A pilot RCT. Acupunct Med 2014;32:242-249.
- Ziegler D, Nowak H, Kempler P, et al. A tüneti diabéteszes polineuropátia kezelése az antioxidáns alfa-liponsavval: A meta-analysis. Diabet Med 2004;21:114-121.
- Ziegler D, Low PA, Litchy WJ, et al. Efficacy and safety of antioxidant treatment with alpha-lipoic acid over 4 years in diabetic polyneuropathy: The NATHAN 1 trial. Diabetes Care 2011;34:2054-2060.
- Kuwabara S, Ogawara K, Harrori T, et al. The acute effects of glycemic control on axonal excitability in human diabetic nerves. Intern Med 2002;41:360-365.
- Peltier A, Goutman SA, Callaghan BC. Fájdalmas diabéteszes neuropátia. BMJ 2014;348:g1799.
- Soykan I, Sivri B, Sarosiek I, et al. Demography, clinical characteristics, psychological and abuse profiles, treatment, and long-term follow-up of patients with gastroparesis. Dig Dis Sci 1998;43:2398-2404.
- Camilleri M, Bharucha AE, Farrugia G. A diabeteses gastroparesis epidemiológiája, mechanizmusai és kezelése. Clin Gastroenterol Hepatol 2011;9:5-12.
- Shin AS, Camilleri M. A diabeteses gastroparesis diagnosztikai értékelése. Diabetes 2013;62:2667-2673.
- Hasler WL, Wilson L, Parkman HP, Lee L. A hasi fájdalom mint tünet jelentősége a gasztroparézisben: Kapcsolat a klinikai tényezőkkel, a betegség súlyosságával, az életminőséggel, a gyomorvisszatartással és a gyógyszerhasználattal. Gastroenterology 2010;138. doi: 10.1016/S0016-5085(10)62131-2.
- Choung RS, Locke GR 3rd, Schleck CD, et al. Risk of gastroparesis in subjects with type 1 and 2 diabetes in the general population. Am J Gastroenterol 2012;107:82-88.
- Maleki D, Locke GR III, Camilleri M, et al. Gastrointestinal tract symptoms among persons with diabetes mellitus in the community. Arch Intern Med 2000;160:2808-2816.
- Bytzer P, Talley NJ, Leemon M, et al. Prevalence of gastrointestinal symptoms associated with diabetes mellitus: A population-based survey of 15,000 adults. Arch Intern Med 2001;161:1989-1996.
- Jones KL, Russo A, Berry MK, et al. A longitudinal study of gastric emptying and upper gastrointestinal symptoms in patients with diabetes mellitus. Am J Med 2002;113:449-455.
- Gaber AO, Hathaway DK, Abell T, et al. Improved autonomic and gastric function in pancreas-kidney vs. kidney-alone transplantation contributes to quality of life. Transplant Proc 1994;26:515-516.
- Punkkinen J, Färkkilä M, Mätzke S, et al. Upper abdominal symptoms in patients with Type 1 diabetes: Nem függnek össze a gyomorürítés autonóm neuropátia okozta károsodásával. Diabet Med 2008;25:570-577.
- Schvarcz E, Palmer M, Aman J, et al. Physiological hyperglycemia slows gastric emptying in normal subjects and patients with insulin-dependent diabetes mellitus. Gastroenterology 1997;113:60-66.
- Miller G, Palmer KR, Smith B, et al. Smoking delays gastric emptying of solids. Gut 1989;30:50-53.
- Rao AS, Camilleri M. Áttekintő cikk: Metoklopramid és tardív diszkinézia. Aliment Pharmacol Ther 2010;31:11-19.
- Patterson D, Abell T, Rothstein R, et al. A double-blind multicenter comparison of domperidone and metoclopramide in the treatment of diabetic patients with symptoms of gastroparesis. Am J Gastroenterol 1999;94:1230-1234.
- Arts J, Holvoet L, Caenepeel P, et al. Klinikai vizsgálat: A botulinum toxin intrapylorikus injekciójának randomizált-kontrollált crossover vizsgálata gasztroparézisben. Aliment Pharmacol Ther 2007;26:1251-1258.
- Friedenberg FK, Palit A, Parkman HP, et al. Botulinum toxin A for the treatment of delayed gastric emptying. Am J Gastroenterol 2008;103:416-423.
- Humanitárius eszközmentesség az Enterra eszközre. Fed Reg 2000;65:78495-78496.
- O’Grady G, Egbuji JU, Du P, et al. High-frequency gastric electrical stimulation for the treatment of gastroparesis: Egy metaanalízis. World J Surg 2009;33:1693-1701.
- Reddymasu SC, Sarosiek I, McCallum RW. Súlyos gasztroparézis: Orvosi terápia vagy elektromos gyomorstimuláció. Clin Gastroenterol Hepatol 2010;8:117-124.
- McCallum RW, Dusing RW, Sarosiek I, et al. Mechanisms of symptomatic improvement after gastric electrical stimulation in gastroparetic patients. Neurogastroenterol Motil 2010;22:161-167.
- Douloumpakas I, Pyrpasopoulou A, Triantafyllou A, et al. Prevalence of musculoskeletal disorders in patients with type 2-es diabetes mellitus: A pilot study. Hippokratia 2007;11:216-218.
- Rosenbloom AL, Silverstein JH, Lezotte DC. A korlátozott ízületi mobilitás gyermekkori diabetes mellitusban a mikrovaszkuláris betegségek fokozott kockázatát jelzi. N Engl J Med 1981;305;191-194.
- Lister DM, Graham-Brown RAC, Burden AC. A diabéteszes cheiroarthropathia feloldása. Br Med J 1986;293:1537.