Az Amerikai Szemészeti Akadémia 2013-as találkozóján részt vettem egy vitában, amely a generikus és a márkás gyógyszerek használatának előnyeiről és hátrányairól szólt. Arra kértek, hogy érveljek a márkás gyógyszerek mellett, de mint a legtöbb vitában, itt is túlzott leegyszerűsítés vakon egyik vagy másik oldalra állni. A valóság ennél bonyolultabb. A generikumok mellett szólnak a költségek, de néha nem ugyanazt a kezelési specifikációt vagy eredményt nyújtják, mint a márkás gyógyszerek, annak ellenére, hogy az Élelmiszer- és Gyógyszerügyi Hivatal erőfeszítéseket tesz ennek biztosítására.
Itt szeretnék beszélni arról, hogy a generikumok miben különbözhetnek az általuk helyettesített márkás gyógyszerektől, és mire kell figyelniük a klinikusoknak.
A bioekvivalencia kérdése
Az új, “innovátor” gyógyszer forgalomba hozatalához szükséges akadályok lényegesen eltérnek a generikus követő gyógyszerekéhez képest. Természetesen részben ez az oka annak, hogy egy márkás gyógyszer többe kerül. Míg a kezdeti innovatív gyógyszernek klinikai vizsgálatokon keresztül kell bizonyítania a biztonságosságot és a hatékonyságot, addig a generikus gyógyszernek csak a bioekvivalenciát kell bizonyítania.
Bár a bioekvivalencia úgy hangzik, mintha biológiai vizsgálatok elvégzését foglalná magában, az FDA meghatározása szerint azt jelenti, hogy be kell bizonyítani, hogy a generikus változat összetevői az eredeti gyógyszer összetevőinek pontos másolatai, beleértve a hatóanyagokat és a segédanyagokat is. (Ha a hatóanyagok és a segédanyagok nem azonosak, a gyógyszer nem minősül generikusnak; ugyanúgy át kell esnie az FDA szokásos jóváhagyásán, mint bármely más új gyógyszernek.) A feltételezés szerint ez azt eredményezi, hogy a generikum ugyanolyan biztonságossággal és hatékonysággal rendelkezik, mint a márkás gyógyszer.
Sajnos az az elképzelés, hogy a generikumok megegyeznek a márkás gyógyszerekkel, mivel az összetevők azonosak, nem feltétlenül igaz. Számos tényező, amely befolyásolja egy helyi gyógyszer hatékonyságát, független az üvegben lévő összetevőktől. Például:
– A palack anyaga számít. Sok márkás gyógyszer összetevői illeszkednek a használt üveg anyagához. Ez minden bizonnyal így volt a latanoprost esetében is, ahol a palack anyagával való kompatibilitás a Xalatan forgalomba hozatalakor a kutatási és fejlesztési folyamat nagy részét képezte. Ezt az FDA közvetlenül nem vizsgálja.
– A palack alakja és mérete befolyásolja a felhasználást. Az innovatív gyógyszerkísérletek nemcsak a gyógyszert tesztelik, hanem a palackot is, amelyben azt a betegekhez juttatják, így a palack alakjának és méretének hatását is figyelembe vették. A generikus gyógyszerek gyártóinak azonban nem kell lemásolniuk a palack formáját és méretét, és ez befolyásolhatja, hogy a betegek mennyire könnyen tudják használni a gyógyszert.
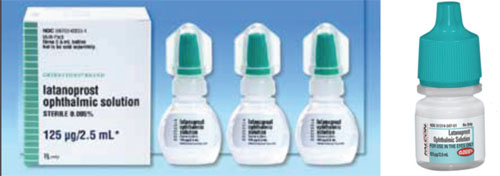
Az egyik kérdés, amely zavart okozhat a márkás gyógyszerről a generikusra, vagy egyik generikusról a másikra való átálláskor, a kupak alakjának és színének különbsége.
A Xalatan például lapos, kis üvegben kerül forgalomba, amelyet csak bizonyos erőfeszítéssel és finomsággal lehet összenyomni ahhoz, hogy egy cseppet be tudjunk csepegtetni. Ezzel szemben a latanoprost egyes generikus palackjai kerekek és merevebbek, így a beteg nehezebben tudja összenyomni a palackot. (Lásd a példákat a szemközti oldalon.) Sok betegünk idős és fizikai korlátokkal küzd. Ha hozzászoktak ahhoz, hogy egy adott lapos és kevésbé merev üveget szorítsanak össze, majd átváltanak egy kerek és merevebb üvegre, akkor az alkalmazás folyamata – és a gyógyszeres kezeléshez való ragaszkodásuk – más lehet, mint amikor az előző üveget használták. Továbbá, mivel a palack formáját és méretét az egyes generikus gyártók választják meg, előfordulhat, hogy a betegek néha lapos, máskor pedig kerek palackban kapják a gyógyszert. Ez sok zavart okozott a betegeink körében.
– A kupak színe nem mindig egyezik. A szemészeti gyógyszeres palackok kupakjainak színét a gyógyszerkategória alapján kell összehangolni. Az FDA igyekszik biztosítani, hogy a szín megfelelő legyen, de előfordult már, hogy más színű kupak csúszott át. Ennek eredményeként néha előfordul, hogy a generikus gyógyszer palack kupakjának színe (valamint alakja és mérete) eltér a márkás gyógyszerétől (lásd a fenti példát). Ez nagy zavart okoz, amikor a betegek megpróbálják megjegyezni, hogy több csepp közül melyik cseppet mikor kell bevenniük.
Még ha a beteg soha nem használta a márkás gyógyszert a megfelelő kupakszínnel, a megváltozott szín akkor is problémát jelent; az új kupak színe valójában lehet, hogy ugyanaz a színű, mint a beteg által szedett másik gyógyszeré. Például a prosztaglandin-analóg flakonoknak elvileg teaszínű kupakkal kell rendelkezniük. Ha a páciense egy olyan generikus változatot használ, amelynek a palackja fehér kupakkal rendelkezik, összetévesztheti más gyógyszercsoportokkal, amelyeknek fehér kupakkal kell rendelkezniük.
– Ha észrevesz egy példát a helytelen kupakszínre, az FDA azt mondta, hogy szeretne hallani róla, hogy lépéseket lehessen tenni az eltérés kijavítására.
– A cseppméret eltérő lehet. A jelenleg forgalomban lévő helyi cseppentős üvegek cseppenként 30-50 µl-es adagot biztosítanak. Sajnos nagy eltérések lehetnek a márkás és a generikus készítmények között, egyszerűen azért, mert a hegynek nagyobb vagy kisebb lyuk lehet. Ez nyilvánvalóan befolyásolhatja, hogy a gyógyszerből mennyi jut ténylegesen a szembe; lehet, hogy kevesebb, lehet, hogy több.
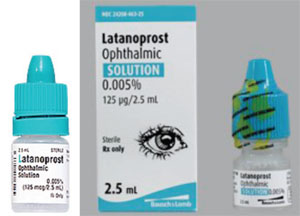
Egy másik probléma a flakon alakja és merevsége közötti különbségek, amelyek megnehezíthetik a cseppek alkalmazását egy idősebb beteg számára. A xalatan például lapos üvegben kerül forgalomba; a gyógyszer számos generikus készítménye kerek üvegben van, amelyet nehezebb összenyomni.
Még érdekesebb, hogy piacra került egy generikus timolol, amelynek a hegyén egyáltalán nem volt lyuk; a betegnek át kellett szúrnia a hegyét, hogy a gyógyszert kivegye, hasonlóan egy tubus pillanatragasztóhoz. Ez sok betegnél zavart okozott; néhányan nem tudták, hogy ezt kell tenniük, és mégis megpróbálták használni a cseppeket. Azt hitték, hogy cseppet tesznek rá, de nem nyitották ki az üveget, így nem jött ki belőle semmi. Mások azt hitték, hogy az üveg hibás vagy üres. Ráadásul a saját készítésű lyuk végül bármilyen méretű lehet, ami befolyásolhatja az adagot, és a lyuk készítésének folyamata könnyen veszélyeztetheti a tartalom sterilitását.
Mindezek a szempontok – a palack anyaga, alakja és mérete, a kupak színe és a cseppnyílás átmérője – nagyon fontosak mind az orvos, mind a beteg számára. Sajnos előfordulhat, hogy ezeket a szempontokat figyelmen kívül hagyják, mert a hangsúly a bioekvivalencia bizonyítására irányul.
– Egy beteg generikus gyógyszere hónapról hónapra másképp nézhet ki. Ez a generikus gyógyszerek másik sajnálatos mellékhatása. Ez azért fordul elő, mert egy adott generikusnak több gyártója is lehet, mindegyiknek más és más az üvege. Például jelenleg hat-nyolc különböző gyártója van a generikus latanoprostnak az amerikai piacon. Az adott gyógyszertár által forgalmazott készítmény változhat, mivel az olyan láncok, mint a CVS, a Walgreens vagy a Walmart általában azt a gyártót választják, amelyik az adott időpontban a legjobb ajánlatot adja a gyógyszertárcsoportnak. Ennek eredményeképpen előfordulhat, hogy egy gyógyszertár megváltoztatja az általa kínált generikus készítményt, ha egy másik generikus gyártótól alacsonyabb ajánlat érkezik. Így még ha a beteg ugyanabba a gyógyszertárba jár is, előfordulhat, hogy különböző időpontokban egy gyógyszer különböző generikus változatát kapja meg. Ez zavaró lehet, ha az üvegek másképp néznek ki és/vagy másképp viselkednek. (Még a tolerancia és az IOP-szabályozás terén is lehet különbség a kettő között.)
A betegtájékoztató
A jelenlegi szabályok megakadályozzák, hogy a gyártók figyelmeztessék az orvosokat vagy a betegeket, még akkor is, ha egy generikus gyógyszerről kiderül, hogy problémás. Van egy szabály, amely előírja, hogy a generikus gyógyszerek gyártóinak az innovatív gyógyszerhez mellékelt betegtájékoztató pontos másolatát kell mellékelniük. Bár ennek a szabálynak az volt a célja, hogy tükrözze azt az elképzelést, hogy a gyógyszerek bioekvivalensek, a nem szándékolt mellékhatás az volt, hogy a generikus gyártókra nem rótták ugyanazokat a gondossági követelményeket és a biztonság garantálásával kapcsolatos terheket, amelyeket a márkagyártóktól megkövetelünk.
Ez azt eredményezte, hogy ha a generikus gyártó bevezet egy gyógyszert a piacra, és észrevesz bizonyos mellékhatásokat vagy nemkívánatos eseményeket, amelyek a generikus termékkel kapcsolatban jelentkeznek, nem változtathatja meg a betegtájékoztatót, hogy figyelmeztesse az orvosokat és a betegeket, hogy probléma állhat fenn. Ráadásul ez a szabály valójában csökkentheti a generikus gyártók motivációját a termékeik megfelelő ellenőrzésére; elvégre nem fenyeget peres eljárás, ha probléma merül fel.
Szerencsére ez a kérdés az FDA tudomására jutott. Az FDA 2013 novemberében olyan szabályra tett javaslatot, amely lehetővé tenné a generikus gyógyszergyártók számára, hogy frissítsék címkéiket, ha potenciális biztonsági aggályokról kapnak információt. Ha ezt elfogadják, ez nagyban hozzájárul a betegek biztonságának biztosításához.
Importált generikumok
A generikumok másik problémája, hogy sok közülük az Egyesült Államokon kívül készül, ahol a minőségellenőrzés néha valóban aggodalomra ad okot. A problémák a gyógyszerekben talált rejtélyes szennyeződésektől kezdve az összetevők tökéletlen egyezésén át egészen az egyenesen csalárd formulákig terjedtek, amelyek egyáltalán nem szolgálnak hasznos célt (ami egyes esetekben súlyos károkat okozhat a betegeknek).
A valóság az, hogy a generikumok nem feltétlenül azonosak a márkás gyógyszerekkel – még akkor sem, ha teljesítették az FDA bioekvivalencia követelményét. Ez azt jelenti, hogy a generikus gyógyszerek használatakor a biztonságosság és a hatékonyság biztosításának terhe minket és betegeinket terheli.
A New York Times szerint az indiai gyógyszeripar jelenleg az Egyesült Államokban elfogyasztott vény nélkül kapható és generikus vényköteles gyógyszerek 40 százalékát adja. Számos gyára világszínvonalú és “gyakorlatilag megkülönböztethetetlen” az amerikai gyártóüzemektől (a Times szerint), kiváló minőségű, megbízható gyógyszereket állítanak elő. Ugyanakkor az Egészségügyi Világszervezet becslése szerint minden ötödik Indiában gyártott gyógyszer hamisítvány. (Hasonló problémákról számoltak be más országokban, köztük Kínában gyártott gyógyszerekkel kapcsolatban is.)
A mi csoportunk néhány évvel ezelőtt végzett egy tanulmányt, amelyben az Indiában gyártott latanoprostot hasonlította össze a Xalatannal. Azt találtuk, hogy a hatóanyagok stabilitása nem volt azonos az idő múlásával vagy hő hatására. Továbbá az összes importált palackban találtunk szennyeződéseket, köztük mikroszkopikus, madzagra emlékeztető szálakat és az általunk “UFO-knak” nevezett dolgokat.”
A lényeg az, hogy a gyártási gyakorlat felügyelete, amely a tengerentúlon történik a nem egyesült államokbeli székhelyű vállalatoknál, különösen azoknál a vállalatoknál, amelyek nem márkás gyógyszereket forgalmaznak, egyszerűen nem ugyanaz.
Egyes orvosok talán azt feltételezik, hogy az ilyen importált gyógyszerek csak akkor jelentenek problémát, ha a betegek az Egyesült Államokon kívül vásárolnak gyógyszereket az interneten keresztül, hogy pénzt takarítsanak meg, de a valóság az, hogy ezek az importált gyógyszerek egyre inkább itthon is elérhetőek. A timolol és a travoprost indiai formulái jelenleg az Egyesült Államokban működő forgalmazókon keresztül kaphatók, és hamarosan más gyógyszerek, például NSAID-ok is elérhetővé válnak. Nyilvánvaló, hogy az Egyesült Államokon kívül számos vállalat állít elő kiváló minőségű generikus gyógyszereket; az aggodalom az, hogy néhányan közülük nem. Ez az orvosokra és a betegekre hárítja azt a terhet, hogy meggyőződjenek arról, hogy egy adott generikus gyógyszer biztonságos és hatékony. (Legalább az Egyesült Államokon belül kapható gyógyszerek átmentek az FDA bioekvivalencia-eljárásán; azok a gyógyszerek, amelyeket egyes betegek az országon kívül az interneten keresztül vásárolnak, nem biztos, hogy átmentek, ami még gyanúsabbá teszi őket.)
Klinikai stratégiák
Az eddig tárgyalt összes változó miatt az orvosoknak szorosan figyelemmel kell lenniük arra, hogy mi történik a betegekkel, amikor egy márkás gyógyszerről egy generikusra vagy egy generikusról egy másikra váltanak. Ébernek kell lennünk, hogy megbizonyosodjunk arról, hogy a szemnyomáskontroll nem ingadozik, és hogy a betegeknél nem jelentkeznek a gyógyszerekkel szembeni intolerancia új jelei és tünetei.
Itt van néhány dolog, amit megtehet betegei (és a rendelője) védelme érdekében:
– Kérje meg a betegeket, hogy hozzák be a cseppjeiket. Megkérem a betegeimet, hogy ezt tegyék meg, függetlenül attól, hogy milyen gyógyszereket használnak, és sokan közülük meg is teszik. Ez lehetőséget ad arra, hogy feljegyezzem, melyik generikus gyártót használják, és mindent megteszek, hogy ezt nyomon kövessem, így ha probléma merül fel, vagy valami megváltozik, meg tudom keresni a lehetséges összefüggést.
– Kérje meg a betegeket, akik új generikusra váltanak, hogy hamarabb térjenek vissza a rendelőbe, mint ahogy egyébként visszahívná őket. Ez lehetővé teszi, hogy megbizonyosodjon arról, hogy nincsenek nemkívánatos következmények. Legyen éber a hatékonyság változásaira vagy új jelekre vagy tünetekre.
– Ha bármilyen problémát észlel, amikor egy beteg generikusra vált, értesítse az FDA-t. Ne feledje, hogy ez a helyzet az orvosra hárítja a terhet, hogy megbizonyosodjon arról, hogy a generikus gyógyszer valóban biztonságos és hatékony.
– Ha egy betegnek nem megy olyan jól a generikus gyógyszer, tegyen erőfeszítéseket annak érdekében, hogy a biztosító fedezze a márkás gyógyszert. Szembesültem már olyan betegekkel, akik jól tűrték a márkás gyógyszert, de nehezen tolerálták a generikust olyan mellékhatások miatt, mint a bőrpír vagy az irritáció. Ezekben az esetekben írunk a biztosítónak, és mindent megteszünk azért, hogy a beteg visszakerüljön a márkás készítményre.
Előfordulhat például, hogy a márkás gyógyszerben van egy bizonyos tartósítószer, míg a generikus készítményben van egy alternatív tartósítószer, amelyre a beteg érzékeny. A Travatan Z az Alcon által gyártott márkás gyógyszer, amely a benzalkónium-klorid helyett a SofZia tartósítószert tartalmazza; a generikus változatok BAK-ot tartalmaznak, mivel bioekvivalenciájuk a travoprost régebbi változatán alapult. Ha egy gyógyszertár a BAK-ra allergiás beteget átállítja a generikus gyógyszerre, az problémássá válik.
Sajnos, mivel évente több ezer beteget látunk a rendelőnkben, nagyon nehéz biztosítani, hogy minden olyan beteg esetében, aki ilyen helyzetbe kerül, megnyerjük a csatát. Mi azonban igyekszünk.
A teher rajtunk van
A generikus gyógyszerek itt vannak, hogy maradjanak, és az összes betegség kezelésének fontos részévé válnak, nem csak a szemészetben. Általában biztonságosak és hatékonyak, és mind a betegek, mind általában az egészségügyi rendszer számára költségmegtakarítást eredményezhetnek. Félreértés ne essék – nagy rajongója vagyok a költségcsökkentésnek. Ha találunk egy biztonságos módot a költségek csökkentésére, miközben fenntartjuk a kiváló ellátást, akkor azt támogatom. Az egyenlet második részét kell szem előtt tartanunk.
Én magam is minden nap használok generikus gyógyszereket, és betegeim túlnyomó többsége már generikus gyógyszereket szed. Majdnem mindannyian nagyon jól vannak, jó IOP-kontrollal és jó toleranciával a gyógyszerekkel szemben. Szóval természetesen nem azt mondom, hogy kerüljük a generikumok használatát. A valóság azonban az, hogy a generikumok nem feltétlenül azonosak a márkás gyógyszerekkel – még akkor sem, ha megfelelnek az FDA bioekvivalencia követelményének. Ez azt jelenti, hogy a generikus gyógyszerek használatakor a biztonságosság és a hatékonyság biztosításának terhe minket és betegeinket terheli. VÉLEMÉNY
Dr. Kahook a denveri Colorado Egyetem orvosi karának The Slater Family Endowed Chair of Ophthalmology és a klinikai és transzlációs kutatás alelnöke. Az Allergan és az Alcon tanácsadója és kutatási támogatásban részesül.