Mi a savasság?
A savasság elengedhetetlen a földi élethez. A savasság gyakran számos anyag tulajdonságait, minőségét, felszívódását és oldhatóságát határozza meg. Így működnek az enzimek, amelyek a szervezetekben szinte minden biológiai folyamatért felelősek, de csak a megfelelő savasság mellett. A vér savasságának kis ingadozása halálos.
Mi a pH?
A pH (pondus Hydrogenii) egy oldat savasságát vagy lúgosságát jelzi. A pH-érték általában 0 és 14 között változik. A 0 és 7 közötti pH-értékkel rendelkező oldat savas, a 7 és 14 közötti pH-értékkel rendelkező pedig lúgos. Az ecet és a kóla pH-értéke 3 alatt van. A szóda és a szappan pH-értéke magasabb, mint 8. A 7-es pH-érték semlegesnek számít. A tiszta víz pH-ja szobahőmérsékleten 7. A csapvíz pH-ja általában egy kicsit magasabb a kalcium jelenléte miatt.
Néhány természetes környezet, például a bőrünk, a növényi szubsztrátumok és a tápközegek enyhén savasak, és pH-értékük 5 és 6,5 között van. Ha megnézzük az emberek által kedvelt dolgokat, azt látjuk, hogy ezek általában enyhén savas vagy semleges anyagok, mint például a víz. A növények is az enyhén savas anyagokat kedvelik. Az 5,5 körüli pH-érték olyan gyakran fordul elő a természetben, hogy egyes növényszakértők ezt az értéket “semlegesnek” tekintik.
Miért fontos a savasság?
A savasság jelentős hatással van számos élelmiszerelem felszívódására és oldhatóságára (lásd az 1. ábrát).
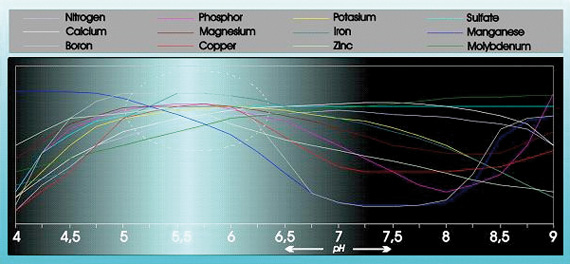
1. ábra
A savasság emellett jelentős hatással van a talaj szerkezetére, a szerves anyagok lebontására és a mikrovilágra. A pH azt is befolyásolja, hogy a termesztőközegben lévő táplálékelemek, nehézfémek, növényvédő szerek és egyéb mikroorganizmusok hogyan mosódnak ki a talajból.
A túl alacsony vagy túl magas pH-érték káros lehet a növényekre nézve, ezért fontos, hogy megfelelő legyen. De honnan tudja, ha a pH rossz? Tapasztalatból! Ezért, hogy segítsünk, felsorolunk néhány tünetet, amit megfigyelhet:
A túl alacsony pH tünetei (a szubsztrát túl savas)
- A legtöbb tápanyag könnyen oldódik, ami mangán-, alumínium- és vastöbbletet okozhat;
- Foszfor-, kálium-, magnézium- és molibdénhiányt okozhat a túlzott öblítés;
- Magnéziumhiány, különösen hideg szubsztrátokban;
- A talaj általában szegényes;
- A talajélet gátolt.
Túl magas pH-érték tünetei (túl lúgos a szubsztrát)
- A legtöbb tápanyag nehezebben oldódik, ami a kalcium-, vas- és foszfátvegyületek kicsapódását okozza;
- Kisebb a mangán, foszfát és különösen a vas, de a réz, cink és bór felszívódása is. Ez különösen nedves, hideg termesztőközegben okoz hiányt.
- Homokos talajokon a szerves anyagok lebomlása jelentősen megnő, ha a pH magas.
Mi határozza meg a pH-t?
Az oldat vagy a szubsztrátum pH-értékét meghatározó egyik legfontosabb tényező a pufferkapacitás. A pufferkapacitás ebben az esetben azt jelenti, hogy egyfajta egyensúly van jelen, amely folyamatosan helyreállítja önmagát. Ha például egy csepp savat teszünk 1 liter csapvízbe, amelynek a pH-értéke 7, az kevéssé befolyásolja a savasságot. Ha azonban egy csepp savat teszünk 1 liter ásványtalanított vízbe (akkumulátorvíz), a pH azonnal drámaian lecsökken. Ennek az az oka, hogy a csapvíz bikarbonátot tartalmaz, míg a de-mineralizált víz nem. A bikarbonát a víz 5,5 és 7,5 közötti pH-értékeinek legfontosabb pufferanyaga.
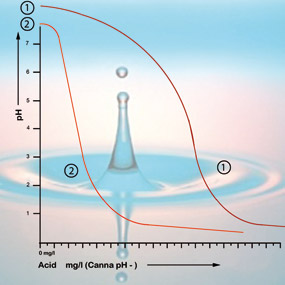 A bikarbonát megköti magát az oldatban lévő savhoz, amely szén-dioxidot bocsát ki a légkörbe. Így semlegesíti a savat, és a savasság változása csak csekély mértékű lesz, amíg még mindig van jelen bikarbonát.
A bikarbonát megköti magát az oldatban lévő savhoz, amely szén-dioxidot bocsát ki a légkörbe. Így semlegesíti a savat, és a savasság változása csak csekély mértékű lesz, amíg még mindig van jelen bikarbonát.
5,3 pH-értéknél az összes bikarbonát elfogyott, és az oldatban nincs több puffer. A pH most már instabil, és azonnal megváltozik, ha sav hozzáadására kerül sor (lásd a 2. ábrát). A bikarbonáttartalom alapján tehát kiszámítható, hogy mennyi sav szükséges ahhoz, hogy a tápoldat a megfelelő savasságú legyen. A csapvíz bi-karbonáttartalmát általában a vízszolgáltató adja meg milligramm/literben.
A pufferkapacitás és a szubsztrát savassága függ annak összetételétől és frissességétől. A szerves anyag, a kalcium és a bikarbonát jelenléte általában meghatározza a pH-értéket. Az agyag mindig tartalmaz kalcium-karbonátot, és viszonylag magas pH-értékkel rendelkezik, amelyet nehéz megváltoztatni, míg a tőzeg és a homokos talajok savasak.
A savasságra maga a növény is nagy hatással van. A gyökerek a növény fejlődési stádiumától, a rendelkezésre álló tápláléktól, a gyökérhőmérséklet és a fényintenzitás különbségeitől függően savas vagy lúgos szubsztanciákat választanak ki. Így érthető, hogy miért ingadozhat folyamatosan a gyökérkörnyezet pH-ja. Egy kifinomult táplálkozási egyensúly a fejlődés különböző fázisaiban a gyökérkörnyezet pH-értékét elfogadható határokon belül tartja.
A mikroélet, a CO2-szint és az algák növekedése szintén hatással lehet a gyökérkörnyezet és a tápoldat tartály savasságára.
A pH-érték mérése

A pH-érték mérése meglehetősen egyszerű – szükség van néhány pH-indikátorra, például lakmuszpapírra vagy pH-tesztkészletre. Ezek viszonylag olcsók, de nem mindig pontosak, és néha 1-2 pH-egységgel eltérhetnek. Minden pH-mérő általában drágább, és a pontosság a mérőeszköz típusától és a kalibráló folyadékkal történő rendszeres kalibrálástól függ.
Minták vétele

A növények öntözéséhez használt víz pH-ja fontos, de a gyökerek körüli savasság is lényeges. Ezért a pH mérésekor nagyon fontos, hogy a megfelelő módon vegyük a mintát, hogy jó eredményeket kapjunk. A minta a gyökérkörnyezetben lévő savasság kora.
Egyszerű a mintavétel és a pH mérése egy recirkulációs rendszerben, egyszerűen mérje meg a recirkulált tápoldatot.
A recirkuláció nélküli szubsztrátrendszerekben a tápoldatot a szubsztrátból (kőzetgyapot, agrofoam stb.) több helyen is kivonják. A szakértők egy éve és egy napja vitatkoznak arról, hogy honnan vegyenek mintát. Mi azt javasoljuk, ahogy számos neves laboratórium is teszi, hogy a gyökerek helyéről vegyünk mintát, ami a csepp- pers alatt és körül van. Vegyünk kis mintákat a lehető legtöbb helyről. Mindig minden mintát egy időben vegyünk, és lehetőleg a második csepegtetés után, a fény – nappal – ciklus alatt.
 A talaj, kókusz és tőzeg szubsztrátokból csak vegyünk kis mennyiségű szubsztrátot több helyről.
A talaj, kókusz és tőzeg szubsztrátokból csak vegyünk kis mennyiségű szubsztrátot több helyről.
A mintánk savasságát az “1:1,5 térfogatkivonat” módszerrel tudjuk a legjobban megmérni. Ezt könnyen elvégezheted magad is, ha a termesztőközeget olyan nedvessé teszed, hogy a víz átfolyik az ujjaidon, amikor elég erősen összegyúrod és összenyomod (1. kép). Használjon például egy 250 ml-es mérőpoharat. Töltse meg a mérőpoharat 150 ml-re ásványmentesített vízzel. Adjunk hozzá táptalajt, amíg a térfogat el nem éri a 250 ml-t (2. kép). Jól rázza össze, és hagyja állni néhány órán át. Ezután szűrjük le, és mérjük meg a pH-t.

A helyes pH-értékek minden táptalajhoz
A táptalajban történő termesztés esetén a gyökérkörnyezet számára az 5,0 és 6,4 közötti pH-értékek megfelelőek. Nem lesz semmilyen káros hatása, ha az értékek kicsit magasabbak vagy alacsonyabbak. Közvetlen káros hatások csak 4-nél alacsonyabb és 8-nál magasabb értékeknél jelentkeznek, a 4-nél alacsonyabb pH-érték gyakran azonnali károsodást okoz a gyökerekben. Ezenkívül a nehézfémek, köztük a mangán és a vas olyan jól felszívódnak, hogy megmérgezik a növényt (nekrózis). A 7 és 8 közötti értékek nem károsítják azonnal a növényt. Az olyan tápanyagok, mint a vas, a foszfát és a mangán ekkor kevésbé állnak rendelkezésre, ami hosszú távon hiányállapotokhoz (klorózis és fejlődési problémák) vezet.
A pH-érték korrigálása
 Ha a gyökérkörnyezet savassága 5 és 6,4 között van, akkor a termesztési környezet pH-ja rendben van, és nem kell semmilyen korrekciós intézkedést tennie. Próbáld meg elkerülni a pH-érték korrekcióját, hacsak nem feltétlenül szükséges. Inkább árt, mint használ; a növény szereti a nyugalmat és a békét. Sokkal fontosabb, hogy hosszabb időn keresztül figyelje, hogyan változik a savtartalom. Ha az érték pH 5 alá csökken vagy pH 6,4 fölé emelkedik, akkor célszerű fokozatosan elkezdeni a korrekciót.
Ha a gyökérkörnyezet savassága 5 és 6,4 között van, akkor a termesztési környezet pH-ja rendben van, és nem kell semmilyen korrekciós intézkedést tennie. Próbáld meg elkerülni a pH-érték korrekcióját, hacsak nem feltétlenül szükséges. Inkább árt, mint használ; a növény szereti a nyugalmat és a békét. Sokkal fontosabb, hogy hosszabb időn keresztül figyelje, hogyan változik a savtartalom. Ha az érték pH 5 alá csökken vagy pH 6,4 fölé emelkedik, akkor célszerű fokozatosan elkezdeni a korrekciót.
A savasság korrigálása a legegyszerűbben úgy érhető el, hogy a növekedési fázisban salétromsavval, a virágzási fázisban foszforsavval csökkentjük a tápoldat savasságát, vagy adott esetben maró káliummal, kálium-hidrogénkarbonáttal és CANNA RHIZOTONIC-kal növeljük azt. Ügyeljünk arra, hogy a használt oldat pH-ja ne csökkenjen túlságosan 5,0 alá. A kőzetgyapotban történő termesztés során a szálak károsodnak, ami nagyon alacsony pH-értékeknél sok lúgos anyag felszabadulását okozza. Ráadásul a pH-t nehezebb szabályozni a bikarbonát hiánya miatt
A gyökérkörnyezet magas pH-ját a felhalmozódott bikarbonát is okozhatja. Ennek orvoslására tartsa fenn a 20%-os vízelvezetést, vagy öblítse át savasabb oldattal.
A pH-méréseket mind a hozzáadott oldatból, mind az aljzatban lévő tápoldatból hasznos feljegyezni. Jó képet kaphat a pH alakulásáról és a megtett intézkedések hatásáról.
- A fehérjebontó enzimeknek savas környezetre (gyomornedv), a szénhidrátbontó enzimeknek pedig lúgos környezetre (nyál) van szükségük.
- Az oldat savasságát a hidrogénionok (= savas) és a hidroxidionok (= lúgos) aránya határozza meg.
- Hiányt okozhat, hogy a növénynek protonokat kell kiválasztania, hogy fel tudja venni ezeket a molekulákat. Egy alacsony pH-jú termesztőközegben már nagyon sok proton van. Ezek az elemek ki is ömlenek, mert a protonok taszítják a molekulákat a közegből a szubsztrátumba.
- A bikarbonát az az anyag, amely a kalciummal együtt a vízkőért felelős. A nátriummal kombinálva a bikarbonátot gyógyszerekben használják a túlzott gyomorsav ellen (Alka-seltzer).
- Néhány laboratóriumban a bikarbonátkeménységgel is dolgoznak. Ahhoz, hogy ezt mg/l bikarbonátra fordítsuk át, a bikarbonátkeménységet meg kell szoroznunk 21,8-cal.
Például: a bikarbonátkeménység 11, akkor 1 liter vízben (11 x 21.8=) 240 mg/liter bikarbonátot. -
Homokos talaj: Gazföld pH 4,6 … 5,2 Épített föld pH 5,0 … 5. 5.6 Agyag: tengeri agyag pH 6.0 … 7.2 folyami agyag pH 6.2 … 6.4 agyag: feldolgozatlan pH 4.0 - Ha jelentős algásodás van, akkor a pH emelkedik, mert a szén-dioxidot eltávolítják az oldatból. A baktériumok képesek átalakítani a nitrogén bizonyos formáit, így azok savasító hatásúak. A levegőben lévő nagy mennyiségű CO2 több szén-dioxidot generál a tápoldatban és fordítva.
- A szódát csak kis mennyiségben használjuk, mert nátriumot tartalmaz, és a növényeknek csak nagyon kis mennyiségű nátriumra van szükségük. Ne feledjük, hogy a magas nátriumkoncentráció károsítja a növényt.
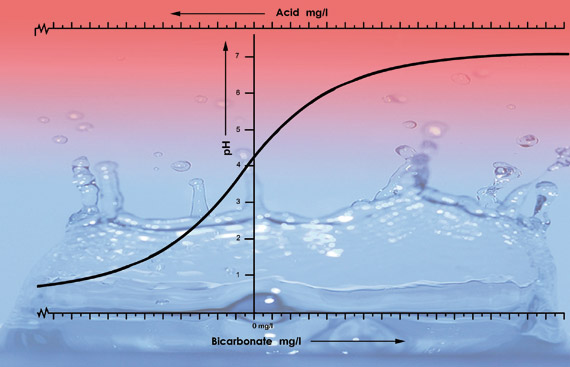
Illusztráció a különböző területekről származó csapvíz pH-értékeiről, eltérő bikarbonát-tartalommal. Az egyes víztípusok 100 literes mintáihoz 33 ml salétromsavat (38%) adtunk. A pH-görbe a pH 5,3 után gyorsabban csökken, mert ennél a víztípusnál a sav az összes bikarbonátot semlegesíti. A pH 5,3 alatt a savassági szint gyorsan felgyorsul.
A recirkulációs rendszerekben a pH-érték jobban ingadozhat, mint a run-to-waste rendszerekben. Ugyanez vonatkozik az EC, ppm értékre is. Ha többet szeretne megtudni az EC-ről, a pH-ról és a ppm-ről, javasoljuk, hogy olvassa el a Mindent az EC-ről, a pH-ról és a ppm-ről az AQUA használatával című cikkünket.