2013年の米国眼科学会で、私はジェネリック医薬品と先発医薬品を使うことの長所と短所に関する討論に参加しました。 私は先発医薬品を支持するよう求められたのですが、ほとんどのディベートでそうであるように、盲目的にどちらかの側に立つのは単純化しすぎです。 現実はもっと複雑です。 ジェネリック医薬品はコスト面では有利ですが、食品医薬品局の努力にもかかわらず、先発医薬品と同じ治療仕様や結果が得られないことがあるのです。
ここでは、ジェネリック医薬品が先発医薬品とどのように異なるのか、また、臨床医がどのような点に注意しなければならないのかについてお話したいと思います。 もちろん、それが先発医薬品が高価である理由の一つでもある。 新薬が臨床試験を通じて安全性と有効性を証明しなければならないのに対し、ジェネリックは生物学的同等性を示すだけでよいのである。
生物学的同等性というと、生物学的な研究を行うように聞こえますが、FDAの定義では、ジェネリック医薬品の成分が、有効成分と賦形剤の両方を含む先発医薬品の成分と正確にコピーされていることを証明しなければならないということなのです。 (有効成分と賦形剤が同一でない場合、その医薬品はジェネリック医薬品とはみなされず、他の新薬と同様に通常のFDA承認を受けなければならない)。 その前提は、ジェネリック医薬品が先発医薬品と同じ安全性と有効性を持つことです。
残念ながら、成分が同じだから先発医薬品と同等という考え方は、必ずしも正しくありません。 外用薬の効能を左右する要因の多くは、ボトルの中の成分とは無関係なのです。 例えば、
-ボトルの材質は重要です。 多くのブランド薬の成分は、使用されているボトルの素材にマッチしているのです。 これは確かにラタノプロストの場合であり、キサラタンを市場に出す際には、ボトル素材との適合性が研究開発の大きな部分を占めていた。 これはFDAが直接調査することではありません。
-ボトルの形や大きさは使用に影響する。 イノベーター医薬品の試験では、医薬品だけでなく、患者さんに届けられるボトルも試験されるため、ボトルの形状や大きさが与える影響も考慮されています。
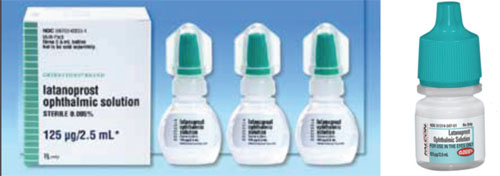
先発医薬品から後発医薬品へ、あるいは後発医薬品から別の医薬品へ変更する際に、混乱を招く問題のひとつにキャップの形や色の違いが挙げられます。
例えば、キサラタンは平らで小さなボトルに入っており、一滴を入れるために絞るのにそれなりの努力と工夫が必要です。 一方、ラタノプロストの一部のジェネリックボトルは丸くて硬いため、患者がボトルを絞るのが難しくなっています。 (患者さんの中には、高齢で体力に自信のない方も少なくありません。 もし、平らで硬度の低いボトルに慣れていて、丸くて硬度の高いボトルに変えたら、塗布の仕方や服薬の仕方も前のボトルを使っていたときと違ってしまうかもしれません。 また、ボトルの形状や大きさはジェネリック医薬品メーカーごとに異なるため、患者さんの手元に届くのは平らなボトルと丸いボトルということもあるようです。 そのため、患者さんには大変ご迷惑をおかけしています。
– キャップの色がいつも同じとは限らない。 眼科用医薬品のキャップの色は、医薬品のカテゴリーに基づいてコーディネートされることを意図している。 FDAはその色が正しいことを確認しようとしますが、違う色のキャップがすり抜けたケースもあるようです。 その結果、ジェネリック医薬品のボトルキャップの色(形状やサイズも)が先発医薬品と異なることがあります(上記例参照)。 そのため、患者さんが数種類の薬のどれをどのタイミングで飲めばいいのかわからなくなってしまうのです。
正しいキャップの色の先発医薬品を使ったことがなくても、色が変わるのは問題です。新しいキャップの色は、実は患者さんが服用している別の薬と同じ色かもしれません。 例えば、プロスタグランジンアナログのボトルは、ティールカラーのキャップであることが想定されています。
キャップの色が正しくない例に気づいたら、FDAは、その不一致を修正するための措置を講じるために、それについて聞きたいと言っています。 現在市販されている外用ドロップボトルは、1滴あたり30~50μlの量を供給しています。 残念ながら、先端の穴が大きかったり小さかったりするだけで、先発品と後発品の間で大きなばらつきが生じることがあります。
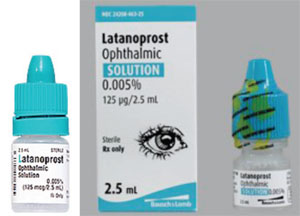
もうひとつの問題は、ボトルの形や硬さの違いで、高齢の患者さんにとって点眼が難しくなることがあります。 例えば、キサラタンは平らなボトルに入っていますが、多くのジェネリック医薬品は丸いボトルに入っていて、絞りにくいのです。
さらに興味深いのは、先端にまったく穴が開いていないチモロールのジェネリック医薬品が発売されたことで、瞬間接着剤のチューブと同じように、先端を刺して薬を取り出す必要がありました。 そのため、多くの患者さんが混乱し、中にはそのことに気づかず、そのまま使おうとしてしまう人もいました。 点滴をしているつもりでも、ボトルを開けていないので、何も出てこないのです。 また、ボトルが不良品か空っぽだと思った人もいた。
ボトルの材質、形状、サイズ、キャップの色、滴下口の直径など、これらの考慮事項はすべて、医師と患者の両方にとって非常に重要である。 残念ながら、生物学的同等性を証明することに重点が置かれているため、こうした配慮が見落とされている可能性があります
-患者のジェネリック医薬品は、月ごとに違って見えることがあります。 これもジェネリック医薬品の残念な副作用のひとつです。 これは、1つのジェネリック医薬品に複数のメーカーが存在し、それぞれが異なるボトルを使用しているために起こります。 例えば、ラタノプロストのジェネリック医薬品には、現在、米国で6~8社のメーカーがあります。 CVS、ウォルグリーン、ウォルマートなどのチェーン店は、通常、薬局グループにとってその時点で最もお得なメーカーを選ぶので、ある薬局が販売するものは変わる可能性があります。 その結果、薬局は、他のジェネリック医薬品メーカーからより低い入札があった場合、提供するジェネリック医薬品を変更する可能性があります。 そのため、同じ薬局に通っている患者さんでも、その時々で異なるジェネリック医薬品を手にすることになります。 そのため、同じ薬局に通っている患者さんでも、その時々で異なるジェネリック医薬品を手にすることになる。 (
添付文書
皮肉なことに、ジェネリック医薬品に問題があることが判明しても、現在のルールでは、メーカーは医師や患者に警告を出すことができません。 ジェネリック医薬品メーカーには、新薬に添付されている添付文書の完全なコピーを添付しなければならないという規則があるのです。 このルールは、医薬品が生物学的に同等であるという考え方を反映させることを意図していますが、意図しない副作用として、先発医薬品メーカーに要求するのと同じ注意義務や安全性確保の負担を後発医薬品メーカーに負わせることを回避してしまっているのです。
その結果、後発医薬品メーカーがある医薬品を市場に導入し、後発医薬品で発生した何らかの副作用や有害事象に気づいたとしても、問題があるかもしれないと医師や患者に警告するために添付文書を変更することが許されないのです。 また、このルールは、ジェネリック医薬品メーカーが自社製品のモニタリングを十分に行おうとする意欲をかえって削ぐことにもなりかねません。 2013年11月、FDAは、ジェネリック医薬品メーカーが安全性に関する潜在的な懸念の情報を得た場合、ラベルを更新することを認める規則を提案しました。
輸入されたジェネリック医薬品
ジェネリック医薬品のもう一つの問題は、その多くが米国外で製造され、品質管理が懸念されることがある点です。 謎の不純物が含まれていたり、成分照合が不完全であったり、まったく役に立たない不正な処方(場合によっては患者さんに重大な損害を与える可能性がある)など、さまざまな問題があります。
ジェネリック医薬品は、FDAの生物学的同等性要件を満たしていても、必ずしも先発医薬品と同じとは限らないというのが実情です。 つまり、ジェネリック医薬品を使用する場合、安全性と有効性を確保する責任は私たちと患者さんにあるのです。
ニューヨーク・タイムズ紙によると、インドの製薬業界は現在、米国で消費される一般用医薬品とジェネリック処方薬の40パーセントを供給しているとのことです。 その工場の多くは世界トップクラスで、米国の製造施設と「事実上区別がつかない」(タイムズ紙より)ほどで、高品質で信頼性の高い医薬品を生産しています。 しかし同時に、WHO(世界保健機関)は、インドで製造される医薬品の5つに1つは偽物であると推定している。 (同様の問題は、中国を含む他の国で製造された医薬品でも報告されています。)
私たちのグループは、数年前にインドで製造されたラタノプロストとXalatanを比較する研究を行いました。 その結果、有効成分の経時的安定性や熱に対する安定性が同じでないことがわかりました。 さらに、すべての輸入ボトルから、糸状の微小なフィラメントや「UFO」と呼ばれるものなどの汚染物質が見つかりました。
ポイントは、米国に拠点を置かない企業、特にブランド薬を市場に出していない企業の、海外で行われる製造慣行の監視は、同じではないということです。
医師の中には、このような輸入医薬品は、患者がお金を節約するためにインターネットを通じて米国外で医薬品を購入するときだけの問題だと考える人もいるかもしれませんが、現実には、これらの輸入医薬品がここでますます入手できるようになっています。 チモロールやトラボプロストのインド製剤は現在、米国に拠点を置く販売業者を通じて入手可能であり、NSAIDsなど他の医薬品も間もなく入手できるようになる予定です。 もちろん、米国外の多くの企業は高品質のジェネリック医薬品を製造していますが、懸念されるのは、そのうちの数社がそうでないことです。 そのため、あるジェネリック医薬品が安全で効果的であるかどうかを確認する負担が医師や患者さんにかかることになります。 (少なくとも、米国内で入手可能な医薬品はFDAの生物学的同等性プロセスを経ていますが、一部の患者がインターネットを通じて国外で購入する医薬品はそうではないため、さらに疑わしいものとなります。)
クリニック戦略
これまで述べてきたすべての変動要因を考慮し、医師は患者が先発医薬品から後発医薬品へ、あるいは後発医薬品から別の医薬品へ切り替える際に何が起こっているかを注視しておくことが必要です。 眼圧コントロールが揺らいでいないか、患者が薬に対する不耐性の新たな兆候や症状を呈していないか、用心しなければなりません。
患者(および診療所)を守るためにできることをいくつか挙げてみましょう。 私は、どの薬を使用しているかにかかわらず、患者さんにこのことをお願いしており、多くの患者さんがそうしています。 そうすることで、どのジェネリックメーカーを使っているかを記録し、問題が発生したり、何かが変わったりしたときに、その関連性を探すことができるよう、最善を尽くす。 そうすることで、不都合な結果が起きていないことを確認することができます。 効能の変化や新たな兆候や症状に注意すること
-患者がジェネリックに切り替えた際に何らかの問題が生じた場合は、FDAに警告すること
-患者がジェネリックに切り替えた際に、新たな兆候や症状が生じた場合は、FDAに警告すること。 この場合、ジェネリック医薬品が本当に安全で効果的であることを確認する責任が医師にあることを忘れないでください。
– もし患者がジェネリック医薬品でうまくいかない場合は、保険会社が先発医薬品をカバーするように努力しましょう。 私は、先発医薬品には耐えられるが、赤みや刺激などの副作用のためにジェネリック医薬品に耐えることが困難な患者さんに直面したことがあります。 そのような場合は、保険会社に手紙を書いて、患者さんを先発製剤に戻してもらえるよう、できる限りの努力をします。
例えば、先発品には特定の防腐剤が入っているが、後発品には患者さんが敏感な別の防腐剤が入っていることがあります。 トラバタンZはアルコン社製の先発医薬品で、塩化ベンザルコニウムの代わりにソフジアという防腐剤を使用していますが、後発医薬品は生物学的同等性が旧バージョンのトラボプロストに基づいているため、BAKを含んでいます。 薬局がBAKにアレルギーのある患者をジェネリック医薬品に切り替えた場合、問題になります。
残念ながら、私たちの診療所では年間数千人の患者を診ているので、この状況に陥ったすべての患者のために勝利を収めることは本当に難しいのです。 しかし、私たちは努力しています。
負担は私たちに
ジェネリック医薬品は、眼科だけでなく、あらゆる病気の治療の主要な部分になりつつあります。 ジェネリック医薬品は一般的に安全で効果的であり、患者さんと医療制度全般の両方にコスト削減をもたらすことができます。 私はコスト削減の大ファンなのです。 優れた医療を維持しながらコストを削減できる安全な方法を見つけることができれば、私は大賛成です。 私自身、毎日ジェネリック医薬品を使用していますし、現在、私の患者の圧倒的大多数がジェネリック医薬品を使用しています。 私自身、毎日ジェネリック医薬品を使用していますが、圧倒的多数の患者さんがジェネリック医薬品を使用しており、眼圧コントロールや薬物への耐性も良好で、ほぼ全員が非常によくやっています。 ですから、ジェネリック医薬品の使用を避けるべきだとは、確かに言いません。 しかし、ジェネリック医薬品は、FDAの生物学的同等性要件を満たしていても、必ずしも先発医薬品と同じであるとは限らないのが実情です。 つまり、ジェネリック医薬品を使用する場合、安全性と有効性を確保する責任は、私たちと患者さんにあるのです。 レビュー
カフック博士は、デンバーのコロラド大学医学部で眼科のスレーター・ファミリー寄付講座および臨床・トランスレーショナル・リサーチの副教授を務めています。 また、アラガン社およびアルコン社のコンサルタントであり、研究支援を受けている。