Diabetes mellitus is duur, maar het grootste deel van de kosten wordt toegeschreven aan complicaties en ziekenhuiszorg.1 Volgens de American Diabetes Association (ADA) bedroegen de totale kosten van diabetes in 2012 naar schatting $245 miljard.1 Naar schatting 43% kwam voor rekening van intramurale ziekenhuiskosten en nog eens 18% voor recepten om de complicaties van diabetes te beheersen.1
De meeste van deze complicaties kunnen worden voorkomen met gerichte glucosecontrole. Epidemiologische gegevens tonen aan dat voor elk procentpunt dat het hemoglobine A1c (HbA1c) daalt, het risico op microvasculaire complicaties met 35% afneemt.2 Het goede nieuws is dat de complicatiecijfers bij diabetes zijn gedaald,3 maar dit is ingehaald door de pure toename van het aantal mensen met diabetes dat complicaties krijgt.
Veel mensen met type 2 diabetes kunnen op het moment van diagnose een diabetesgerelateerde complicatie hebben. Zowel bij type 1- als type 2-diabetes zijn sommige complicaties, zoals retinopathie en nefropathie, geruisloos. Dit vereist een agressieve gerichte aanpak omdat wachten op symptomen te laat zal zijn. Zelfs diabetische neuropathie zal asymptomatisch zijn bij tot 50% van de mensen met meetbare afwijkingen.4
In dit artikel worden de aanbevelingen uit de ADA 2017 Standards of Care voor microvasculaire complicaties en relevante standpuntverklaringen besproken, en worden preventieve screening en klinische parels belicht voor de eerstelijnsarts die patiënten met diabetes behandelt.
- Diabetische retinopathie
- Tabel 1. Retinopathiestadia met beschrijving
- Clinical Pearls
- Diabetes Kidney Disease
- Tabel 2. Belangrijkste studies die aantonen dat de glycemie onder controle blijft met een A1c lager dan 7%
- Tabel 3. Estimated GFR with Stage and Description
- Tabel 4. Albuminurie-categorieën bij CKD
- Figuur 1. Voorgestelde evaluatiefrequentie (aantal keren per jaar) per eGFR- en albuminuriecategorie
- Tabel 5. Red Flags Suggesting Nondiabetic Glomerular Disease
- Tabel 6. Dosisaanpassingen en aanbevelingen voor glucoseverlagende middelen bij patiënten met nierinsufficiëntie
- Klasse
- Medicatie
- Clinical Pearls
- Diabetische Perifere Neuropathie
- Tabel 7. Andere oorzaken van neuropathie67
- Tabel 8. Tabel 8. Vaak gebruikte farmacologische middelen voor DPN4,69
- Clinical Pearls
- Gastroparese
- Clinical Pearls
- Diabetische Cheiroarthropathie
- Conclusie
Diabetische retinopathie
Diabetische retinopathie is een veel voorkomende microvasculaire complicatie van type 1 en type 2 diabetes. Naar schatting 3,7 miljoen mensen wereldwijd zijn matig tot ernstig visueel gehandicapt als gevolg van diabetische retinopathie, en meer dan 800.000 mensen wereldwijd zijn blind als gevolg van diabetische retinopathie.5 Het is de meest voorkomende oorzaak van nieuw ontstane blindheid bij volwassenen tussen 20-74 jaar.6 Er zijn sterke correlaties gelegd met glykemische controle, bloeddrukcontrole, en ziekteduur. Door vroege, regelmatige screening en controle van deze risicofactoren kan diabetische retinopathie worden opgespoord en behandeld om visusstoornissen te voorkomen.
Duur van diabetes is de grootste risicofactor voor de progressie van diabetische retinopathie. Bij type 1-diabetes komt retinopathie in de eerste 3-5 jaar of vóór de puberteit zelden voor.7 In de daaropvolgende 20 jaar zullen bijna alle patiënten met type 1-diabetes diabetische retinopathie ontwikkelen.7 Bij patiënten met type 2-diabetes zal maar liefst 21% op het moment van de diagnose een zekere mate van retinopathie hebben.7 Chronische hyperglykemie, nefropathie, hypertensie en dyslipidemie zijn andere factoren die het risico op of de samenhang met diabetische retinopathie vergroten.8 Tot 50% van de patiënten met albuminurie (ongeacht de geschatte glomerulaire filtratiesnelheid) zal retinopathie hebben.9 Tabel 1 beschrijft de verschillende stadia van retinopathie.
Tabel 1. Retinopathiestadia met beschrijving |
|
|
Stadium |
Beschrijving |
|
Mild Non-Proliferatieve Diabetische Retinopathie |
Microaneurysma’s aanwezig |
|
Meerdere Niet-Proliferatieve Diabetische Retinopathie |
Microaneurysma’s, retinale dot of blot bloedingen, harde exsudaten, of wattenvlekjes kunnen aanwezig zijn |
|
Severe Niet-Proliferatieve Diabetische Retinopathie |
Intraretinale bloedingen, veneuze beading, of intraretinale microvasculaire afwijkingen kunnen aanwezig zijn |
|
Proliferatieve Diabetische Retinopathie |
Neovascularisatie, glasvocht- of preretinale bloedingen aanwezig |
Pathofysiologie. Milde, niet-proliferatieve afwijkingen die worden gekenmerkt door een verhoogde vasculaire permeabiliteit kunnen overgaan in matige tot ernstige nonproliferatieve diabetische retinopathie (NPDR).7 Proliferatieve diabetische retinopathie wordt gekenmerkt door de proliferatie van nieuwe retinale bloedvaten.7 Maculair oedeem, een verdikking van het centrale netvlies met exsudatie en oedeem, kan zich in elk stadium van retinopathie voordoen.7 Diabetische retinopathie kan worden versneld door zwangerschap, puberteit, gebrek aan glycemische controle, hypertensie en cataractchirurgie.7
Het voorkomen van diabetische retinopathie. Glycemische controle is de sleutel tot het voorkomen van diabetische retinopathie. In de Diabetes Control and Complications Trial (DCCT) evalueerden onderzoekers het effect van strenge glykemische controle en progressie van geen of minimale retinopathie op baseline naar matige NPDR.10 Bij patiënten in de groep met intensieve therapie die op baseline geen retinopathie hadden, was het gemiddelde risico op retinopathie over 36 maanden met 76% verminderd.10 Bij patiënten in de groep met intensieve therapie die al een minimale tot matige NPDR vertoonden, was het risico op progressie 54% lager dan bij patiënten die de conventionele behandeling gebruikten.10 In de oorspronkelijke Action to Control Cardiovascular Risk in Diabetes (ACCORD) trial werden deelnemers met diabetes type 2 die al 10 jaar diabetes hadden en waarvan bekend was dat ze hart- en vaatziekten hadden, gerandomiseerd naar intensieve of standaardtherapie voor glykemie, systolische bloeddruk, en dyslipidemie. Vier jaar later was de progressie van retinopathie verminderd bij diegenen met voorafgaande intensieve glycemiecontrole, ongeacht vergelijkbare huidige HbA1c-niveaus.11 Vergelijkbare erfeniseffecten werden niet gezien in de groepen met intensieve bloeddrukcontrole of met fenofibraat voor dyslipidemie.11
Screening. Aangezien maculair oedeem en proliferatieve diabetische retinopathie asymptomatisch kunnen zijn, is screening van vitaal belang voor vroege opsporing en behandeling. Bij patiënten met diabetes type 1 moet vijf jaar na de diagnose met screening worden begonnen.8 Bij patiënten met diabetes type 2 moet bij de diagnose met screening worden begonnen.8 De screening moet worden uitgevoerd door een oogarts of optometrist die ervaring heeft met diabetische retinopathie. De screening moet worden uitgevoerd met verwijding van de ogen. Als er al retinopathie aanwezig is, wordt doorverwijzing naar een oogarts aanbevolen.8 Jaarlijks moet een herhaalde evaluatie worden uitgevoerd als er minimale of geen ziekte wordt gevonden.8
Zwangerschap is een periode met een hoog risico op proliferatieve retinopathie. Bij zwangere vrouwen met reeds bestaande diabetes type 1 of 2 moet het oogonderzoek voor de conceptie of in het eerste trimester plaatsvinden. De onderzoeken moeten elk trimester en een jaar na de bevalling worden herhaald.8 Voor mensen met zwangerschapsdiabetes zijn na de bevalling geen aanvullende oogonderzoeken nodig.
Zwangerschap bij patiënten met reeds bestaande type 1- of type 2-diabetes kan leiden tot een snelle progressie van diabetische retinopathie. Dit geldt vooral als er sprake is van een slechte glycemische controle op het moment van de conceptie.14 Vrouwen met diabetes die zwanger zijn of van plan zijn zwanger te worden, moeten voor de conceptie worden geadviseerd over het risico van ontwikkeling of progressie van diabetische retinopathie en de noodzaak van glycemische controle.8 Een snelle verslechtering van de retinopathie kan echter optreden bij een snelle implementatie van intensieve glycemische controle als er al retinopathie aanwezig is.8 Diabetes tijdens de zwangerschap lijkt niet hetzelfde risico te geven op het ontwikkelen van diabetische retinopathie tijdens de zwangerschap.8
Behandeling. Naast glycemische controle is ook aangetoond dat bloeddrukcontrole (< 140 mmHg systolisch) de progressie van diabetische retinopathie vermindert, maar er is geen extra voordeel van een strikte controle van de systolische bloeddruk < 120 mmHg.12 Fenofibraat kan ook de progressie van diabetische retinopathie vertragen, vooral bij zeer milde NPDR, bij patiënten met dyslipidemie.13 Aspirine bleek geen effect te hebben op de progressie van retinopathie, de ontwikkeling van glasvochtbloeding, of de duur van glasvochtbloeding, en het kan veilig worden gebruikt voor andere medische indicaties zonder oogletsel.7
De behandeling van patiënten met diabetes moet aanbevelingen voor lichaamsbeweging omvatten. Degenen met milde nonproliferatieve retinopathie kunnen veilig beginnen met lichamelijke activiteit. Patiënten met matige nonproliferatieve retinopathie moeten echter activiteiten vermijden die de bloeddruk sterk verhogen, zoals powerlifting.15 Patiënten met ernstige nonproliferatieve of instabiele retinopathie moeten elke fysieke activiteit vermijden die krachtig is (springen, schokken), alle activiteiten met het hoofd naar beneden en het inhouden van de adem.15 In het geval van een glasvochtbloeding mag niet aan lichaamsbeweging worden gedaan.15
Eerdere detectie van diabetische retinopathie is belangrijk omdat behandeling verlies van het gezichtsvermogen kan voorkomen of terugdraaien. In de Diabetic Retinopathy Study (DRS) ontdekten onderzoekers dat fotocoagulatiechirurgie een effectieve behandeling was voor diabetische retinopathie. De Early Treatment Diabetic Retinopathy studie en DRS toonden aan dat fotocoagulatie het risico op gezichtsverlies verminderde, met het meeste voordeel bij patiënten die een verder gevorderde basislijnziekte hadden.16,17 Huidige gegevens leveren bewijs dat intravitreale antivasculaire endotheliale groeifactor (anti-VEGF) middelen effectiever zijn voor de behandeling van maculair oedeem dan monotherapie of combinatietherapie met lasercoagulatie.8 Bovendien kan anti-VEGF het gezichtsvermogen verbeteren, terwijl fotocoagulatie alleen verder gezichtsverlies voorkomt.18,19 Een nadeel van anti-VEGF is dat het gedurende de eerste 12 maanden maandelijkse intravitreale therapie vereist.
Clinical Pearls
- Er zijn geen specifieke tekenen of symptomen van vroege diabetische retinopathie.
- Screening op diabetische retinopathie dient plaats te vinden bij patiënten:
– met type 1 diabetes vijf jaar na diagnose.
– bij patiënten met type 2 diabetes bij diagnose.
- Counseling en verhoogde onderzoeken moeten worden gegeven aan diabetische vrouwen die van plan zijn zwanger te worden of zwanger zijn, omdat diabetische retinopathie snel kan versnellen tijdens de zwangerschap.
- Nauwgezette glycemische controle en bloeddrukcontrole (< 140 mmHg systolisch) kunnen de ontwikkeling van diabetische retinopathie voorkomen.
- Tot 50% van de patiënten met albuminurie (ongeacht het eGFR-niveau) zal retinopathie hebben.9
- Behandeling met fotocoagulatie kan progressie van de ziekte voorkomen en anti-VEGF behandeling kan gezichtsverlies door macula-oedeem terugdraaien.
Diabetes Kidney Disease
Diabetes kidney disease (DKD), de voorkeursterm van de ADA, is de belangrijkste oorzaak van chronische nierziekte (CKD) in de Verenigde Staten.20,21 DKD heeft aanzienlijke gevolgen op lange termijn voor de levenskwaliteit van patiënten met diabetes en is verantwoordelijk voor tot 40% van de nierziekten in het eindstadium (ESRD).20 Op basis van het Kidney Disease Outcomes Quality Initiative (KDOQI) van de National Kidney Foundation en de ADA 2017 Standards of Care, zal deze paragraaf richtlijnen geven voor streefwaarden voor HbA1c, medicatiebeheer en therapeutische behandeling voor patiënten met DKD.
De KDOQI stratificeert streefwaarden voor HbA1c-niveaus op basis van het risico van de patiënt op hypoglykemie en comorbiditeiten. Dit initiatief is gebaseerd op drie publicaties die aantonen dat glykemische controle met een HbA1c van minder dan 7% de progressie van nierziekte bij patiënten met type 2 diabetes voorkomt of vermindert.22,23,24 Deze studies zijn samengevat in tabel 2. De ADA beveelt aan om bij patiënten met een hoger risico op hypoglykemie het streefwaarde HbA1c boven de 7% te brengen.8 De KDOQI beveelt aan om bij patiënten met CKD stadium 4 en 5 met een beperkte levensverwachting een HbA1c van meer dan 7% aan te houden.25
Tabel 2. Belangrijkste studies die aantonen dat de glycemie onder controle blijft met een A1c lager dan 7% |
|
|
Test |
Resultaten |
|
Actie bij diabetes en vaatziekten: Preterax and Diamicron Modified Release Controlled Evaluation (ADVANCE) Trial22 |
21% reductie nieuwe macroalbuminurie en niervervangende therapie bij A1c lager dan 7% |
|
Veterans Affairs Diabetes Trial (VADT)23 |
37% reductie in macroalbuminurie en 32% reductie in microalbuminurie bij A1c lager dan 7% |
|
De Action to Control Cardiovascular Risk in Diabetes (ACCORD)-studie24 |
2% reductie in macroalbuminurie en 21% reductie in microalbuminurie bij A1c lager dan 7% |
Epidemiologie. Mannen en vrouwen worden in gelijke mate door DKD getroffen.20 De piekincidentie voor het ontwikkelen van DKD ligt 15 jaar na de diagnose.21 Afro-Amerikanen hebben drie tot vijf keer meer kans op het ontwikkelen van diabetische nefropathie dan blanken.20 Mexicaanse Amerikanen en Pima-indianen hebben ook een hoger risico op het ontwikkelen van DKD.20
Proteïnurie is een voorspeller van cardiovasculaire morbiditeit en mortaliteit door alle oorzaken bij diabetes.21 Aanwezigheid van DKD is een factor voor een verhoogd risico op hart- en vaatziekten. Patiënten met DKD hebben consequent te maken met een hogere sterfte aan hart- en vaatziekten.26 Bovendien is de mortaliteit door alle oorzaken hoger bij patiënten met DKD.21
Bij type 1-diabetes beginnen microvasculaire complicaties zoals DKD zich ongeveer 10-20 jaar na de diagnose te ontwikkelen; bij type 2-diabetes is het precieze begin vaak onbekend en is eerdere screening dus gerechtvaardigd.27
Pathofysiologie en pathogenese. Aangenomen wordt dat hyperglykemie drie belangrijke histologische veranderingen in de glomeruli induceert die tot DKD leiden: 1) mesangiale expansie, 2) verdikking van de glomerulaire keldermembraan, en 3) glomerulaire sclerose.28 Hoewel de precieze pathogenese van het ontstaan van DKD onbekend is, wordt aangenomen dat hyperglykemie in eerste instantie hyperfiltratie en nierschade veroorzaakt als gevolg van histologische veranderingen en activering van cytokinen.20 Typisch kan albuminurie het eerste teken van DKD zijn.29
Dit wordt verder verergerd als gevolg van comorbide condities van hyperlipidemie, arteriosclerose, hypertensie, en obesitas, die allemaal bijdragen aan nierschade en daaropvolgende functievermindering. Centrale zwaarlijvigheid leidt tot hypertensie door hyperactivering van het renine-angiotensine-aldosteronsysteem en het sympathische zenuwstelsel.20 Naarmate de niervasculatuur arteriosclerotischer wordt, neemt ook de progressie van diabetische nefropathie toe. Een belangrijk onderscheidend kenmerk van diabetische nefropathie ten opzichte van andere vormen van CKD is dat de glomeruli en nieren aanvankelijk meestal normaal of groter zijn.20
Classificatie. Zowel de eGFR als de aanwezigheid van albuminurie worden gebruikt om CKD te classificeren.30,31 De eGFR is gebaseerd op ras, leeftijd, geslacht, gewicht en serumcreatininespiegels. (Zie tabel 3.) Historisch werd de term microalbuminurie gebruikt om matig verhoogde albumineniveaus aan te duiden. De National Kidney Foundation beveelt nu aan de termen “licht”, “matig” of “ernstig verhoogd” te gebruiken om de albuminurieniveaus te beschrijven, gebaseerd op de niveaus in tabel 4.31 De albumine-creatinineverhouding is de eerste test die wordt gebruikt om albuminurie te detecteren.
Tabel 3. Estimated GFR with Stage and Description |
||
|
Stage |
GFR (mL/min per 1.73 m2) |
Beschrijving |
|
90+ |
Glomerulaire hyperfiltratie |
|
|
Mild verminderde nierfunctie |
||
|
3A |
Matig verminderde nierfunctie |
|
|
3B |
||
|
Zeer verminderde nierfunctie |
||
|
< 15 of aan de dialyse |
Eind-stadium van nierfalen |
|
Tabel 4. Albuminurie-categorieën bij CKD |
||
|
Categorie |
Albuminen-naarCreatininespiegels |
Beschrijving |
|
A1 |
< 30 |
Normaal tot licht verhoogd |
|
A2 |
Zwaar verhoogd |
Zwaar verhoogd |
|
A3 |
> 300 |
Zwaar verhoogd |
De twee classificatieschema’s vertegenwoordigen de tweeledige route naar de ontwikkeling van CKD. Het ene is door verhoging van creatinine en verslechtering van de GFR. De andere is door de ontwikkeling van albuminurie. Toenemende albuminurie wordt vaak gevolgd door een daling van de eGFR;32 dit kan echter worden voorkomen door het gebruik van angiotensine-converting enzyme (ACE)-remmers of angiotensine-receptorblokkers (ARB’s) en glycemische controle. (Zie afbeelding 1.)
Figuur 1. Voorgestelde evaluatiefrequentie (aantal keren per jaar) per eGFR- en albuminuriecategorie
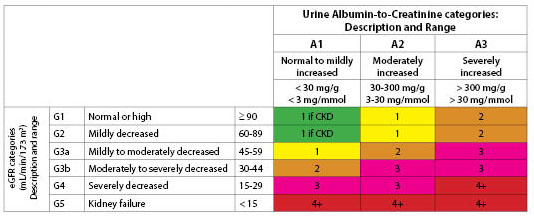
Geprint met toestemming van Kidney Disease: Improving Global Outcomes (KDIGO).
Algemene symptomen. De meeste mensen hebben geen symptomen van diabetische nefropathie. Vaak hebben patiënten wel aanwijzingen voor of een diagnose van andere microvasculaire complicaties.20 Vroege DKD is meestal asymptomatisch. Een late bevinding van DKD is een schuimende urine. Als een patiënt ernstig hypoalbuminemisch is, kan hij of zij zich bovendien presenteren met pedaal oedeem en vermoeidheid.20 Patiënten met DKD hebben meestal systemische hypertensie. Patiënten met diabetische nefropathie hebben meestal ook retinopathie en neuropathie.8
Diagnostische mogelijkheden. Aangezien er geen symptomen zijn, is routinematige screening van cruciaal belang. De ADA beveelt een jaarlijkse screening aan van de verhouding albumine/creatinine in de urine.8 Daarnaast moet ten minste jaarlijks de eGFR worden getest bij patiënten met type 1 diabetes die vijf jaar hebben doorgemaakt en bij alle patiënten met type 2 diabetes of patiënten met comorbide hypertensie en diabetes.8 Er is geen duidelijke aanbeveling voor het verkrijgen van beeldvorming, zoals een echografie, voor de diagnose van DKD.
Differentiële Diagnose. Sommige rode vlaggen kunnen erop wijzen dat diabetes niet de enige oorzaak van CKD is. Als een persoon gevorderde CKD heeft zonder aanwijzingen voor andere microvasculaire complicaties, is dit een waarschuwing. Overdreven proteïnurie met een plotseling begin (minder dan vijf jaar na het begin van diabetes) van urinesediment met dysmorfe rode cellen en afzettingen, of een abrupte daling van de GFR, suggereert een nierziekte van niet-diabetische etiologie.20 Serum- of urine-elektroforese kan worden gedaan als er een vermoeden is van multipel myeloom. De afwezigheid van albuminurie bij een verlaagde eGFR en diabetes vereist onderzoek naar andere oorzaken van CKD dan DKD.21 Tabel 5 geeft een lijst van rode vlaggen die wijzen op een niet-diabetische glomerulaire ziekte.
Tabel 5. Red Flags Suggesting Nondiabetic Glomerular Disease
- Ontstaan van proteïnurie < 5 jaar na het gedocumenteerde begin van type 1 diabetes of acuut begin van nierziekte
- Aute achteruitgang van eGFR; diabetische nefropathie
- Urinesediment met dysmorfe rode cellen of cellulaire afzettingen
- Aanwezigheid van andere microvasculaire complicaties zoals neuropathie of retinopathie
- Tekenen en/of symptomen van een andere systemische aandoening
Behandeling. Een kenmerk van diabetesnefropathie is beheersing van glucose, zoutreductie, bloeddruk en dyslipidemie. Bovendien moeten patiënten nefrotoxische medicatie en supplementen vermijden, zoals aminoglycosiden en niet-steroïdale ontstekingsremmers. Patiënten moeten worden doorverwezen naar een nefroloog in stadium IV nierziekte of als er sprake is van snel afnemende nierfunctie. Andere indicaties voor doorverwijzing zijn afhankelijk van de complexiteit van het geval. Nieuwere orale medicatie voor diabetes kan de progressie van nierfalen helpen voorkomen.
Glykemische controle. Bij patiënten met diabetische nefropathie zijn de keuze van de geneesmiddelen, de controle en de farmacologie van invloed. Naarmate de eGFR van een patiënt afneemt, moet de dosis van sommige orale middelen worden aangepast. Insuline blijft de centrale therapie voor glucosecontrole bij patiënten met diabetes en gevorderde CKD.31 Tabel 6 toont de aanbevolen dosisaanpassingen voor antiglykemische medicatie bij patiënten met nierziekte. In 2016 is aangetoond dat zowel empagliflozin als canagliflozin de progressie van CKD en microalbuminurie vermindert.33,34 Empagliflozin verlaagde de progressie van nefropathie en verlaagde het risico op belangrijke nadelige cardiovasculaire voorvallen in vergelijking met placebo wanneer het werd toegevoegd aan de standaard type 2 diabeteszorg in de baanbrekende Empagliflozin Cardiovascular Outcome Event Trial in Type 2 Diabetes Mellitus Patients (EMPA-REG) uitkomststudie.33
Tabel 6. Dosisaanpassingen en aanbevelingen voor glucoseverlagende middelen bij patiënten met nierinsufficiëntie |
||
|
Glucose-verlagende middelen |
Doseringsaanpassingen bij patiënten met nierinsufficiëntie |
|
Klasse |
Medicatie |
|
|
Biguaniden |
Metformine |
eGFR 30 tot 45 mL/min/1.73 m2: Niet aanbevolen om therapie te starten. Indien na aanvang van de therapie, voordelen/risico’s van voortzetting van de therapie beoordelen. eGFR < 30 mL/min/1,73 m2: Gebruik is gecontra-indiceerd |
|
Sulfonylureas |
Glimepiride |
Mild tot matig gestoorde patiënten: Initieer met 1 mg eenmaal daags Erge stoornis: Gebruik is gecontra-indiceerd |
|
Glipizide |
Extended-release: Initieer met 2,5 mg eenmaal daags |
|
|
Glyburide |
eGFR < 60 mL/min/1,73 m2: Gebruik wordt afgeraden |
|
|
Meglitiniden |
Nateglinide |
Geen doseringsaanpassing noodzakelijk |
|
Repaglinide |
CrCl 20 tot 40 mL/min: Initieer met 0.5 mg bij de maaltijd CrCl < 20 mL/min: Geen informatie |
|
|
Thiazolidinediones |
Pioglitazone |
Geen doseringsaanpassing noodzakelijk |
|
Rosiglitazone |
Geen doseringsaanpassing noodzakelijk |
|
|
α-Glucosidaseremmers |
Acarbose |
SCr > 2.0 mg/dL: gebruik wordt niet aanbevolen |
|
Miglitol |
CrCl < 25 mL/min of SCr >2.0 mg/dL: gebruik wordt afgeraden |
|
|
DPP-4 remmers |
Alogliptine |
CrCl 30 tot 60 mL/min: 12.5 mg eenmaal daags CrCl < 30 mL/min: 6,25 mg eenmaal daags ESRD die hemodialyse vereist: 6.25 mg eenmaal daags en toedienen zonder rekening te houden met tijdstip van hemodialyse |
|
Linagliptine |
Geen doseringsaanpassing nodig |
|
|
Saxagliptine |
CrCl ≤ 50 mL/min: 2,5 mg eenmaal daags |
CrCl ≤ 50 mL/min: 2,5 mg eenmaal daags 30 mL/min: 2,25 mg eenmaal daags RD die hemodialyse behoeven.5 mg eenmaal daags ESRD die hemodialyse vereist: 2.5 mg eenmaal daags en toedienen na hemodialyse |
|
Sitagliptine |
CrCl 30 tot 50 mL/min: 50 mg eenmaal daags CrCl < 30 mL/min: 25 mg eenmaal daags ESRD die hemodialyse of peritoneale dialyse vereist: 25 mg eenmaal daags en toedienen zonder rekening te houden met tijdstip van hemodialyse |
|
|
Vildagliptine |
CrCl < 50 mL/min: 50 mg eenmaal daags |
|
|
Bilezuursequestratiemiddelen |
Colesevelam |
Geen doseringsaanpassingen nodig |
|
Dopamine-2 agonisten |
Bromocriptine |
Geen informatie |
|
SGLT-2 remmers |
Canagliflozin |
eGFR 45 tot 60 mL/min/1.73 m2: Niet meer dan 100 mg eenmaal daags eGFR < 45 mL/min/1,73 m2: Niet aanbevolen om de therapie te starten. Indien na aanvang, de therapie staken bij patiënten met eGFR persistent < 45 mL/minute/1,73 m2. eGFR < 30 mL/min/1,73 m2/ESRD/Hemodialyse: Gebruik is gecontra-indiceerd |
|
Dapagliflozin |
eGFR < 60 mL/min/1,73 m2: Niet aanbevolen om de therapie te starten. Indien na aanvang, de therapie staken bij patiënten met eGFR persistent tussen 30 en < 60 mL/min/1,73 m2. eGFR < 30 mL/min/1,73 m2/ESRD/Hemodialyse: Gebruik is gecontra-indiceerd |
|
|
Empagliflozin |
eGFR < 45 mL/min/1,73 m2: Niet aanbevolen om de therapie te starten. Bij patiënten met eGFR persistent < 45 mL/min/1,73 m2. eGFR < 30 mL/min/1,73 m2. ESRD/ Hemodialyse na aanvang van de behandeling staken: Gebruik is gecontra-indiceerd |
|
|
GLP-1 receptor agonisten |
Albiglutide |
Geen doseringsaanpassing nodig |
|
Dulaglutide |
Geen doseringsaanpassing |
|
|
Exenatide |
CrCl 30 tot 50 mL/min: Geen informatie. Voorzichtig gebruiken. CrCl < 30 mL/min/ ESRD: Gebruik wordt afgeraden |
|
|
Liraglutide |
Geen informatie |
|
|
Lixisenatide |
EGFR 15 tot 29 mL/min/1.73 m2: Geen informatie. Bewaken op verhoogde nadelige GI effecten die kunnen leiden tot dehydratie en verslechtering van de nierfunctie. eGFR <15 mL/min/1.73 m2/ ESRD: Gebruik wordt afgeraden |
|
|
Amylinemimetica |
Pramlintide |
CrCl ≥15 mL/min: Geen aanpassing van de dosering noodzakelijk ESRD: Geen informatie |
|
Insulinen |
Rapid-werkende analogen
Kortwerkende
Tussenwerkende
Intermediate-werkend
Basisinsulineanalogen
|
De insulinebehoefte kan afnemen als gevolg van veranderingen in de klaring of het metabolisme van insuline. Controleer de bloedglucose nauwgezet. |
Bloeddruk. De behandeling van de bloeddruk moet beginnen bij 140/90 mmHg voor patiënten met diabetes en diabetische nierziekte.37 In de United Kingdom Prospective Diabetes Study (UKPDS) werd een vermindering van 12% van het risico op diabetische complicaties gevonden met elke 10 mmHg verlaging van de systolische druk totdat de druk 120 mmHg was.38 De voorkeursmedicatie blijft ACE-remmers of ARB’s voor personen met hypertensie en diabetes, DKD, en CKD. Het is aangetoond dat ACE-remming de ontwikkeling van DKD vertraagt wanneer deze wordt gestart bij patiënten met een licht verhoogde albuminurie. De creatinine kan tot 30% stijgen bij het starten van een ACE-remmer of ARB.39 Overweeg de evaluatie van andere onderliggende nierziekten als de creatinine meer stijgt dan dit.
De KDOQI raadt af ACE/ARB’s te geven aan patiënten met diabetes type 2 die normotensief en normoalbuminurisch zijn.40,41,42 ACE-remmers of ARB’s worden voorgesteld voor diabetespatiënten die normotensief zijn met microalbuminurie.31,37 Er is geen specifieke dosis of titratie voor deze personen. Dubbele blokkade van het renine-angiotensinesysteem door zowel ACE als ARB’s wordt niet aanbevolen vanwege het verhoogde risico op hyperkaliëmie, verminderde nierfunctie en hypotensie.43
Zoutreductie. De 2012 Reduction of Endpoints in Non-insulin-dependent diabetes mellitus with the Angiotensin II Antagonist Losartan (RENAAL) Trial en Irbesartan Diabetic Nephropathy Trial (IDNT) toonden aan dat natriumarme diëten de nefroprotectieve en cardioprotectieve effecten van ARB’s verhoogden bij patiënten met type 2 diabetes en diabetische nefropathie.44,45
Renale Dialyse en Renale Transplantatie. Patiënten met ESRD moeten naar de nefrologie worden doorverwezen. Behandelingsopties omvatten peritoneale dialyse of hemodialyse, niertransport, of de optie om de behandeling te stoppen en palliatieve of hospicezorg te beginnen. Uit één observationele studie bleek dat patiënten die op jongere leeftijd (< 60 jaar) met dialyse begonnen, een slechtere overleving hadden.46
Referral. Figuur 1 bevat indicaties voor verwijzing op basis van GFR- en albuminurieclassificatie. Overweeg andere oorzaken van nierziekte die niet gerelateerd zijn aan diabetes, vooral bij patiënten met type 1 diabetes waarbij het begin van retinopathie niet voorafgaat aan de ontwikkeling van nefropathie.21 Nefrologen kunnen helpen de diagnose te verduidelijken, resistente hypertensie en hyperkaliëmie te controleren en patiënten voor te bereiden op dialyse.8
Er moet ook rekening mee worden gehouden dat de ontwikkeling van nefropathie mogelijk niet gerelateerd is aan de diabetes zelf. Bij patiënten met type 1 diabetes gaat het ontstaan van retinopathie meestal vooraf aan de ontwikkeling van nefropathie.47 Iemand die zich presenteert met nefropathie, maar zonder retinopathie, moet worden onderzocht op andere oorzaken. Verwijzing naar een nefroloog moet plaatsvinden om de oorzaak van nefropathie vast te stellen wanneer deze onzeker is of wanneer er moeilijk te behandelen, DKD-gerelateerde problemen zijn, waaronder anemie, hyperparathyreoïdie en voortschrijdende nierziekte met een eGFR < 30 mL/min/1,73 m2.8 Het hebben van een consulterende nefroloog wanneer zich stadium 4 CKD ontwikkelt (eGFR < 30 mL/min/1,73 m2) wordt geassocieerd met een verminderde morbiditeit, verminderde kosten voor de gezondheidszorg en uitgestelde dialyse.48 Overweeg een verwijzing in stadium 3B om patiënten eerder voor te bereiden en voor nefrologie maximaal medisch te behandelen.
Clinical Pearls
- Jaarlijkse screening op DKD dient plaats te vinden door middel van urinealbumine-onderzoek en een meting van de eGFR.
- Bloeddruk- en glucosecontrole kunnen preventie van nefropathieprogressie bieden. Handhaaf de bloeddruk < 140/90 mmHg bij patiënten met diabetes en CKD. ACE-remmers of ARB’s moeten de behandeling van keuze zijn.
- ACE-remmers en ARB’s mogen niet worden gebruikt om nefropathie te voorkomen als de bloeddruk en eiwituitscheiding normaal zijn. ACE-remmers en ARB’s mogen niet in combinatie worden gebruikt.
- Patiënten met CKD stadia 3-5 hebben een verhoogd risico op hypoglykemie. Voorzichtigheid is geboden met orale middelen zoals sulfonylureum.
- Bij sommige patiënten met CKD is het aangewezen het streefcijfer HbA1c > 7% vast te stellen, vooral wanneer het risico op hypoglykemie groot is.
Diabetische Perifere Neuropathie
Een algemeen aanvaarde definitie van diabetische perifere neuropathie (DPN) in de klinische praktijk is “de aanwezigheid van symptomen en/of tekenen van perifere zenuwstoornissen bij mensen met diabetes na uitsluiting van andere oorzaken.”49 De ADA classificatie van distale symmetrische polyneuropathie is: 1) voornamelijk kleine-vezel neuropathie, 2) voornamelijk grote-vezel neuropathie, en 3) gemengde kleine- en grote-vezel neuropathie (meest voorkomend).
Pathofysiologie en Pathogenese. De ontwikkeling en progressie van DPN komen voort uit de complexe relaties tussen de zenuwen en de hen omringende cellen.50 Zowel vasculaire factoren als metabole interacties dragen bij aan alle stadia van DPN.51 Het algemeen aanvaarde inzicht in menselijke diabetes die leidt tot de ontwikkeling van DPN is de complexe interactie tussen hyperglykemie, de duur van diabetes, leeftijdsgerelateerde neuronale schade, de mate van bloeddruk- en bloedlipidencontrole, en gewicht.52,53,54,55 Hyperglykemie activeert talrijke biochemische routes die de metabolische toestand van een zenuwcel bepalen en in combinatie met een verminderde zenuwperfusie bijdraagt tot de progressie van neuropathieën. Een baanbrekende studie, de DCCT, ondersteunt de betekenis van hyperglykemie in de pathogenese van neuropathie.10,56,57 Een ander hyperglykemie-gerelateerd mechanisme dat leidt tot DPN is hyperglykemie-geïnduceerde oxidatieve en nitrosatieve stress met een toename van de productie van vrije radicalen.58,59
Naast hyperglykemie is onlangs gesuggereerd dat laaggradige ontsteking mogelijk een belangrijke rol speelt in de pathogenese van diabetische neuropathieën, leidend tot tekorten in perifere en autonome zenuwvezels.51,60 De complexe reeks van metabole en vasculaire factoren veroorzaakt de onbalans tussen schade en herstel in zenuwvezels, waarbij vooral distale gevoelsvezels worden aangetast en wordt bijgedragen aan het geleidelijke verlies van gevoel dat de klinische symptomen van diabetische polyneuropathie manifesteert.58,61
Gemeenschappelijke Symptomen. Bij navraag naar de ervaren symptomen van DPN dient men te letten op de plaats (meestal gevoeld in handen en voeten), uitlokkende factoren, kenmerken van de ongemakken, evenals het begin en de frequentie van nachtelijke exacerbatie omdat de symptomen patiëntspecifiek zijn.4 Zowel kleine als grote vezels worden aangetast door verhoogde bloedglucose, en de ervaren symptomen variëren afhankelijk van de klasse van aangetaste sensorische vezels. Wanneer de aangetaste zenuwvezels overwegend klein zijn, zijn de symptomen meestal pijn (stekend, lancerend, prikkend, brandend, pijnlijk, vervelend en overgevoelig), dysesthesieën (onaangenaam gevoel van branden, tintelen, prikkelen en steken) en gevoelloosheid.4
De intensiteit van het ongemak kan variëren van het voelen van kleine abnormale sensaties tot het gehandicapt zijn door de pijn die ’s nachts kan verergeren en de slaap kan verstoren, wat in verband is gebracht met depressie vanwege een perceptie van een verminderde kwaliteit van leven.4
Anderzijds kunnen patiënten, wanneer vooral de grote vezels zijn aangedaan, gevoelloosheid en tintelingen in hun ledematen voelen, onvast lopen en hun evenwicht verliezen (wat kan leiden tot vallen).4 Bij sommige patiënten kunnen de symptomen verergeren naarmate hun bloedglucosespiegel daalt als gevolg van intensiever therapeutisch beheer van diabetes. Patiënten kunnen asymptomatisch zijn, maar in verschillende mate sensorisch verlies hebben; een ongewenst gevolg van ernstig sensorisch verlies ten gevolge van diabetische neuropathie kan pijnloos letsel zijn, wat leidt tot een verhoogd risico op voetulceratie of, in ernstige gevallen, amputatie.62
De meest voorkomende vorm van diabetische perifere neuropathie is distale symmetrische polyneuropathie met een progressief verlies van sensorische zenuwvezels.4 Het typische “kous”-patroon ontstaat bilateraal door de beschadigingen die optreden op de meest distale delen van de langste zenuwen (die het eerst worden aangetast).63,64,65 Naarmate de tijd vordert, ontstaat een “kous-handschoen”-patroon, dat sensorisch verlies en de typische symptomen van DNP bevordert, door proximaal voortschrijdende zenuwafwijkingen.4
Clinische diagnose. Een klinische diagnose van DPN kan worden gesteld op basis van neuropathische tekenen en symptomen van een patiënt met diabetes na uitsluiting van andere oorzaken van neuropathie.66 Asymptomatische diabetische perifere neuropathie kan voorkomen bij tot 50% van degenen die deze complicatie hebben; daarom is implementatie van preventieve voetzorg essentieel, vooral voor degenen die een hoog risico lopen op blessures als gevolg van gevoelloze voeten.4 Jaarlijkse screening op DPN moet worden uitgevoerd bij alle patiënten met diabetes door middel van speldenprikken, temperatuur, trillingswaarneming (met behulp van een 128-Hz stemvork), 10-g monofilament druksensatie, en enkel diepe peesreflexen; potentiële voetulcera kunnen worden voorspeld door een verlies van 10-g monofilament sensatie (verlies van beschermende sensatie) en een verminderde waarneming van trillingen.63 De Standards of Medical Care in Diabetes-2017 van de ADA blijven een jaarlijkse 10-g monofilamenttest aanbevelen om patiënten te identificeren die risico lopen op het ontwikkelen van ulceratie en amputatie.8 Bovendien bevelen de 2017 ADA-richtlijnen screening op DPN aan bij de diagnose van diabetes type 2 en vijf jaar na de diagnose van diabetes type 1.8
In 2009 heeft het Toronto Consensus Panel on Diabetic Neuropathies de diagnostische criteria geactualiseerd om diagnostische categorieën te bieden. Daarnaast kunnen verschillende goed gevalideerde screeningsinstrumenten door zorgverleners worden meegenomen in het diagnoseproces, waaronder het Michigan Neuropathy Screening Instrument (MNSI), de Toronto Clinical Neuropathy Score, en de Utah Neuropathy Scale. In tabel 7 worden andere oorzaken van neuropathie beschreven die moeten worden uitgesloten.
Tabel 7. Andere oorzaken van neuropathie67
- Alcohol of andere toxinen
- Neurotoxische medicatie, vooral chemotherapie
- Vitamine B12-deficiëntie
- Hypothyreoïdie
- Renale aandoening
- Maligniteiten (multipel myeloom, bronchogeen carcinoom)
- Humaan immunodeficiëntievirus (HIV)
- Chronische inflammatoire demyeliniserende neuropathie, erfelijke neuropathieën, en vasculitis
Diagnostische onderzoeken. Er bestaan verschillende diagnostische tests om de aanwezigheid van DPN te bevestigen. Zenuwgeleidingsonderzoek wordt al jaren beschouwd als de gouden standaard diagnostische test voor DPN vanwege de objectieve metingen zonder reacties van patiënten, wat leidt tot een hoge betrouwbaarheid.4 Kwantitatieve sensorische tests evalueren het vermogen van patiënten om lichte aanraking, vibratie en temperatuurdiscriminatie te detecteren, wat een zekere mate van subjectiviteit met zich meebrengt.4 Andere methoden, waaronder huidbiopsie en intra-epidermale zenuwvezeldichtheid en corneale confocale microscopie, worden niet routinematig gebruikt in de klinische praktijk, maar kunnen worden gebruikt in klinische trials.4
Behandelingsopties: Farmacologische behandeling. De farmacologische behandeling van DPN is voor symptomatische verbetering, dus de gebruikte medicijnen zijn niet bedoeld om progressie te voorkomen. Tabel 8 geeft een overzicht van de geneesmiddelen uit de drie meest gebruikte klassen (anticonvulsiva, antidepressiva en opioïden) om de neuropathische symptomen onder controle te houden. Hoewel verschillende middelen vaak worden gebruikt als eerste benadering voor de behandeling van DPN, zijn alleen pregabaline en duloxetine door de FDA goedgekeurd voor de behandeling van deze aandoening; daarom wordt elk van deze middelen aanbevolen als eerste keuze voor symptomatische neuropathische pijn.4 Gabapentine, hoewel niet door de FDA goedgekeurd voor gebruik bij de behandeling van DPN, wordt vaak gebruikt als eerste benadering, die een vergelijkbare werkzaamheid heeft als de door de FDA goedgekeurde middelen. Tricyclische antidepressiva (bijv. amitriptyline) – niet door de FDA goedgekeurde middelen tegen DPN – zijn effectief bij de behandeling van DPN, maar moeten met voorzichtigheid worden gebruikt vanwege een hoger risico op bijwerkingen.
Tabel 8. Tabel 8. Vaak gebruikte farmacologische middelen voor DPN4,69 |
|||||
|
Farmaceutisch middel (NNT range 30-50% verbetering*) |
Maximale dagelijkse dosis voor DNP (mg/dag) |
Gemeenschappelijke bijwerkingen |
Aanpassing van de dosis nodig? |
Contra-indicaties |
Overwegingen bij het voorschrijven |
|
Anticonvulsiva
|
|||||
|
Pregabalin (3.3-8,3) |
Duizeligheid Somnolentie Gewichtstoename Perifeer oedeem Wazig zicht Constipatie |
Renaal: Ja Hepatisch: Nee |
Hypersensitiviteit voor pregabaline |
Sterk bewijs; goedgekeurd door FDA; gereguleerde stof |
|
|
Gabapentine (3.3-7.2) |
3,600 |
Duizeligheid Ataxie Somnolentie Hoofdpijn Nausea Diarree Wichtstoename |
Renal: Ja Hepatic: Nee |
Hypersensitiviteit voor gabapentine |
Matig bewijs; niet goedgekeurd door FDA |
|
Antidepressiva
|
|||||
|
Amitriptyline (2.1-4.2) |
Zware sedatie; verwardheid; anticholinerge effecten (constipatie, wazig zien) |
Renal: Nee Hepatic: Nee Lagere doses worden aanbevolen voor oudere patiënten |
Hypersensitiviteit voor amitriptyline; gelijktijdige toediening met of binnen 14 dagen van MAO’s; gelijktijdige toediening met cisapride; acute herstelfase na myocardinfarct |
Matig bewijs; niet goedgekeurd door de FDA; voorzichtig gebruiken bij personen met een voorgeschiedenis van hart- en vaatziekten |
|
|
Duloxetine (3..8-11) |
(V.S.) |
Nausea; sedatie; gegeneraliseerde slaperigheid |
Renaal: Ja Hepatisch: Vermijd gebruik bij leverfunctiestoornis |
Hypersensitiviteit; gelijktijdige toediening met of binnen 14 dagen na MAO’s; inleiden bij personen die linezolid of IV methyleenblauw krijgen |
Matig bewijs; Door FDA goedgekeurd; kan worden toegevoegd aan pregabaline of gabapentine |
|
Venlafaxine (5.2-8.4) |
Nausea; sedatie; gegeneraliseerde slaperigheid |
Renaal: Ja Hepatisch: Ja |
zwak bewijs; niet goedgekeurd door FDA; kan worden toegevoegd aan gabapentin |
||
|
Opioïden
|
|||||
|
Tramadol (2..1-6.4) |
Somnolentie Nausea Overgeven Constipatie Licht gevoel in het hoofd Duizeligheid Hoofdpijn |
Renaal: Ja Hepatic: Nee |
Hypersensitiviteit voor tramadol, opioïden of een bestanddeel van de formulering; ER formulering: significante ademhalingsdepressie en acute of ernstige astma; IR formulering: acute intoxicatie met alcohol, hypnotica, narcotica, centraal werkende analgetica, opioïden, of psychotrope drugs |
Laag potentieel voor misbruik (Schedule IV gecontroleerde substantie); niet aanbevolen voor gebruik als eerstelijns- of tweedelijnsmiddel |
|
|
Tapentadol (N/A) |
Immediate-release: Extended-release: |
Somnolentie Nausea Overgeven Constipatie Duizeligheid |
Renale: Gebruik niet aanbevolen wanneer Hepatic: Geen |
overgevoeligheid voor tapentadol; significante ademhalingsdepressie; acute of ernstige astma; paralytische ileus; binnen 14 dagen na gebruik van MAO-remmers |
Goedgekeurd door de FDA; op lijst II geplaatste gereguleerde stof; niet aanbevolen voor gebruik als eerstelijns- of tweedelijnsmiddel |
|
De informatie heeft betrekking op farmaceutische middelen die zijn verkregen uit de respectieve bijsluiters (waarnaar wordt verwezen met handelsnamen) |
|||||
De richtlijn van de American Academy of Neurology (AAN) beveelt de volgende topische middelen aan: capsaïcine en isosorbidedinitraat spray (matig bewijs) en Lidoderm patch (zwak bewijs).69 Oxcarbazepine, lamotrigine, lacosamide, clonidine, pentoxifylline, en mexiletine worden in de AAN-richtlijn niet aanbevolen bij de behandeling van DPN.69
Daarnaast zijn opioïden door sommigen aanbevolen voor gebruik bij refractaire DPN. De opioïden die door de AAN-richtlijn worden aanbevolen zijn dextromethorfan (400 mg/dag), morfinesulfaat (getitreerd tot 120 mg/dag), en oxycodon (gemiddeld 37 mg/dag, max 120 mg/dag); er zijn echter onvoldoende gegevens om te suggereren het ene middel boven het andere te gebruiken.69 De auteurs van dit artikel bevelen aan om opioïden alleen te gebruiken in ernstige refractaire gevallen met nauwgezette monitoring van patiënten die echte functionele verbetering krijgen van opioïden. De auteurs volgen de 2016 position statement van de Centers for Disease Control and Prevention dat opioïden beperkt langetermijngebruik hebben bij niet-kanker type pijn.70
Een van de uitdagingen in de farmacologische behandeling van DPN is onvoldoende head-to-head studies waarin kwaliteit-van-leven uitkomsten zijn opgenomen.4 In een recente studie waarin een acht weken durende therapie tussen hooggedoseerde pregabaline, hooggedoseerde duloxetine, of in een combinatie werd vergeleken, werden geen significante verschillen gevonden in gemiddelde pijnverandering tussen monotherapie en combinatietherapie.71 Er zijn meer studies nodig waarin twee werkzame stoffen worden vergeleken om inzicht te verschaffen in het verbeteren van de zorg voor mensen die lijden aan diabetische perifere neuropathie.
Niet-farmacologische behandeling. Procedures. De ANN-richtlijn suggereert om percutane elektrische zenuwstimulatie gedurende drie tot vier weken te overwegen voor de behandeling van DPN.69 Een pilot, twee-staps acupunctuur, gerandomiseerde, gecontroleerde trial72 en een single-blind, placebo-gecontroleerde, gerandomiseerde trial73 waarin de effectiviteit van acupunctuur bij DPN werd geëvalueerd, toonden beide verbeteringen aan in uitkomstmaten die geassocieerd worden met pijn. Verdere studies zijn echter nodig om de rol van acupunctuur bij de behandeling van DPN te bevestigen.
Alfa-liponzuur. Er zijn aanwijzingen dat het gebruik van het antioxidant alfa-liponzuur zou kunnen helpen bij het verminderen van vrije radicaal-gemedieerde oxidatieve stress en de volgende voordelen zou kunnen bieden: het aanpakken van de pathogenese, het vertragen van de ontwikkeling, en het verbeteren van de symptomen van DPN.74,75
Preventie. Van modificaties van de levensstijl, gericht op gezonde voeding en lichamelijke activiteit, is voortdurend aangetoond dat ze de prevalentie van diabetes en de complicaties ervan, waaronder diabetische perifere neuropathie, verminderen.68 Intensieve glykemische controle blijkt het risico op diabetische neuropathie bij patiënten met diabetes te helpen verlagen door de zenuwfunctie te verbeteren.61,76,77 De DCCT heeft de rol van glykemische controle bij het voorkomen en stoppen van de progressie van diabetische neuropathie bij type 1 diabetes vastgesteld.10,56
Clinical Pearls
- Tot 50% van de patiënten kan pijnloze of asymptomatische perifere neuropathie hebben.
- Patiënten met neuropathie wordt aanbevolen om voetverzorgingseducatie te krijgen (dagelijkse zelfinspectie van de voeten) en regelmatige podotherapeutische zorg voor geselecteerde patiënten.
- Patiënten met DPN die tekenen vertonen van verlies van beschermend gevoel met of zonder misvorming moet worden geadviseerd om elke drie tot zes maanden een arts te raadplegen voor preventieve maatregelen.64
- Om de symptomen van DPN effectief te behandelen, wordt een multidisciplinaire aanpak essentieel; deze uitgebreide aanpak kan farmacologische, psychologische en/of fysische therapie omvatten.
- Een nieuwe standpuntverklaring over diabetische neuropathie gepubliceerd door de ADA beveelt screening op DPN aan bij patiënten met prediabetes die symptomen van perifere neuropathie vertonen.4
- Specialistische zorg is nodig voor mensen met perifere aandoeningen, niet-zintuiglijke neuropathie, of Charcot-voet.
Gastroparese
Een andere vorm van diabetesneuropathie is gastroparese. Deze aandoening gaat gepaard met symptomen van het bovenste deel van het maagdarmkanaal, zoals misselijkheid, braken, vroegtijdige verzadiging of postprandiale volheid, buikpijn en een opgeblazen gevoel, maar zonder obstructie van de afvoer. Hoewel er een aantal oorzaken van gastroparese zijn, wordt geschat dat diabetes verantwoordelijk is voor ongeveer een derde van alle gevallen.78
Pathofysiologie. Voorgestelde pathofysiologische mechanismen voor diabetische gastroparese zijn onder andere verminderde glycemische controle, vagale of prevertebrale sympathische ganglia neuropathie, afwijkingen van interstitiële cellen van Cajal, verlies van stikstofmonoxide synthase, en, mogelijk, myopathie.79,80
Klinische presentatie. In een vroeg stadium van deze aandoening zijn de patiënten meestal asymptomatisch. Er is geen lineair verband tussen de symptomen en de ernst van de neuropathie. De grote verscheidenheid aan symptomen maakt het moeilijk de diagnose te stellen. Andere klinische presentaties zijn anorexia, ondervoeding, gewichtsverlies, en hypoglykemie als gevolg van het niet op elkaar aansluiten van de absorptie van voedsel en insuline. Pijn wordt misschien niet zo vaak gemeld, maar is voor veel mensen wel belangrijk. In een door de NIH gefinancierd consortium had 72% van de patiënten met gastroparese buikpijn.81 Bij 18% van deze patiënten was dit het dominante symptoom. Pijn werd geïnduceerd door eten (72%), was nachtelijk (74%), en interfereerde met de slaap (66%) voor deze patiënten.81
Hoe vaak komt diabetes gastroparese voor? De cumulatieve 10-jaars incidentie van gastroparese is geschat op 5,2% bij type 1 diabetes en 1% bij type 2 diabetes onder patiënten met diabetes in de gemeenschap.82 Andere studies hebben percentages tussen 5-12% gevonden.83,84 De percentages zijn echter veel hoger wanneer de diagnose wordt gebaseerd op symptomen in plaats van op het maagledigingsonderzoek.
Gastroparese komt vaker voor bij type 1 diabetes dan bij type 2 diabetes, en het wordt het meest gezien nadat de persoon al meer dan 10 jaar diabetes heeft en de andere microvasculaire complicaties van retinopathie, nefropathie, en perifere neuropathie heeft ontwikkeld. Als een patiënt zich eerder dan verwacht presenteert met gastroparese, moeten andere etiologieën worden onderzocht, meestal perioperatieve vagale zenuwbeschadiging of farmacologische effecten van incretine-gebaseerde middelen – glucagon-like peptide-1 receptor agonisten (GLP-1RA) en dipeptidyl-peptidase 4 remmers (DPP-4 remmers).
Als een patiënt eenmaal symptomen van gastroparese ontwikkelt, blijven de symptomen meestal bestaan en zijn stabiel gedurende 12-25 jaar. Dit geldt zelfs als er een verbeterde glucosecontrole is,85 behalve in het geval van een pancreas- en niertransplantatie.86 Hoewel er geen duidelijk bewijs is dat gastroparese zelf de mortaliteit verhoogt, vermindert het wel aanzienlijk alle aspecten van de kwaliteit van leven.87
Diagnostiek. Een aantal testen kan helpen bij de diagnose. De gouden standaard voor deze diagnose is gastro-oesofageale scintigrafie. Deze is niet-invasief, test de fysiologie, en geeft kwantitatieve resultaten. Gastroparese kan worden gediagnosticeerd als er tenminste 35% retentie is van een standaard vetarme maaltijd vier uur na inname.80
Om de meest accurate testresultaten te verkrijgen, moet het pre-test protocol het staken van alle motiliteitsveranderende medicatie omvatten gedurende tenminste twee tot drie dagen voor de test, inclusief prokinetica, opiaten, en anticholinergica. Incretine middelen, zoals GLP-1 agonisten en DPP-4 remmers, moeten ook worden gestaakt, omdat bekend is dat zij de maaglediging vertragen. Van hyperglykemie is ook aangetoond dat het de maaglediging vertraagt, en de glucose moet lager zijn dan 275 mg/dL voordat met het onderzoek wordt begonnen.79,88
Patiënten moeten zich onthouden van roken en het nuttigen van alcohol op de testdag, omdat beide de maaglediging kunnen vertragen.89 Bovendien kunnen GLP-1RAs gastroparese verergeren omdat ze de maaglediging vertragen. Verder kunnen sommige mensen subklinische gastroparese hebben die aan het licht komt wanneer een GLP-1RA wordt gestart.
Behandeling. De behandeling van gastroparese hangt grotendeels af van de ernst van de symptomen. De algemene principes voor behandeling omvatten ondersteunende behandelingen (vloeistoffen, elektrolyten, glucose controle, en voeding), medische behandelingen (prokinetica, anti-emetica, en pijnstilling), en invasieve behandelingen (chirurgie, Botox injecties, maag pacing, of elektrische stimulatie).79
Ondersteunende behandeling wordt meestal gestart in het ziekenhuis en is gericht op normalisatie van vloeistof, elektrolyten, en voedingsstoornissen. Bij het geven van voedingsondersteuning wordt de voorkeur gegeven aan enterale voeding boven parenterale voeding, omdat dit fysiologisch beter is en kan helpen de darmflora in stand te houden. Verder kunnen dieetveranderingen zeer nuttig zijn bij gastroparese. Vezelarme, vetarme diëten met weinig reststoffen worden aanbevolen voor patiënten met gastroparese.85 Vezelrijke diëten kunnen de symptomen doen toenemen, omdat ze meer vertering vereisen.
Medicatie. Prokinetica: In de Verenigde Staten zijn metoclopramide en erythromycine de meest gebruikte medicatie om gastroparese te behandelen. Echter, metoclopramide heeft een black box waarschuwing vanwege het risico op tardieve dyskinesie. De ontwikkeling van deze aandoening is direct gerelateerd aan de duur van het gebruik van metoclopramide en het aantal ingenomen doses. Bij gebruik van deze medicatie is het het beste om het alleen te gebruiken bij symptomatische patiënten en te beginnen met de laagste effectieve dosis 15 minuten voor de maaltijd. Drug holidays kunnen soms helpen om de duur van de effecten te verlengen.90
Domperidon is een meer selectieve dopamine-agonist die even effectief is als metoclopramide, maar minder bijwerkingen van het centrale zenuwstelsel heeft.91
Antiemetica: Antiemetica kunnen worden gebruikt om de symptomen te helpen verlichten. Het risico op medicatie-interacties is echter aanzienlijk en moet zorgvuldig in de gaten worden gehouden.
Pijnbestrijding kan een uitdaging zijn bij patiënten met gastroparese. Tricyclische antidepressiva worden vaak gebruikt als eerstelijns therapie voor pijn bij gastroparese. Tweedelijns benaderingen zijn de zwakke mu-opioid receptor agonist, tramadol, die ook serotonine vrijgeeft en de heropname van noradrenaline remt, en het gamma-aminoboterzuur analoog, gabapentine. Het gebruik van narcotica bij gastroparese wordt echter niet aanbevolen, omdat het kan bijdragen aan constipatie en verergering van de symptomen.
Invasieve behandelingen: Botox injecties worden vaak gebruikt bij de behandeling van gastroparese, maar het gebruik ervan wordt niet ondersteund in klinische studies.92,93
Het gastrische elektrische stimulatie apparaat werd in 2000 door de FDA goedgekeurd onder een humanitarian device exemption.94 Het gastrische elektrische stimulatie apparaat levert hoogfrequente, laag-energetische elektrische stimulatie aan de maag. Het is nuttiger bij diabetische gastroparese dan bij idiopathische gastroparese. Een meta-analyse toonde aanzienlijke voordelen voor de symptomen van patiënten. Het exacte mechanisme van het voordeel is nog steeds niet bekend.95 Er wordt verondersteld dat elektrische stimulatie van de maag leidt tot veranderingen in de centrale mechanismen die misselijkheid en braken controleren, de vagale functie verhoogt, en resulteert in verminderde gevoeligheid voor distensie.97 Patiënten die goed reageren, reageren meestal snel. Dit heeft sommigen ertoe gebracht om eerst een proef met tijdelijke plaatsing van elektroden aan te bevelen alvorens deze op lange termijn toe te passen.
Clinical Pearls
- Diabetische gastroparese komt vaker voor bij mensen met langdurige diabetes en bij mensen met andere microvasculaire complicaties.
- De gouden standaard diagnose voor gastroparese is gastro-oesofageale scintigrafie.
- Vezelarme, vetarme, vetarme diëten worden aanbevolen bij diabetische gastroparese.
- Farmacologische en interventionele behandelingen hebben beperkte voordelen en aanzienlijke risico’s op lange termijn.
Diabetische Cheiroarthropathie
Een van de minder bekende diabetescomplicaties is cheiroarthropathie. Deze aandoening wordt gekenmerkt door een beperkte beweeglijkheid van de gewrichten als gevolg van verdikking van de huid bij mensen met langdurige diabetes. Het was waarschijnlijk de eerste complicatie die bij type 1 diabetes werd vastgesteld. De prevalentie varieert sterk van 8-50%.98
Cheiroarthropathie wordt vermoedelijk veroorzaakt door de glycosylering en cross-linking van collageen. Het kan de huid en pezen aantasten, en kan resulteren in beperkte gewrichtsmobiliteit, meestal extensie van de vingers, stijfheid, en pijn. Het klassieke lichamelijke onderzoeksteken voor diabetische cheiropathie is het “gebedsteken”. Bij deze aandoening is iemand niet in staat zijn of haar handen volledig plat te leggen om te “bidden”, waardoor er een ruimte tussen de vingers van de linker- en rechterhand ontstaat. Er zijn aanwijzingen dat degenen die cheiropathie ontwikkelen een drie keer groter risico op microvasculaire complicaties hebben.99
Diabetische cheiropathie is meestal erger bij mensen met langdurige of slecht gecontroleerde glycemie. Gelukkig ervaren veel mensen verlichting van de symptomen en verbeterde mobiliteit wanneer de glucosecontrole verbetert.100
Conclusie
Het beheer van diabetescomplicaties vereist een multidisciplinair team. Vroegtijdige screening van retinopathie, nefropathie en neuropathie is essentieel, gezien de asymptomatische aard van de ziekte. Het kenmerk van diabetes management voor alle complicaties blijft glycemische en bloeddruk controle.
- American Diabetes Association. Kosten van diabetes. Beschikbaar op: http://www.diabetes.org/advocacy/news-events/cost-of-diabetes.html?referrer=https://www.google.com/. Bijgewerkt op 22 juni 2015. Accessed Feb. 8, 2017.
- UK Prospective Diabetes Study Group. Intensieve bloedglucoseregeling met sulfonylureum of insuline vergeleken met conventionele behandeling en risico op complicaties bij patiënten met type 2 diabetes. Lancet 1998;352:837-853.
- Gregg EW, Yanfed L, Wang J. Changes in diabetes-related complications in the United States, 1990-2010. N Engl J Med 2014;370:1514-1523.
- Pop-Busui R, Boulton A, Feldman E, et al. Diabetes neuropathy: Een standpuntverklaring van de American Diabetes Association. Diabetes Care 2017;40:136-154.
- Leasher JL, Bourne RR, Flaxman SR, et al. Wereldwijde schattingen over het aantal mensen dat blind of slechtziend is door diabetische retinopathie: Een meta-analyse van 1990 tot 2010. Diabetes Care 2016;39:1643-1649.
- National Eye Institute. Feiten over diabetische oogziekte. Beschikbaar op: https://nei.nih.gov/health/diabetic/retinopathy. Bijgewerkt sept. 2015. Accessed Feb. 8, 2017.
- Fong, DS, Aiello L, Gardner TW, et al. Retinopathie bij diabetes. Diabetes Care 2004;27(Suppl 1):S84-S87.
- American Diabetes Association. Standaarden voor medische zorg bij diabetes-2017. Diabetes Care 2017;40:(Suppl 1):S4-S5.
- Doggen K, Nobels F, Scheen AJ, et al. Cardiovasculaire risicofactoren en complicaties geassocieerd met albuminurie en verminderde nierfunctie bij met insuline behandelde diabetes. J Diabetes Complications 2013;27:370-375.
- The Diabetes Control and Complications Trial Research Group. Het effect van intensieve behandeling van diabetes op de ontwikkeling en progressie van complicaties op lange termijn bij insuline-afhankelijke diabetes mellitus. N Engl J Med 1993;329:977-986.
- Action to Control Cardiovascular Risk in Diabetes Follow-On (ACCORDION) Eye Study Group en de Action to Control Cardiovascular Risk in Diabetes Follow-On (ACCORDION) Study Group. Persistent effects of intensive glycemic control on retinopathy in type 2 diabetes in the Action to Control Cardiovascular Risk in Diabetes (ACCORD) follow-on study. Diabetes Care 2016;39:1089-1100.
- ACCORD Study Group, ACCORD Eye Study Group, Chew EY, et al. Effecten van medische therapieën op de progressie van retinopathie bij type 2 diabetes. N Engl J Med 2010;363:233-244.
- Chew EY, Davis MD, Danis RP, et al. The effects of medical management on the progression of diabetic retinopathy in persons with type 2 diabetes: The Action to Control Cardiovascular Risk in Diabetes (ACCORD) Eye Study. Ophthalmology 2014;121:2443-2451.
- Diabetes Control and Complications Trial Research Group. Effect van zwangerschap op microvasculaire complicaties in de Diabetes Control and Complications Trial. Diabetes Care 2000;23:1084-1091.
- Colberg SR, Sigal RJ, Yardley JE, et al. Physical activity/exercise and diabetes: Een standpuntverklaring van de American Diabetes Association. Diabetes Care 2016;39:2065-2079.
- The Diabetic Retinopathy Study Research Group. Voorlopig rapport over effecten van fotocoagulatietherapie. Am J Ophthalmol 1976;81:383-396.
- Early Treatment Diabetic Retinopathy Study Research Group. Fotocoagulatie voor diabetisch maculair oedeem: Early Treatment Diabetic Retinopathy Study report number 1. Arch Ophthalmol 1985;103:1796-1806.
- Nguyen QD, Brown DM, Marcus DM, et al. Ranibizumab for diabetic macular edema: Resultaten van 2 fase III gerandomiseerde trials: RISE en RIDE. Ophthalmology 2012;119:789-801.
- Wong TY, Cheung CMG, Larsen M, et al. Diabetic retinopathy. Nat Rev Disease Prim doi:10.1038/nrdp.2016.12; published online March 17, 2016.
- Batuman V, Soman AS, Schmidt RJ, Soman SS. Diabetes nefropathie. Medscape Beschikbaar op: http://emedicine.medscape.com/article/238946-overview. Bijgewerkt op 30 sept. 2016. Accessed Feb. 12, 2017.
- Tuttle KR, Bakris GL, Bilous RW, et al. Diabetic kidney disease: Een verslag van een ADA-consensusconferentie. Diabetes Care 2014;37:2864-2883. https://doi.org/10.2337/dc14-1296
- Patel A, MacMahon S, Chalmers J, et al. Intensive blood glucose control and vascular outcomes in patients with type 2 diabetes. N Engl J Med 2008;358:2560-2572.
- Duckworth W, Abraira C, Moritz T, et al. Glucosecontrole en vasculaire complicaties bij veteranen met type 2 diabetes. N Engl J Med 2009;360:129-139.
- Ismail-Beigi F, Craven T, Banerji MA, et al. Effect van intensieve behandeling van hyperglykemie op microvasculaire uitkomsten bij type 2-diabetes: Een analyse van de ACCORD gerandomiseerde trial. Lancet 2010;376:419-430.
- National Kidney Foundation. KDOQI klinische praktijkrichtlijn voor diabetes en CKD: 2012 update. Am J Kidney Dis 2012;60:850-886.
- Fox CS, Matsushita K, Woodward M, et al. Chronic Kidney Disease Prognosis Consortium. Associations of kidney disease measures with mortality and end-stage renal disease in individuals with and without diabetes: Een meta-analyse. Lancet 2012;380:1662-1673.
- Hahr AJ, Molitch ME. Management van diabetes mellitus bij patiënten met een chronische nierziekte. Clin Diabetes Endocrinol 2015. doi: 10.1186/s40842-015-0001-9.
- Alsaad KO, Herzenberg AM. Distinguishing diabetic nephropathy from other casues of glomerulosclerosis: An update. J Clin Pathol 2007;60:18-26.
- Narva AS, Bilous RW. Laboratoriumbeoordeling van diabetische nierziekte. Diabetes Spectr 2015;28:162-166.
- Levey AS, Stevens LA, Schmid CH, et al. A new equation to estimate glomerular filtration rate. Ann Intern Med 2009;150:604-612.
- National Kidney Foundation. KDOQI richtlijnen voor de klinische praktijk voor chronische nierziekte: Evaluatie, classificatie en stratificatie. Am J Kidney Dis 2002;39(2 Suppl 1):S1-S266.
- de Boer IH, Rue TC, Cleary PA, et al. Lange-termijn nieruitkomsten van patiënten met type 1 diabetes mellitus en microalbuminurie: Een analyse van het Diabetes Control and Complications Trial/Epidemiology of Diabetes Interventions and Complications cohort. Arch Intern Med 2011;171:412-420.
- Wanner C, Inzucchi SE, Lachin JM, et al. Empagliflozin and progression of kidney disease in type 2 diabetes. N Engl J Med 2016;375:323-334.
- Heerspink HJL, Desai M, Jardine M, et al. Canagliflozin vertraagt progressie van nierfunctieafname onafhankelijk van glycemische effecten. J Am Soc Nephrol 2016;28:1-8.
- Lexi-Drugs. Lexicomp. Wolters Kluwer Health, Inc. Riverwoods, IL. Beschikbaar op: http://online.lexi.com. Accessed Oct. 31, 2016.
- Micromedex Solutions. Truven Health Analytics, Inc. Ann Arbor, MI. Beschikbaar op: http://www.micromedexsolutions.com. Accessed Oct. 31, 2016.
- James PA, Oparil S, Carter BL, et al. 2014 evidence-based guideline for the management of high blood pressure in adults. JAMA 2014;311:507-520.
- King P, Peacock I, Donnelly R. The United Kingdom Prospective Diabetes Study (UKPDS): Klinische en therapeutische implicaties voor type 2 diabetes. Br J Clin Pharmacol 1999;48:643-648.
- Jackevicius CA, Wong J, Aroustamian I, et al. Rates and predictors of ACE inhibitor discontinuation subsequent to elevated serum creatinine: Een retrospectieve cohortstudie. BMJ Open 2014;4:e005181.
- Mauer M, Zinman B, Gardiner R, et al. Renale en retinale effecten van enalapril en losartan bij type 1 diabetes. N Engl J Med 2009;361:40-51.
- Bilous R, Chaturvedi N, Sjølie AK, et al. Effect van candesartan op microalbuminurie en albumine-excretiesnelheid bij diabetes: Drie gerandomiseerde onderzoeken. Ann Intern Med 2009;151:11-20.
- Haller H, Ito S, Izzo JL Jr, et al. Olmesartan for the delay or prevention of microalbuminuria in type 2 diabetes. N Engl J Med 2011;364:907-917.
- Makani H, Bangalore S, Desouza KA, et al. Efficacy and safety of dual blockade of the renin-angiotensin system: Meta-analyse van gerandomiseerde trials. BMJ 2013;346:f360.
- Miao Y, Ottenbros SA, Laverman GD, et al. Effect van een verlaging van het urinezuur op de nieruitkomsten tijdens de behandeling met losartan: A post-hoc analysis of the reduction of endpoints in non-insulin-dependent diabetes mellitus with the Angiotensin II Antagonist Losartan Trial. Hypertension 2011;58:2-7.
- Lewis EJ, Hunsicker LG, Clarke WR, et al. Renoprotective effect of the angiotensin-receptor antagonist irbesartan in patients with nephropathy due to type 2 diabetes. N Eng J Med 2001;354:851-860.
- Adler A, Casula A, Steenkamp R, et al. Associatie tussen glycemie en mortaliteit bij diabetische personen op niervervangingstherapie in het V.K. Diabetes Care 2014;37:1304-1311.
- Sharma SG, Bomback AS, Radhakrishnan J, et al. Het moderne spectrum van nierbiopsiebevindingen bij patiënten met diabetes. Clin J Am Soc Nephrol 2013;8:1718-1724.
- Smart NA, Dieberg G, Ladhani M, Titus T. Early referral to specialist nephrology services for preventing the progression to end-stage kidney disease. Cochrane Database Syst Rev 2014;6:CD007333.
- Boulton AJM, Gries FA, Jervell JA. Richtlijnen voor de diagnose en poliklinische behandeling diabetische perifere neuropathie. Diabet Med 1998;15:508-514.
- O’Brien PD, Hinder LM, Sakowski SA, Feldman EL. ER stress in diabetische perifere neuropathie: Een nieuw therapeutisch doelwit. Antioxid Redox Signal 2014;21:621-633.
- Cameron NE, Cotter MA. Pro-inflammatoire mechanismen in diabetische neuropathie: Focus op de nucleaire factor kappa B pathway. Curr Drug Targets 2008;9:60-67.
- Tesfaye S, Chaturvedi N, Eaton SE, et al. Vascular risk factors and diabetic neuropathy. N Engl J Med 2005;352:341-350.
- Wiggin TD, Sullivan KA, Pop-Busui R, et al. Verhoogde triglyceriden gecorreleerd met progressie van diabetische neuropathie. Diabetes 2009;58:1634-1640.
- Stella P, Ellis D, Maser RE, Orchard TJ. Cardiovasculaire autonome neuropathie (expiratie en inspiratie ratio) in type 1 diabetes. Incidentie en voorspellers. J Diabetes Complications 2000;14:1-6.
- Witten DR, Tesfaye S, Chaturvedi N, et al. Risicofactoren voor cardiale autonome neuropathie bij type 1 diabetes mellitus. Diabetologia 2005;48:164-171.
- Diabetes Control and Complication Trial (DCCT) Research Group. Effect of intensive diabetes treatment on nerve conduction in the Diabetes Control and Complications Trial. Ann Neurol 1995;38:869-880.
- Diabetes Control and Complication Trial (DCCT) Research Group. The effect of intensive diabetes therapy on measures of autonomic nervous system function in the Diabetes Control and Complications Trial (DCCT). Diabetologia 1998;41:416-423.
- Edwards JL, Vincent AM, Cheng HT, Feldman EL. Diabetische neuropathie: Mechanismen tot beheer. Pharmacol Ther 2008;120:1-34.
- Vincent AM, Callaghan BC, Smith AL, Feldman EL. Diabetische neuropathie: Cellulaire mechanismen een therapeutisch doelwit. Nat Rev Neurol 2011;7:573-583.
- Kellogg AP, Wiggin T, Larkin D, et al. Protective effects of cyclooxygenase-2 gene inactivation against peripheral nerve dysfunction and intraepidermal nerve fibers loss in experimental diabetes. Diabetes 2007;56:2997-3005.
- Callaghan BC, Cheng HT, Stables CL, et al. Diabetische neuropathie: Klinische manifestaties en huidige behandelingen. Lancet Neurol 2012;11:521-534.
- Boulton AJM, Kirsner RS, Vileikyte L. Klinische praktijk: Neuropathische diabetische voetulcera. N Eng J Med 2004;351:48-55.
- Boulton AJM, Vinik AI, Arezzo JC, et al. Diabetic neuropathies: Een verklaring van de American Diabetes Association. Diabetes Care 2005;28:956-962.
- Boulton AJM, Armstrong DG, Albert SF, et al. Comprehensive foot examination and risk assessment: A report of the task force of the foot care interest group of the American Diabetes Association, with endorsement by the American Association of Clinical Endocrinologists. Diabetes Care 2008;31:1679-1685.
- Tesfaye S, Boulton AJ, Dyck PJ, et al. Diabetic neuropathies: Update on definitions, diagnostic criteria, estimation of severity, and treatments. Diabetes Care 2010;33:2285-2293.
- Dyke PJ, Albers JW, Andersen H, et al. Diabetic polyneuropathies: Update on research definition, diagnostic criteria and estimation of severity. Diabetes Metab Res Rev 2011;27:620-628.
- Freeman R. Niet alle neuropathie is diabetes is van diabetische etiologie: Differentiële diagnose van diabetische neuropathie. Curr Diabe Rep 2009;9:423-431.
- Balducci S, Iacobellis G, Parisi L, et al. Oefentraining kan de natuurlijke geschiedenis van diabetische perifere neuropathie wijzigen. J Diabetes Complications 2006;20:216-223.
- Bril V, England J, Franklin GM, et al. Evidence-based guideline: Behandeling van pijnlijke diabetische neuropathie. Rapport van de American Academy of Neurology, de American Association of Neuromuscular and Electrodiagnostic Medicine, en de American Academy of Physical Medicine and Rehabilitation. Neurology 2011;76:1758-1765.
- Dowell D, Haegerich TM, Chou R. CDC Guideline for prescribing opioids for chronic pain – United States 2016. MMWR Recomm Rep 2016;65:1-49.
- Tesfaye S, Wilhelm S, Lledo A, et al. Duloxetine en pregabaline: Hoge-dosis monotherapie of hun combinatie? De “COMBO-DN studie” – een multinationale, gerandomiseerde, dubbelblinde, parallelle groep studie bij patiënten met diabetische perifere neuropathische pijn. Pain 2013;154:2616-2625.
- Ahn AC, Bennani T, Freeman R, et al. Two styles of acupuncture for treating painful diabetic neuropathy – a pilot randomized control trial. Acupunct Med 2007;25:11-17.
- Garrow A, Xing M, Vere J, et al. Role of acupuncture in the management of diabetic painful neuropathy (DPN): Een pilot RCT. Acupunct Med 2014;32:242-249.
- Ziegler D, Nowak H, Kempler P, et al. Behandeling van symptomatische diabetische polyneuropathie met het antioxidant alfa-liponzuur: Een meta-analyse. Diabet Med 2004;21:114-121.
- Ziegler D, Low PA, Litchy WJ, et al. Efficacy and safety of antioxidant treatment with alpha-lipoic acid over 4 years in diabetic polyneuropathy: The NATHAN 1 trial. Diabetes Care 2011;34:2054-2060.
- Kuwabara S, Ogawara K, Harrori T, et al. The acute effects of glycemic control on axonal excitability in human diabetic nerves. Intern Med 2002;41:360-365.
- Peltier A, Goutman SA, Callaghan BC. Pijnlijke diabetische neuropathie. BMJ 2014;348:g1799.
- Soykan I, Sivri B, Sarosiek I, et al. Demografie, klinische kenmerken, psychologische en misbruikprofielen, behandeling, en lange termijn follow-up van patiënten met gastroparese. Dig Dis Sci 1998;43:2398-2404.
- Camilleri M, Bharucha AE, Farrugia G. Epidemiology, mechanisms, and management of diabetic gastroparesis. Clin Gastroenterol Hepatol 2011;9:5-12.
- Shin AS, Camilleri M. Diagnostische beoordeling van diabetische gastroparese. Diabetes 2013;62:2667-2673.
- Hasler WL, Wilson L, Parkman HP, Lee L. Importance of abdominal pain as a symptom in gastroparesis: Relation to clinical factors, disease severity, quality of life, gastric retention, and medication use. Gastroenterology 2010;138. doi: 10.1016/S0016-5085(10)62131-2.
- Choung RS, Locke GR 3rd, Schleck CD, et al. Risk of gastroparesis in subjects with type 1 and 2 diabetes in the general population. Am J Gastroenterol 2012;107:82-88.
- Maleki D, Locke GR III, Camilleri M, et al. Gastro-intestinal tract symptoms among persons with diabetes mellitus in the community. Arch Intern Med 2000;160:2808-2816.
- Bytzer P, Talley NJ, Leemon M, et al. Prevalentie van gastro-intestinale symptomen geassocieerd met diabetes mellitus: Een bevolkingsonderzoek onder 15.000 volwassenen. Arch Intern Med 2001;161:1989-1996.
- Jones KL, Russo A, Berry MK, et al. A longitudinal study of gastric emptying and upper gastrointestinal symptoms in patients with diabetes mellitus. Am J Med 2002;113:449-455.
- Gaber AO, Hathaway DK, Abell T, et al. Improved autonomic and gastric function in pancreas-kidney vs kidney-alone transplantation contributes to quality of life. Transplant Proc 1994;26:515-516.
- Punkkinen J, Färkkilä M, Mätzke S, et al. Upper abdominal symptoms in patients with Type 1 diabetes: Unrelated to impairment in gastric emptying caused by autonomic neuropathy. Diabet Med 2008;25:570-577.
- Schvarcz E, Palmer M, Aman J, et al. Physiological hyperglycemia slow gastric emptying in normal subjects and patients with insulin-dependent diabetes mellitus. Gastroenterology 1997;113:60-66.
- Miller G, Palmer KR, Smith B, et al. Smoking delays gastric emptying of solids. Gut 1989;30:50-53.
- Rao AS, Camilleri M. Review article: Metoclopramide en tardieve dyskinesie. Aliment Pharmacol Ther 2010;31:11-19.
- Patterson D, Abell T, Rothstein R, et al. A double-blind multicenter comparison of domperidone and metoclopramide in the treatment of diabetic patients with symptoms of gastroparesis. Am J Gastroenterol 1999;94:1230-1234.
- Arts J, Holvoet L, Caenepeel P, et al. Clinical trial: Een gerandomiseerd-gecontroleerde cross-over studie van intrapylorische injectie van botulinum toxine bij gastroparese. Aliment Pharmacol Ther 2007;26:1251-1258.
- Friedenberg FK, Palit A, Parkman HP, et al. Botulinum toxin A for the treatment of delayed gastric emptying. Am J Gastroenterol 2008;103:416-423.
- Humanitarian Device Exemption for Enterra Device. Fed Reg 2000;65:78495-78496.
- O’Grady G, Egbuji JU, Du P, et al. High-frequency gastric electrical stimulation for the treatment of gastroparesis: Een meta-analyse. World J Surg 2009;33:1693-1701.
- Reddymasu SC, Sarosiek I, McCallum RW. Ernstige gastroparese: Medische therapie of elektrische stimulatie van de maag. Clin Gastroenterol Hepatol 2010;8:117-124.
- McCallum RW, Dusing RW, Sarosiek I, et al. Mechanismen van symptomatische verbetering na elektrische stimulatie van de maag bij gastroparese patiënten. Neurogastroenterol Motil 2010;22:161-167.
- Douloumpakas I, Pyrpasopoulou A, Triantafyllou A, et al. Prevalentie van musculoskeletale aandoeningen bij patiënten met type 2 diabetes mellitus: Een pilootstudie. Hippokratia 2007;11:216-218.
- Rosenbloom AL, Silverstein JH, Lezotte DC. Limited joint mobility in childhood diabetes mellitus indicates increased risk for microvascular disease. N Engl J Med 1981;305;191-194.
- Lister DM, Graham-Brown RAC, Burden AC. Resolutie van diabetische cheiroarthropathie. Br Med J 1986;293:1537.