Een isobarisch proces is een thermodynamisch proces verandering in de toestand van een bepaalde hoeveelheid materie waarbij de druk constant blijft. Wat kan veranderen is een of meer van de toestandsvariabelen. Als er warmte aan het systeem wordt overgedragen, wordt er arbeid verricht en verandert ook de inwendige energie van het systeem.
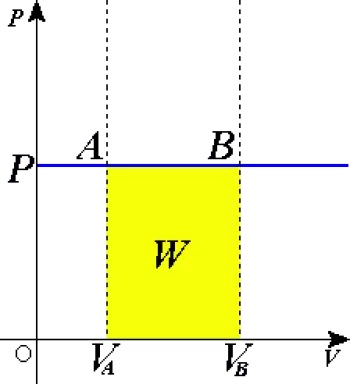
In een druk-volumediagram drijft het een horizontale lijn volgens de ideale gaswet.
Het isobarische proces wordt beheerst door de wet van Charles. Volgens de wet van Charles is voor een vaste massa ideaal gas bij constante druk het volume recht evenredig met de Kelvintemperatuur.
Isobarische processen worden geregeld door de eerste wet van de thermodynamica. Bij deze processen is de toename van de energie gelijk aan de toename van de enthalpie min de druk vermenigvuldigd met de toename van het volume:ΔE = ΔH – P – ΔV.
Niet te verwarren met isothermische processen, die bij constante druk worden uitgevoerd, of met adiabatische processen, waarbij geen warmte wordt uitgewisseld. Bij deze processen kan een drukverandering optreden. Wanneer het proces in een constant volume wordt uitgevoerd, wordt het een isochorisch proces genoemd.
Isobarisch proces Voorbeelden
Om dit thermodynamisch proces beter te begrijpen, helpt het ons een paar voorbeelden te zien.
-
Expansiefase van de cilinder van een motor.
-
Kook water in een open vat.
-
Verwarming van een aardbol onder invloed van zonnestraling.
-
Heteluchtballonnen experiment isobarisch en isochronisch proces.
Verwarming van de lucht van een ballon
De volumeverandering die een ballon ondergaat als de zonnestralen erop schijnen, is een voorbeeld van een isobarisch proces. Terwijl de zon de temperatuur verhoogt, ondergaat het volume van het gas (de lucht) een isobare expansie.
Aan het begin van de ochtend vertoont het een bepaalde druk, volume en temperatuur; naarmate de lucht binnenin opwarmt, neemt de druk toe, maar deze varieert niet door de toename van het volume.
Cilinderuitzettingsfase van een warmtemotor
De cilinder in een warmtemotor kan afhankelijk van de fase van de cyclus worden uit- of samengedreven. De expansie van lucht in een cilinder met een beweegbare zuiger waaraan warmte wordt toegevoerd, geschiedt door een isobarisch proces. Op dezelfde wijze wordt tijdens de compressie het volume isobarisch verkleind.
Het volume zal toenemen in verhouding tot de temperatuur en de druk zal constant blijven. Dit is in overeenstemming met de wet van Charles.
Koken van water in een open vat
Een alledaags voorbeeld van een isobarisch proces is het koken van water in een open vat. Door warmte-energie aan het water toe te voeren, stijgt de temperatuur en wordt het stoom.
De verkregen stoom heeft een hogere temperatuur en neemt een groter volume in, maar de druk blijft constant. Vanaf het begin is de druk gelijk aan de atmosferische druk.
Het verwarmen van een heteluchtballon
Een heteluchtballon is een voorbeeld van het isobarische proces.
Heteluchtballonnen werken omdat hete lucht opstijgt. Door de lucht binnenin de ballon met de brander te verhitten, wordt deze lichter dan de koelere lucht aan de buitenkant. Hierdoor gaat de ballon omhoog zweven, alsof hij zich in water bevindt.
De druk binnenin de ballon is dezelfde als de atmosferische druk. Als de piloot warmte in de lucht injecteert, stijgt de temperatuur. Hierdoor neemt de dichtheid van de lucht af en door het verschil tussen zijn dichtheid en die van de lucht, gaat de ballon omhoog.
Thermodynamisch wordt een deel van de warmte omgezet in arbeid waardoor de heteluchtballon omhoog gaat. Een deel van deze warmte komt buiten het systeem terecht door thermodynamisch contact van de buitenlucht en door het verlies van warme lucht bij het uitzetten.
W 1-2 = P ( V 2 – V 1 ) W 1-2 = n R ( T 2 – T 1 ) Q 1-2 = m c p ( T 2 – T 1 ) Q 1-2 = ( k / ( k -1)) P ( V 2 – V 1 )
Waar,
-
W 1-2 de hoeveelheid arbeid verricht door de verandering van de toestand
-
Q 1-2 de hoeveelheid toegevoerde of afgevoerde warmte
-
P de druk
-
V het volume
-
T de absolute temperatuur
-
n de hoeveelheid stof (gewoonlijk uitgedrukt in mol)
-
m de massa van de stof
-
cp de soortelijke warmte van de stof bij constante druk
-
k is een verhouding die gelijk is aan het quotiënt van de soortelijke warmte bij constante druk en constant volume, respectievelijk
Uit de eerste vergelijking kunnen we afleiden dat als het systeem uitzet (ΔV is positief), het systeem positieve arbeid verricht. Is daarentegen de volumetoename negatief, dan krimpt het systeem en is de arbeid negatief.
Toestandsvergelijking van een ideaal gas
De toestandsvergelijking van een ideaal gas (soms de Mendelejev – Clapeyron-vergelijking of de Clapeyron-vergelijking) is een formule die het verband legt tussen druk, molair volume en de absolute temperatuur van een ideaal gas. De vergelijking luidt:
pV = nRT
Waar,
p – druk,
V- gasvolume,
n- de hoeveelheid gas,
R – universele gasconstante , R ≈ 8,314 J / (mol⋅K),
T – thermodynamische temperatuur, K kelvin.