Introduktion
Tethered cord syndrome (TCS) är en neurologisk utvecklingsstörning som orsakas av en onormalt låg conus medullaris. Det uppträder vanligtvis i barndomen, men kan kvarstå oupptäckt fram till vuxen ålder och kan vara förknippat med ett intraduralt lipom. Patienter med samtidig abnormitet (t.ex. myelomeningocele) och tydliga kliniska symtom (t.ex. progressiv bensvaghet, urininkontinens) kan kräva kirurgisk behandling. Målet med operationen är att avbinda ryggmärgen för att lindra ryggmärgssträckningen. Indikationerna för kirurgi är dock fortfarande kontroversiella (1).
Däremot är den spinal durala arteriovenösa fisteln (SDAVF) ett förvärvat tillstånd. Det är den vanligaste kärlmissbildningen i ryggraden hos vuxna. Den bildas i neuralforamen genom en onormal, direkt förbindelse mellan duralartären (som försörjer duralrotshylsan och den intilliggande spinal dura) och den medullära venen (som dränerar det koronala venösa plexus) (2, 3).
Den kan visa sig med ryggsmärta och progressivt neurologiskt underskott. En SDAVF kräver vanligtvis antingen kirurgisk eller endovaskulär behandling.
Det är mycket sällsynt att TCS, lipom (eller lipomyelomeningocele) och en SDAVF på sakralnivå sammanfaller. I detta meddelande rapporterar vi två sådana patienter. (4-6).
Fallmaterial
Fall 1
En 30-årig kvinna presenterades med en 10-årig historia av smärta i lumbosakrala ryggraden; hon hade haft tillfällig strålning till båda nedre extremiteterna. Efter sin första förlossning fick hon ont i ryggen. MRT visade på en tethered cord på L4-nivå och ett filum terminale lipom. MRT:n visade också på slingrande vener på ryggmärgsytan (figur 1C). Nio år senare, under den andra graviditeten, noterade hon svaghet och känselförlust, obalans med urin- och avföringsinkontinens. Vid intagningen hade hon bilateral svaghet i plantarflexion (grad 4 enligt det modifierade systemet från Medical Research Council) och nedsatt känsel i glutealregionerna och benen samt plantarrespons. Babinski- och Rossolimo-tecken fanns bilateralt. En upprepad MRT visade intraspinala T2 hyperintensiva förändringar i den thorakala ryggraden och conus (figurerna 1A, B, D). Dessa förändringar stämde överens med neurologiskt underskott och efter uteslutning av inflammatoriska demyeliniserande sjukdomar, baserat på en MRT av hjärnan och ett antikroppstest för aquaporin-4, ställdes diagnosen myelopati. På grund av beskrivna plågsamma vener på ryggmärgsytan (figur 1B) genomgick patienten spinal digital subtraktionsangiografi (DSA). DSA-området var från Th6-nivån till den coccygeala artären. Resultaten visade inte på någon vaskulär missbildning. Den preliminära diagnosen var därför symtomatisk TCS och filum terminale lipom. Med tanke på svaghet och neurologiskt underskott planerades kirurgisk ryggmärgsavsättning utan lipomresektion.
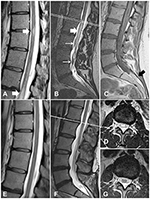
Figur 1. MR-bilder av ryggmärgen i fall 1, före och efter behandling. (A) Myelopatiska förändringar i den thorakala ryggmärgen (vita pilar). (B) Myelopatiska förändringar i conus medullaris (tjock pil) och förtjockade torturkärl (tunna pilar). (C) T1WI-sekvens visar ett filum terminale lipom (svart pil). (D) Ett tvärsnitt på L1/L2-nivå visar myelopatiska förändringar. (E-G) Uppföljningsbilder visar att de myelopatiska förändringarna är upplösta och att de förtjockade venerna har försvunnit.
Sakralkanalen öppnades med ett mediansnitt. Dura var tunn och genomskinlig. Efter en dura- och arachnoidincision i medellinjen visualiserades en tumör som föreföll vara ett lipom. Den uppslukade filum terminale och spinalnerverötterna kaudalt, till S2-nivån. S1- och S2-nervrötterna var placerade lateralt om tumören. Ett förtjockat, slingrande, ljusrött kärl noterades också på filum terminale, som löpte i kranial riktning. Den yttre ytan av dura undersöktes bilateralt på sakrala nivån för att söka efter en SDAVF. En tydligt synlig nidus identifierades vid S3-nivån på vänster sida. Ett empiriskt test utfördes för att stödja detta fynd. Ett klipp placerades på den arterialiserade venen, intraduralt, under några minuter. Därefter ändrade kärlet på filum terminale tydligt färg, från klarrött till blågrått, och dess spänning minskade. SDAVF kopplades sedan bort intraduralt och nidus koagulerades extraduralt. Dessutom skars filum terminale av och prover av lipom togs för histologi. Dura suturerades vattentätt och såret stängdes i lager.
Det postoperativa förloppet var händelselöst. Några dagar senare skrevs patienten ut. En uppföljande MRT visade att de myelopatiska förändringarna hade upphört (figurerna 1E-G). Vid 1-årsuppföljningen hade patienten förbättrats avsevärt, utan inkontinens eller motoriskt underskott.
Fall 2
En 33-årig man presenterade sig med en tvåårig historia av smärta i lumbosakrala ryggraden med progressiv svaghet i nedre extremiteterna, urinfrekvens och inkontinens. Symtomen intensifierades efter träning och långvarigt stående. MRT av ländryggen visade att det fanns ett band vid L3-nivån, ett filum terminale lipom och ödem i ryggmärgen. Den visade också på slingrande vener på ryggmärgens bakre yta (figurerna 2A, D).
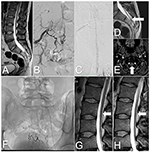
Figur 2. Bilder av ryggmärgen i fall 2, före och efter behandling. (A) T2-viktad MRT: Tethered cord och sakrala lipom. (B) DSA: SDAVF på S2-S3-nivå som försörjs av de laterala sakrala artärerna. (C) DSA: Skruvade vener på den bakre ytan av den cervikala ryggmärgen. (D) T2-viktad MRT: Vener på den bakre ytan av den fasthållna ryggmärgen (pil). (E) TOF MRI: Dränerande ven (pil) vid den atlanto-occipitala korsningen. (F) Röntgen av det sakrala området visar emboliska medel efter tre emboliseringar. (G) Lumbal T2-viktad MRT: Efter den sista emboliseringen syns slingrande kärl på ryggmärgens bakre yta (pil). (H) Uppföljande MRT: 6 månader efter operationen syns inte längre de tortuösa kärlen på ryggmärgens bakre yta (pil).
Den neurologiska undersökningen avslöjade bilateral höftledsböjningssvaghet (grad 4 enligt det modifierade Medical Research Council-systemet), plantarböjningssvaghet (grad 3 enligt det modifierade Medical Research Council-systemet) och nedsatt känsel i S2-S3-dermatomen. Babinski- och Rossolimo-tecken fanns bilateralt. På grundval av de kliniska och radiologiska tecknen misstänktes en SDAVF. En DSA bekräftade SDAVF på S2-S3-nivå, i dura som försörjs av laterala sakrala artärer och grenar från de inre iliakala artärerna. Skruvade dränerande vener fanns på den bakre ytan av hela ryggmärgen och slutade intrakraniellt (figurerna 2B, C, E).
Patienten genomgick tre endovaskulära emboliseringar, var och en med ett annat medel. Först utfördes embolisering med Onyx™ 18 som administrerades i två mikrokatetrar. Denna behandling resulterade i en ocklusion av fisteln. Patienten förbättrades avsevärt, men på grund av dålig penetration av den dränerande venen rekanaliserades fisteln efter några veckor och symtomen återkom.
En andra embolisering utfördes 4 månader senare. Den vaskulära åtkomsten till fisteln var mer komplicerad. En 25-procentig Phil™-injektion var genomförbar endast genom de små sakrala grenarna av den vänstra inre artären iliacus interna. Med detta förfarande uppnåddes en betydande minskning av flödet genom fisteln. Arton månader senare försökte man embolisera fisteln med utspätt lim. Trots god ocklusion av fisteln som observerades i en DSA, förblev de slingrande kärlen synliga i den uppföljande MRT:n (figurerna 2F,G). Symtomen kvarstod och patienten var kvalificerad för kirurgisk behandling.
Målet med operationen var att ockludera den dränerande venen och den arteriella tillförseln och att reducera lipomet. Med ett mediansnitt öppnades sacralkanalen på höger sida. Duran var tjock och det fanns flera kärl som var fyllda med emboliska medel. Det fanns ett stort, ljusrött kärl extraduralt och ett intraduralt vid S2-S3-nivån. En klämma placerades på den arterialiserade venen intraduralt i ett par minuter. Därefter bytte kärlet färg och spänningen minskade. Både intra- och extradurala kärl koagulerades. Därefter visualiserades lipomet och avlägsnades delvis. Dura suturerades vattentätt och såret stängdes i lager.
Det postoperativa förloppet var händelselöst och några dagar senare skrevs patienten ut. Efter 6 månader visade en uppföljande MRT att det inte fanns några snirkliga kärl på ryggmärgens bakre yta och att de myelopatiska förändringarna hade minskat betydligt (figur 2H). Vid uppföljningen förbättrades patienten avsevärt, utan inkontinens, med viss urinfrekvens och lätt svaghet (grad 4 enligt det modifierade systemet från Medical Research Council).
Diskussion
Den samtidiga förekomsten av TCS, ett intraduralt lipom och en SDAVF på sakrala nivån, även om den är exceptionell, bör hållas i minnet, mot bakgrund av det ökande antalet rapporterade fall. Denna studie beskrev det femte och sjätte sådana fallet, med ett TCS och en SDAVF på sakralnivå (tabell 1). Nyligen listades ett av dessa fall av Horiuchi et al. och ytterligare två tillkom av Talenti et al. (6, 8).

Tabell 1. Litteraturöversikt om sammanträffande av sakral dural arteriovenös fistel (DAVF), tethered cord syndrome (TCS) och filum terminale lipom/lipomyelomeningocele.
Årsaken till detta tredubbla sammanträffande är gåtfull. Å ena sidan tros SDAVF vara en förvärvad enhet, till skillnad från primära spinalanomalier. Denna egenskap föreslog att samexistensen av dessa patologier kunde vara oavsiktlig. Å andra sidan har både lipom och angiom ett mesenkymalt ursprung. Tidigare rapporter om kombinerade intramedullära AVM och lipom tyder på att det kan finnas ett samband mellan dessa etiologier (9, 10). Såvitt vi vet har dock inga tidigare studier beskrivit samexistensen av dysrafiska anomalier och en SDAVF på sakrala nivån, som presenterades i barndomen. En sökning i databasen Medline visade inte heller på någon rapport om en medfödd SDAVF. Flera rapporter har dock beskrivit en SDAVF sekundärt till följd av antingen kirurgi eller trauma (11-15). Teoretiskt sett skulle därför en tidigare operation av en myelomeningocele senare kunna utlösa bildandet av en SDAVF.
I tidigare studier har det rapporterats att en venös sinustrombos med tillhörande intravenös hypertoni och en venös utflödesobstruktion skulle kunna initiera bildandet av shuntar (16-18). Därför kan en alternativ förklaring till den samtidiga förekomsten av störningar som hittades i våra fall ha varit att ett lipom orsakade tryck, vilket blockerade det venösa utflödet och därmed främjade bildandet av en SDAVF. Denna alternativa mekanism skulle vara orelaterad till en tidigare historia av trauma eller kirurgi.
Förvärvade SDAVF är vanligtvis lokaliserade i thorakolumbala regionen, och medelåldern vid presentationen är cirka 60 år (19). Sacrala SDAVFs är sällsynta, och medelåldern vid presentation av SDAVFs som förekommer tillsammans med ett TCS är 41 år (tabell 1). Därför är det också möjligt att en medfödd anomali, t.ex. ett intraduralt lipom, kan främja bildandet av en SDAVF vid yngre ålder. Nyligen beskrev Horiuchi et al. två fall och granskade nio tidigare publicerade fall av SDAVF och AVM som samexisterade med spinal lipom av olika typer och på olika spinalnivåer (8). Både Djindjian et al. och Horiuchi et al. postulerade att den mest sannolika mekanismen bakom en fördröjd SDAVF-bildning kan vara adipocyternas frisättning av angiogena faktorer; dessa faktorer kan påverka angiogenesen (20) och leda till lokal hypervaskularisering (5, 8). Dessutom har Jellema et al. uteslutit protrombotiska faktorer i patogenesen för SDAVF (21).
Det symptomatiska sammanträffandet av TCS, sakrala lipom och SDAVF ger upphov till frågan: Vad är det exakt som driver symtomen? Talenti et al. beskrev nyligen diagnostiska och terapeutiska svårigheter för två liknande fall (6). Hos båda dessa patienter resulterade inte en initial avtätering av ryggmärgen och avlägsnande av lipomet/lipomyelomeningocele i vare sig förbättring eller försämring. Efter spinal angiografi tog man därefter itu med den spinala vaskulära patologin. Naturhistorien för filum terminale lipom är godartad; endast 5 % av patienterna uppvisar TCS-symptom (22). Därför var lipomet den minst sannolika orsaken till den neurologiska försämringen. Icke desto mindre kan i viss utsträckning både TCS och SDAVF orsaka liknande symtom. Ett TCS blir symptomatiskt oftare hos barn än hos vuxna (23). Däremot utvecklas funktionsnedsättningar i samband med SDAVF hos äldre och medelålders personer. Dessutom inducerar sakrala SDAVF hyperintensiviteter i ryggmärgen, som är synliga på T2-viktad MRT, och som vanligtvis försvinner efter framgångsrik behandling (24). Den mest sannolika orsaken till neurologisk försämring är därför SDAVF, baserat på medelåldern hos patienter med sammanfallande TCS, sakrala lipom och SDAVF (se tabell 1) och baserat på det goda postoperativa utfallet; dvs. upplösningen av de intramedullära förändringarna, som visades i MRT. Dessutom kan SDAVF-symptomen, till skillnad från TCS, förvärras vid fysisk ansträngning och vid ökande intraabdominellt tryck, vilket var fallet i båda de fall som beskrevs i den aktuella studien.
I patienter med detta tredubbla sammanträffande var SDAVF alltid den direkta orsaken till ökande symtom. Därför bör huvudmålet för behandlingen vara ocklusion. I litteraturen verkade endovaskulär embolisering vara lika effektiv som kirurgi, och embolisering var den enda behandlingen i liknande fall (24). Tyvärr var embolisering antingen ogenomförbar eller ineffektiv i våra fall. Med kirurgi kunde både SDAVF och TCS utforskas och behandlas i ett och samma ingrepp.
I vårt första fall var det initiala målet för kirurgin att avtäta ryggmärgen, eftersom SDAVF inte bekräftades på en preoperativ DSA. Frågan kvarstår dock, varför var SDAVF dold på DSA? Oldfield et al. beskrev tre fall av SDAVF som inte upptäcktes i en DSA, men som var mycket misstänkta utifrån andra neuroimagingmodaliteter. Dessa SDAVVF:er kopplades framgångsrikt bort under operationen (25). De faktorer som hindrade spinal DSA-detektion var bland annat fetma, aortaaneurysm, aortaatroskleros med tortuositet och orifestation eller tortuositet i de lumbala artärerna. I vårt fall kan en möjlig förklaring till de falskt negativa DSA-resultaten vara att DSA:n inte var tillräckligt noggrann, vilket innebär att vi inte undersökte inflödet på den sakrala nivån.
De två fall som beskrivs här visade att sakrala SDAVF:er kan vara svåra att upptäcka i DSA:er och svåra att ockludera med endovaskulär embolisering. Tidigare studier som presenteras i tabell 1 beskriver också misslyckade emboliseringar vid behandling av SDAVFs (4, 6, 8). Totalt har det förekommit 5 misslyckade försök till endovaskulär ocklusion i 3 av 6 rapporterade fall (tabell 1). Således drog vi slutsatsen att ett kirurgiskt tillvägagångssätt kan vara överlägset endovaskulär embolisering, eftersom kirurgi erbjuder en behandling i ett steg.
Slutsatser
Den samtidiga förekomsten av TCS, lipom och SDAVF på sakral nivå är exceptionellt sällsynt. Tidigare rapporter och våra resultat avslöjar att kirurgi kan vara överlägsen endovaskulär embolisering vid behandling av sakrala SDAVF med samexisterande entiteter, eftersom kirurgi erbjuder en behandling i ett steg. Ett växande antal rapporterade fall har indikerat att symtomen på denna trippelstörning kan orsakas enbart av SDAVF och inte av TCS eller lipom, som är tydligt synliga i neuroimaging.
Samtycke
Ett skriftligt informerat samtycke inhämtades från deltagarna för publicering av denna fallrapport.
Författarbidrag
PK utformade projektet och granskade det kritiskt. ŁP förberedde manuskriptet, samlade in och granskade data. PJ, MZ och MG samlade in falldata. BC granskade anatomin. AM gjorde det slutliga godkännandet av den version som ska publiceras.
Intressekonfliktförklaring
Författarna förklarar att forskningen utfördes i avsaknad av kommersiella eller ekonomiska relationer som skulle kunna uppfattas som en potentiell intressekonflikt.
1. Drake JM. Kirurgisk behandling av den fastbundna ryggmärgen – att gå den hårda linjen. Neurosurg Focus. (2007) 23:E4. doi: 10.3171/FOC-07/08/E4
PubMed Abstract | CrossRef Full Text
2. McCutcheon IE, Doppman JL, Oldfield EH. Microvascular anatomy of dural arteriovenous abnormalities of the spine: a microangiographic study. J Neurosurg. (1996) 84:215-20. doi: 10.3171/jns.1996.84.2.0215
PubMed Abstract | CrossRef Full Text | Google Scholar
3. Gailloud P. Spinal dural arteriovenous fistula (SDAVF) variant med dubbelt perimedullärt och epiduralt dränage. Eur Spine J. (2017). 27(Suppl 3):375-9. doi: 10.1007/s00586-017-5298-x
PubMed Abstract | CrossRef Full Text | Google Scholar
4. Krisht KM, Karsy M, Ray WZ, Dailey AT. Extraspinal typ I dural arteriovenös fistel med en lumbosakral lipomyelomeningocele: en fallrapport och litteraturgenomgång. Case Rep Neurol Med. (2015) 2015:526321. doi: 10.1155/2015/526321
PubMed Abstract | CrossRef Full Text | Google Scholar
5. Djindjian M, Ayache P, Brugieres P, Poirier J. Sacral lipom i filum terminale med dural arteriovenös fistel. Fallbeskrivning. J Neurosurg. (1989) 71(5 Pt 1):768-71. doi: 10.3171/jns.1989.71.5.0768
PubMed Abstract | CrossRef Full Text | Google Scholar
6. Talenti G, Vitale G, Cester G, Della Puppa A, Faggin R, Causin F. Sällsynt samband mellan spinal durala arteriovenösa fistlar och dysrafier: rapport om två fall och genomgång av litteraturen med fokus på fallgropar vid diagnos och behandling. Intervent Neuroradiol. (2017) 23:458-64. doi: 10.1177/1591019917714636
PubMed Abstract | CrossRef Full Text | Google Scholar
7. Przepiórka Ł, Kunert P, Juszynńska P, Zawadzki M, Ciszek B, Głowacki M, et al. Coincidence of tethered cord, filum terminale lipoma, and sacral dural arteriovenous fistula: report of two cases and a literature review. Front Neurol. (2018) 9:807. doi: 10.3389/fneur.2018.00807
CrossRef Full Text | Google Scholar
8. Horiuchi Y, Iwanami A, Akiyama T, Hikata T, Watanabe K, Yagi M, et al. Spinal arteriovenös fistel som samexisterar inom ett spinal lipom: rapport om två fall. Spinal Cord Series Cases (2017) 3:17079. doi: 10.1038/s41394-017-0011-1
PubMed Abstract | CrossRef Full Text | Google Scholar
9. Weon YC, Chung JI, Roh HG, Eoh W, Byun HS. Kombinerad spifnal intramedullär arteriovenös missbildning och lipomyelomeningocele. Neuroradiology (2005) 47:774-9. doi: 10.1007/s00234-005-1336-1
PubMed Abstract | CrossRef Full Text | Google Scholar
10. Rice JF, Jelsma RK. Kombinerad arteriovenös malformation och intramedullärt lipom: kirurgi och emboloterapi. Am J Neuroradiol. (1986) 7:171-3.
PubMed Abstract | Google Scholar
11. Asakuno K, Kim P, Kawamoto T, Ogino M. Dural arteriovenös fistel och progressivt conus medullaris-syndrom som komplikationer av lumbaldiskektomi. Fallbeskrivning. J Neurosurg. (2002) 97(3 Suppl):375-9. doi: 10.3171/spi.2002.97.3.0375
PubMed Abstract | CrossRef Full Text | Google Scholar
12. Kang JW, Koo JH, Kim DK, Joo YJ, Kim TH, Song SH. Myelopati orsakad av spinal dural arteriovenös fistel efter första lumbala kotkroppsfraktur – en fallrapport. Ann Rehabil Med. (2011) 35:729-32. doi: 10.5535/arm.2011.35.5.729
PubMed Abstract | CrossRef Full Text | Google Scholar
13. Vankan Y, Demaerel P, Heye S, Van Calenbergh F, van Loon J, Maleux G, et al. Dural arteriovenös fistel som en sen komplikation av en fraktur i övre halsryggen. Fallbeskrivning. J Neurosurg. (2004) 100(4 Suppl Spine):382-4. doi: 10.3171/spi.2004.100.4.0382
PubMed Abstract | CrossRef Full Text | Google Scholar
14. Nishimura Y, Natsume A, Ginsberg HJ. Spinal dural arteriovenös fistel i samband med L-4 isthmisk spondylolisthesis. J Neurosurg Spine (2014) 20:670-4. doi: 10.3171/2014.3.SPINE13492
PubMed Abstract | CrossRef Full Text | Google Scholar
15. Khaldi A, Hacein-Bey L, Origitano TC. Spinal epidural arteriovenös fistel med sent uppkommen perimedullär venös hypertension efter lumbalkirurgi: fallrapport och diskussion av patofysiologin. Spine (2009) 34:E775-9. doi: 10.1097/BRS.0b013e3181ae4a52
PubMed Abstract | CrossRef Full Text | Google Scholar
16. Jablawi F, Nikoubashman O, Mull M. Arterial Hypertension is associated with symptomatic spinal dural arteriovenous fistulas. World Neurosurg. (2017) 103:360-3. doi: 10.1016/j.wneu.2017.04.050
PubMed Abstract | CrossRef Full Text | Google Scholar
17. Borden JA, Wu JK, Shucart WA. Ett förslag till klassificering av spinala och kraniala durala arteriovenösa fistelmissbildningar och konsekvenser för behandlingen. J Neurosurg. (1995) 82:166-79. doi: 10.3171/jns.1995.82.2.0166
PubMed Abstract | CrossRef Full Text | Google Scholar
18. Lawton MT, Jacobowitz R, Spetzler RF. Omdefinierad roll för angiogenes i patogenesen för durala arteriovenösa missbildningar. J Neurosurg. (1997) 87:267-74. doi: 10.3171/jns.1997.87.2.0267
PubMed Abstract | CrossRef Full Text | Google Scholar
19. Wojciechowski J, Kunert P, Nowak A, Dziedzic T, Czernicki T, Wojtowicz K, et al. Kirurgisk behandling av spinala durala arteriovenösa fistlar: Resultat, komplikationer och prognostiska faktorer. Neurol Neurochir Pol. (2017). 51:446-53. doi: 10.1016/j.pjnns.2017.07.001
PubMed Abstract | CrossRef Full Text | Google Scholar
20. Lucarelli E, Sangiorgi L, Benassi S, Donati D, Gobbi GA, Picci P, et al. Angiogenes i lipom: En experimentell studie i kycklingembryots chorioallantoiska membran. Int J Mol Med. (1999) 4:593-6. doi: 10.3892/ijmm.4.6.593
PubMed Abstract | CrossRef Full Text | Google Scholar
21. Jellema K, Tijssen CC, Fijnheer R, de Groot PG, Koudstaal PJ, van Gijn J. Spinal durala arteriovenösa fistlar är inte associerade med protrombotiska faktorer. Stroke (2004) 35:2069-71. doi: 10.1161/01.STR.0000135766.22285.dc
CrossRef Full Text | Google Scholar
22. Cools MJ, Al-Holou WN, Stetler WR Jr, Wilson TJ, Muraszko KM, Ibrahim M, et al. Filum terminale lipomas: prevalens, naturlig historia och konusposition. J Neurosurg Pediatr. (2014) 13:559-67. doi: 10.3171/2014.2.PEDS13528
PubMed Abstract | CrossRef Full Text | Google Scholar
23. Al-Holou WN, Muraszko KM, Garton HJ, Buchman SR, Maher CO. Utfallet av frigörande av tethered cord vid sekundärt och multipla upprepade tethered cord-syndrom. J Neurosurg Pediatr. (2009) 4:28-36. doi: 10.3171/2009.2.PEDS08339
PubMed Abstract | CrossRef Full Text | Google Scholar
24. Gioppo A, Farago G, Giannitto C, Caputi L, Saladino A, Acerbi F, et al. Sacrala durala arteriovenösa fistlar: en diagnostisk och terapeutisk utmaning – erfarenhet från ett enda centrum av 13 fall och genomgång av litteraturen. J Neurointerv Surg. (2017). 10:415-21. doi: 10.1136/neurintsurg-2017-013307
PubMed Abstract | CrossRef Full Text | Google Scholar
25. Oldfield EH, Bennett A 3rd Chen MY, Doppman JL. Framgångsrik hantering av spinala durala arteriovenösa fistlar som inte upptäckts med arteriografi. Rapport om tre fall. J Neurosurg. (2002) 96(2 Suppl):220-9. doi: 10.3171/spi.2002.96.2.0220
PubMed Abstract | CrossRef Full Text | Google Scholar