Co je to srážení?
Srážení je v kuchyni rozbití emulze nebo koloidu na velké části různého složení fyzikálně-chemickými procesy flokulace, krémování a koalescence. Srážení je záměrné a žádoucí při výrobě sýrů a tofu; nezáměrné a nežádoucí při výrobě omáček a krémů. Ke srážení dochází přirozeně v mléce, pokud se mléko nespotřebuje do data spotřeby nebo pokud mléko zůstane venku v teple.
Mléko se skládá z několika sloučenin, především z tuku, bílkovin a cukru. Bílkoviny v mléce jsou obvykle suspendovány v koloidním roztoku, což znamená, že malé molekuly bílkovin se volně a nezávisle vznášejí. Tyto plovoucí molekuly bílkovin lámou světlo a přispívají (spolu se suspendovaným tukem) k bílému vzhledu mléka. Za normálních okolností se tyto bílkovinné molekuly navzájem odpuzují, takže se mohou vznášet, aniž by se shlukovaly, ale při změně pH roztoku se mohou vzájemně přitahovat a vytvářet shluky. K tomu dochází při srážení mléka, kdy při poklesu pH a zvýšení kyselosti se molekuly bílkovin (kaseinu a dalších) vzájemně přitahují a stávají se z nich „sraženiny“ plovoucí v roztoku průsvitné syrovátky. Tato reakce shlukování probíhá rychleji při vyšších teplotách než při nízkých teplotách.
Jaké jsou podukty v mléce, které umožňují jeho srážení?
Mléko je emulze nebo koloid z kuliček másla a tuku ve směsi obsahující vodu, sacharidy, minerály a bílkoviny.
Hlavními složkami mléka jsou voda, tuk, bílkoviny, laktóza (mléčný cukr) a minerální látky (soli). Mléko obsahuje také stopová množství dalších látek, jako jsou barviva, enzymy, vitamíny, fosfolipidy (látky s vlastnostmi podobnými tuku) a plyny.
Jaký je obsah tuku v mléce?
Podle údajů The Dairy Council má plnotučné mléko 3,9 % tuku (tj. obsahuje 3,9 g tuku na 100 g), polotučné mléko má 1,7 % tuku, mléko s 1 % tuku má 1 % tuku a odstředěné mléko má 0,3 % tuku.
Jaké bílkoviny obsahuje mléko?
Většina mléka vypitého v USA pochází z mléčných žláz krav. Hlavní bílkoviny obsažené v mléce jsou jedinečné a nenacházejí se v jiných tkáních než v mléčných žlázách. Mléčné bílkoviny, zejména kaseiny, mají aminokyselinové složení užitečné pro růst a vývoj mláďat. Další bílkoviny v mléce zahrnují řadu enzymů, bílkoviny podílející se na transportu živin, bílkoviny podílející se na odolnosti vůči nemocem (protilátky a další), růstové faktory atd. (viz odkaz 1). Kasein tvoří 79,5 % bílkovin obsažených v kravském mléce
Mléko obsahuje 3,3 % celkových bílkovin. Mléčné bílkoviny obsahují všech 9 esenciálních aminokyselin potřebných pro člověka. Mléčné bílkoviny jsou syntetizovány v mléčné žláze, ale 60 % aminokyselin použitých k tvorbě bílkovin se získává z kravské stravy. Celkový obsah mléčných bílkovin a složení aminokyselin se liší v závislosti na plemeni krávy a genetice jednotlivých zvířat.2)
Syrovátkové bílkoviny tvoří 19,3 % obsahu bílkovin v mléce. V mléce většiny druhů jsou 3 nebo 4 kaseiny; jednotlivé kaseiny mají odlišné molekuly, ale podobnou strukturu. Všechny ostatní bílkoviny, které se v mléce vyskytují, jsou sdruženy pod názvem syrovátkové bílkoviny. Hlavními syrovátkovými bílkovinami v kravském mléce jsou beta-laktoglobulin a alfa-laktalbumin.
β-laktoglobulin je hlavní syrovátkovou bílkovinou kravského a ovčího mléka a je přítomen i u mnoha dalších druhů savců; významnou výjimkou je člověk.

Molekula kaseinu
Rodina příbuzných fosfoproteinů (αS1, αS2, β, κ).
Kasein obsahuje vysoký počet prolinových zbytků, které spolu neinteragují. Neexistují zde ani disulfidické můstky. V důsledku toho má relativně málo terciární struktury. Je relativně hydrofobní, takže je špatně rozpustný ve vodě. V mléce se vyskytuje ve formě suspenze částic, tzv. kaseinových micel,
Kasein obsahuje vysoký počet prolinových zbytků, které spolu neinteragují. Neexistují v něm ani disulfidické můstky. V důsledku toho má relativně málo terciární struktury. Je relativně hydrofobní, takže je špatně rozpustný ve vodě. V mléce se vyskytuje ve formě suspenze částic, tzv. kaseinových micel,
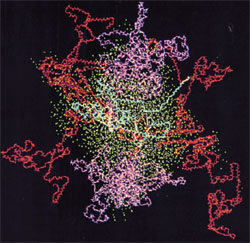
Obrázek: Kaseinová micela, kappa kasein modře, alfa kasein červeně, beta kasein purpurově, kyslík z vody azurově. Zdroj: Kumosinski, T.F., King, G. a Farrell, H.M., Jr. (1994). porovnání trojrozměrných molekulárních modelů hovězích submicelulárních kaseinů pomocí maloúhlového rozptylu rentgenového záření.
Kaseiny v kravském mléce mohou obsahovat různé formy, přičemž kravské mléko obvykle obsahuje jeden ze dvou typů beta kaseinu. v závislosti na genetickém profilu jednotlivé krávy bude produkované mléko obsahovat buď A1-beta kaseiny, nebo A2-beta kaseiny.
Všechny molekuly kaseinu mají alespoň jeden esterově vázaný fosfát. To nemá žádná ze syrovátkových bílkovin.
Izoelektrický bod kaseinu je 4,6.
Kasein má izoelektrický bod 4,6. Protože pH mléka je 6,6, má kasein v mléce záporný náboj.
Kaseiny mají velmi nerovnoměrné rozložení nábojů podél molekuly, zatímco u hlavních syrovátkových bílkovin jsou náboje rozloženy rovnoměrněji. To vysvětluje jednu z hlavních vlastností kaseinů v mléce, jejich amfifilní povahu. Nabité oblasti jsou obecně vodomilné neboli hydrofilní a nenabité oblasti podél molekuly jsou spíše hydrofobní neboli nenávidí vodu. Protože jsou tyto oblasti nerovnoměrně rozloženy podél molekuly, jsou tyto oblasti více exponované.
U proteinů s rovnoměrným rozložením se hydrofilní a hydrofobní oblasti v podstatě vzájemně vyruší. Právě díky amfifilní povaze molekul kaseinu vzniká jedna z nejdůležitějších vlastností kaseinu, kaseinová micela. Většina kaseinů v mléce se nachází ve složitých volných agregátech zvaných micely.
Kaseinová micela je stabilizována dvěma způsoby. Zaprvé fosforečnan vápenatý se v mléce vyskytuje ve vysokých koncentracích a uvnitř samotné kaseinové micely. Koncentrace je taková, že se tvoří malé agregace fosfátu. Část fosfátu může relativně volně přecházet do micely a z micely a část fosfátu je pevně vázána na bílkovinu. Tento vázaný fosfát je v malých agregacích nerozpuštěného (koloidního) fosforečnanu vápenatého. Ty mají tendenci stmelovat micelu a stabilizovat její strukturu.
K-kasein a srážení mléka
Další stabilizační účinek je způsoben vlastností K-kaseinu. K-kasein má ve své struktuře sacharidovou skupinu, která je esterifikována na threonin v bílkovině. Tato sacharidová skupina obsahuje některé záporně nabité skupiny. Výsledkem je, že K-kasein je v jedné části molekuly hydrofilnější. V micelách se K-kasein a do jisté míry i B-kasein samy umisťují co nejblíže vodnímu rozhraní micely nebo do něj zasahují. To stabilizuje micelu tím, že zabraňuje agregaci micel sterickým odpuzováním (zabráněním těsnému přiblížení mezi kaseinovými micelami) U K-kaseinu je peptidová vazba mezi 105. a 106. aminokyselinou zranitelná vůči hydrolýze proteolytickými enzymy (mikrobiální koagulátor nebo syřidlo). To je mechanismus tvorby sýřeniny (odstraněním části bílkoviny obsahující sacharidy a tím snížením sterické stability). Ztráta ochrany K-kaseinu umožňuje, aby se kaseinové micely shlukovaly a tvořily souvislou sýřeninu.
Aby bylo možné pochopit, jak chymosin sráží mléko, je třeba vědět něco o mléčných bílkovinách. Většinu mléčných bílkovin tvoří kasein a existují čtyři hlavní typy kaseinových molekul: alfa-s1, alfa-s2, beta a kappa. Kaseiny alfa a beta jsou hydrofobní bílkoviny, které se snadno srážejí vápníkem – běžná koncentrace vápníku v mléce je mnohem vyšší než koncentrace potřebná k vysrážení těchto bílkovin. Kasein kappa je však výrazně odlišná molekula – nesráží se vápníkem. Při vylučování se kaseiny samy sdružují do agregátů zvaných micely, v nichž se alfa a beta kaseiny nesrážejí díky interakcím s kappa kaseinem. V podstatě kappa kasein normálně udržuje většinu mléčných bílkovin rozpustných a zabraňuje jejich spontánnímu srážení.
Vstupuje chymosin
Chymosin proteolyticky rozřezává a inaktivuje kappa kasein, přeměňuje ho na parakappa-kasein a menší bílkovinu zvanou makropeptid. Para-kappa-kasein nemá schopnost stabilizovat micelární strukturu a kaseiny nerozpustné ve vápníku se vysráží a vytvoří tvaroh.
Molekuly kaseinu lze také oddělit od syrovátky vysrážením kaseinu kyselinou (podobně jako se to děje v žaludku při konzumaci mléka) nebo narušením micelární struktury částečnou hydrolýzou molekul bílkovin pomocí proteolytického enzymu. V žaludku mláďat mnoha druhů se nachází enzym zvaný rennin, který specificky hydrolyzuje část kaseinové micely, což vede k tvorbě tvarohu. Klasická metoda srážení kaseinu v kravském mléce, která se provádí v laboratoři, spočívá v pomalém přidávání HCl (0,1 N), čímž se sníží pH mléka na 4,6. Srážení kaseinu v kravském mléce se provádí v laboratoři. Kasein se postupně vysráží, zatímco ostatních mléčných bílkovin se vysráží poměrně málo. Různé kombinace řízeného srážení kyselinou a enzymatické hydrolýzy kaseinu jsou základem sýrařského průmyslu. Často se používají specifické bakteriální kultury k vytvoření podmínek pro snížené pH a sekreci proteolytických enzymů, které tvoří různé druhy sýrů.
Co je syrovátka?
Syrovátka je tekutina, která zůstane po sražení a scezení mléka. Syrovátkové bílkoviny se skládají z α-laktalbuminu, β-laktoglobulinu, sérového albuminu, imunoglobulinů,
Syrovátková bílkovina je vysoce kvalitní bílkovina přirozeně se vyskytující v mléčných výrobcích. Jedná se o „kompletní“ bílkovinu, která obsahuje všechny esenciální aminokyseliny požadované lidským organismem a je snadno stravitelná.
Sýrové bílkoviny, nazývané také sérové bílkoviny, neobsahují fosfor a nesrážejí se při pH 4,6.
Sýr lze použít k výrobě sýra ricotta. Tradičně se syrovátka z ovčího mléka vaří, dokud nevznikne měkký nadýchaný tvaroh.
Vliv pH
Při poklesu pH a zvýšení kyselosti se molekuly bílkovin (kaseinu) vzájemně přitahují a stávají se z nich „tvarohy“ plovoucí v roztoku průsvitné syrovátky. Tato reakce shlukování probíhá rychleji při vyšších teplotách než při nízkých teplotách.
Sraženiny jsou mléčný výrobek získaný srážením mléka v procesu zvaném srážení. Srážení může být způsobeno přidáním syřidla nebo jakékoli jedlé kyselé látky, jako je citronová šťáva nebo ocet, a následným ponecháním v klidu.