¿Qué es el cuajado?
En cocina, el cuajado es la ruptura de una emulsión o coloide en grandes partes de diferente composición mediante los procesos físico-químicos de floculación, cremación y coalescencia. El cuajado es intencionado y deseable en la elaboración de quesos y tofu; no intencionado y no deseable en la elaboración de salsas y natillas. La cuajada se produce de forma natural en la leche si ésta no se utiliza antes de la fecha de caducidad, o si la leche permanece al aire libre a temperaturas cálidas.
La leche está formada por varios compuestos, principalmente grasa, proteína y azúcar. La proteína de la leche está normalmente suspendida en una solución coloidal, lo que significa que las pequeñas moléculas de proteína flotan libremente y de forma independiente. Estas moléculas proteicas flotantes refractan la luz y contribuyen (junto con la grasa en suspensión) al aspecto blanco de la leche. Normalmente, estas moléculas de proteína se repelen entre sí, lo que les permite flotar sin aglutinarse, pero cuando el pH de su solución cambia, pueden atraerse entre sí y formar aglomeraciones. Esto es lo que ocurre cuando la leche se cuaja, ya que al bajar el pH y volverse más ácida, las moléculas de proteína (caseína y otras) se atraen entre sí y se convierten en «cuajos» que flotan en una solución de suero translúcido. Esta reacción de aglutinación se produce más rápidamente a temperaturas más cálidas que a temperaturas frías.
¿Cuáles son los poductos de la leche que le permiten cuajar?
La leche es una emulsión o coloide de glóbulos de grasa de mantequilla dentro de una mezcla que contiene agua, carbohidratos, minerales y proteínas.
Los principales componentes de la leche son el agua, la grasa, las proteínas, la lactosa (azúcar de la leche) y los minerales (sales). La leche también contiene trazas de otras sustancias como pigmentos, enzimas, vitaminas, fosfolípidos (sustancias con propiedades similares a las de la grasa) y gases.
¿Cuál es el contenido de grasa de la leche?
Según The Dairy Council, la leche entera tiene un 3,9% de grasa (es decir, contiene 3,9g de grasa por 100g), la leche semidesnatada tiene un 1,7% de grasa, la leche con un 1% de grasa y la leche desnatada tiene un 0,3% de grasa.
¿Qué proteínas contiene la leche?
La mayoría de la leche que se bebe en Estados Unidos procede de las glándulas mamarias de las vacas. Las principales proteínas que se encuentran en la leche son únicas y no se encuentran en otros tejidos que no sean las glándulas mamarias. Las proteínas de la leche, especialmente las caseínas, tienen una composición de aminoácidos útil para el crecimiento y el desarrollo de las crías. Otras proteínas de la leche incluyen una serie de enzimas, proteínas implicadas en el transporte de nutrientes, proteínas implicadas en la resistencia a las enfermedades (anticuerpos y otras), factores de crecimiento, etc. (véase la referencia 1). La caseína constituye el 79,5% de las proteínas que se encuentran en la leche de vaca.
La leche contiene un 3,3% de proteínas totales. Las proteínas de la leche contienen los 9 aminoácidos esenciales que necesita el ser humano. Las proteínas de la leche se sintetizan en la glándula mamaria, pero el 60% de los aminoácidos utilizados para construir las proteínas se obtienen de la dieta de la vaca. El contenido total de proteínas de la leche y la composición de aminoácidos varía en función de la raza de la vaca y de la genética de cada animal.(2)
La proteína de suero comprende el 19,3% del contenido proteico de la leche. Hay 3 o 4 caseínas en la leche de la mayoría de las especies; las diferentes caseínas son moléculas distintas pero de estructura similar. Todas las demás proteínas que se encuentran en la leche se agrupan bajo el nombre de proteínas del suero. Las principales proteínas del suero en la leche de vaca son la beta-lactoglobulina y la alfa-lactoalbúmina.
La beta-lactoglobulina es la principal proteína del suero de la leche de vaca y de oveja y también está presente en muchas otras especies de mamíferos; una notable excepción es el ser humano.

La molécula de caseína
Una familia de fosfoproteínas relacionadas (αS1, αS2, β, κ).
La caseína contiene un elevado número de residuos de prolina, que no interactúan. Tampoco hay puentes disulfuro. Como resultado, tiene relativamente poca estructura terciaria. Es relativamente hidrofóbica, por lo que es poco soluble en agua. Se encuentra en la leche como una suspensión de partículas, llamadas micelas de caseína,
La caseína contiene un elevado número de residuos de prolina, que no interactúan. Tampoco hay puentes disulfuro. Como resultado, tiene relativamente poca estructura terciaria. Es relativamente hidrofóbica, por lo que es poco soluble en agua. Se encuentra en la leche como una suspensión de partículas, llamadas micelas de caseína,
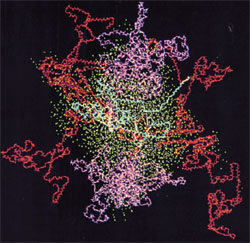
Imagen: Micela de caseína, caseína kappa en azul, caseína alfa en rojo, caseína beta en magenta, oxígeno del agua en cian. Fuente: Kumosinski, T.F., King, G. y Farrell, H.M., Jr. (1994).Comparación de los modelos moleculares tridimensionales de las caseínas submicelares bovinas con la dispersión de rayos X de ángulo pequeño.
Las caseínas de la leche de vaca pueden incluir diferentes formas, y la leche de vaca suele contener uno de los dos tipos de caseína beta. dependiendo del perfil genético de una vaca individual, la leche producida contendrá caseínas A1-beta o caseínas A2-beta.
Todas las moléculas de caseína tienen al menos un fosfato unido a un éster. Ninguna de las proteínas del suero tiene esto.
El punto isoeléctrico de la caseína es de 4,6. Dado que el pH de la leche es de 6,6, la caseína tiene una carga negativa en la leche.
Las caseínas tienen una distribución muy desigual de las cargas a lo largo de la molécula, mientras que en las principales proteínas del suero, las cargas están distribuidas más uniformemente. Esto explica una de las principales propiedades de las caseínas de la leche, su naturaleza anfifílica. Las regiones cargadas son, en general, amantes del agua o hidrófilas y las regiones no cargadas a lo largo de la molécula son más hidrofóbicas u odian el agua. Como estas regiones están repartidas de forma desigual a lo largo de la molécula, estas regiones están más expuestas.
En las proteínas con distribuciones uniformes, las regiones hidrofílicas e hidrofóbicas se anulan básicamente entre sí. Es debido a la naturaleza anfifílica de las moléculas de caseína que surge una de las propiedades más importantes de la caseína, la micela de caseína. La mayoría de las caseínas de la leche se encuentran en intrincados agregados sueltos llamados micelas.
La micela de caseína se estabiliza de dos maneras. En primer lugar, el fosfato de calcio se encuentra en altas concentraciones en la leche y dentro de la propia micela de caseína. La concentración es tal que se forman pequeños agregados de fosfato. Una parte del fosfato es relativamente libre para entrar y salir de la micela y otra parte está fuertemente unida a la proteína. Este fosfato unido se encuentra en pequeños agregados de fosfato cálcico no disuelto (coloidal). Estos tienden a cementar la micela estabilizando su estructura.
La K-caseína y el cuajado de la leche
El otro efecto estabilizador se debe a una propiedad de la K-caseína. La K-caseína tiene dentro de su estructura un grupo de carbohidratos que está esterificado a la treonina de la proteína. Este grupo de carbohidratos contiene algunos grupos cargados negativamente. El resultado es que la K-caseína se hace más hidrófila en una parte de la molécula. En la micela, la K-caseína y, en cierta medida, la B-caseína se auto-ubican cerca de la interfaz de agua de la micela o se extienden hacia ella. Esto estabiliza la micela impidiendo la agregación de las micelas por repulsión estérica (impidiendo el acercamiento entre las micelas de caseína). En el caso de la K-caseína, el enlace peptídico entre los aminoácidos 105 y 106 es vulnerable a la hidrólisis por enzimas proteolíticas (coagulante microbiano o cuajo). Este es el mecanismo de formación de la cuajada (al eliminar la parte de la proteína que contiene carbohidratos y reducir así la estabilidad estérica). La pérdida de la protección de la caseína K permite que las micelas de caseína se agreguen y formen una cuajada coherente.
Para entender cómo la quimosina coagula la leche, hay que saber algo sobre las proteínas de la leche. La mayor parte de la proteína de la leche es caseína y hay cuatro tipos principales de moléculas de caseína: alfa-s1, alfa-s2, beta y kappa. Las caseínas alfa y beta son proteínas hidrofóbicas que se precipitan fácilmente con el calcio: la concentración normal de calcio en la leche es muy superior a la necesaria para precipitar estas proteínas. Sin embargo, la caseína kappa es una molécula claramente diferente: no es precipitable por el calcio. Cuando las caseínas se segregan, se autoasocian en agregados denominados micelas, en los que las caseínas alfa y beta no se precipitan gracias a sus interacciones con la caseína kappa. En esencia, la caseína kappa normalmente mantiene soluble la mayor parte de la proteína de la leche y evita que se coagule espontáneamente.
Entra la quimosina
La quimosina corta e inactiva proteolíticamente la caseína kappa, convirtiéndola en para-kappa-caseína y en una proteína más pequeña llamada macropéptido. La para-kappa-caseína no tiene la capacidad de estabilizar la estructura micelar y las caseínas insolubles en calcio precipitan, formando una cuajada.
Las moléculas de caseína también pueden separarse del suero mediante la precipitación de la caseína con ácido (similar a lo que ocurre en el estómago cuando se consume leche) o mediante la alteración de la estructura micelar por hidrólisis parcial de las moléculas de proteína con una enzima proteolítica. En el estómago de las crías de muchas especies hay una enzima llamada renina que hidroliza específicamente parte de la micela de caseína dando lugar a la formación de una cuajada. Un método clásico de precipitación de la caseína en la leche de vaca que se realiza en el laboratorio consiste en añadir lentamente HCl (0,1 N) para bajar el pH de la leche a 4,6. La caseína formará gradualmente un precipitado, mientras que las demás proteínas de la leche precipitarán relativamente poco. Diferentes combinaciones de precipitación ácida controlada e hidrólisis enzimática de la caseína son la base de las industrias queseras. A menudo se utilizan cultivos bacterianos específicos para establecer las condiciones de disminución del pH y la secreción de enzimas proteolíticas que forman los diferentes tipos de queso.
¿Qué es el suero?
El suero es el líquido que queda después de que la leche se haya cuajado y colado. Las proteínas del suero están compuestas por α-lactoalbúmina, β-lactoglobulina, albúmina sérica, inmunoglobulinas,
La proteína del suero es una proteína de alta calidad que se encuentra de forma natural en los productos lácteos. Es una proteína «completa» que contiene todos los aminoácidos esenciales necesarios para el cuerpo humano y es fácil de digerir.
Las proteínas de suero, también llamadas proteínas de suero, no contienen fósforo y no se coagulan a un pH de 4,6.
El suero puede utilizarse para hacer queso ricotta. Tradicionalmente, el suero de la leche de oveja se cuece hasta obtener una cuajada suave y esponjosa.
Efecto del pH
A medida que el pH desciende y se vuelve más ácido, las moléculas de proteína (caseína) se atraen entre sí y se convierten en «cuajos» que flotan en una solución de suero translúcido. Esta reacción de aglutinación ocurre más rápidamente a temperaturas más cálidas que a temperaturas frías.
Los cuajos son un producto lácteo que se obtiene mediante la coagulación de la leche en un proceso llamado cuajado. La coagulación puede producirse añadiendo cuajo o cualquier sustancia ácida comestible, como el zumo de limón o el vinagre, y dejándola reposar.