Die Fähigkeit, die Thoraxhöhle vollständig zu entleeren, Ansammlungen von Pleuraflüssigkeit aufzulösen, alle Aspekte des Pleuraraums vollständig zu visualisieren und die Morbidität einer Thorakotomie zu vermeiden, hat die Thorakoskopie für die Behandlung von Empyemen und Hämothorax attraktiv gemacht.
Patientenauswahl
Die Fähigkeit, die Brusthöhle vollständig zu entleeren, Ansammlungen von Pleuraflüssigkeit aufzulösen, alle Aspekte des Pleuraraums vollständig zu visualisieren und die Morbidität einer Thorakotomie zu vermeiden, hat die Thorakoskopie für die Behandlung von Empyem und Hämothorax attraktiv gemacht.
Tabelle 1: Laborkriterien für die Drainage eines Empyems
Ein Erguss, der mehr als 50 % des Hemithorax einnimmt oder lokalisiert ist;
eine positive Gram-Färbung oder Kultur der Pleuraflüssigkeit;
eine eitrige Pleuraflüssigkeit mit einem pH-Wert unter 7.20 oder eine Glukose unter 60,
ein Milchsäure-Dehydrogenase-Wert von mehr als dem Dreifachen der oberen Normgrenze für Serum.
Patienten, bei denen durch eine Pleurapunktion ein infizierter Pleuraerguss nachgewiesen wird und die die Laborkriterien für einen Eingriff erfüllen, sind Kandidaten für eine thorakoskopische Dekortikation.
Wenn sich das Empyem im exsudativen oder fibrinopurulenten Stadium befindet und seit etwa 3 Wochen oder weniger besteht, ist die thorakoskopische Intervention in der Regel erfolgreich (Video 1, Video 2 unten). Wenn das Empyem länger als 3 Wochen besteht (Organisierungsphase), kann die Durchführung einer adäquaten Dekortikation aufgrund dichterer Adhäsionen und des Vorhandenseins einer anhaftenden pulmonalen viszeralen Schale schwieriger sein. Patienten mit einem exsudativen oder fibrinopurulenten Empyem können fast immer thorakoskopisch behandelt werden; eine CT-Untersuchung ist nicht hilfreich, um vorherzusagen, bei welchen Patienten eine Thorakotomie erforderlich ist. Die Umwandlung in eine offene Thorakotomie wird durchgeführt, wenn dies erforderlich ist, und sollte nicht als Versagen der Thorakoskopie, sondern vielmehr als Ausübung eines reifen chirurgischen Urteilsvermögens betrachtet werden. Die Thorakoskopie ist auch dann indiziert, wenn die Art des Pleuraprozesses nicht diagnostiziert werden kann, da sie eine gezielte Pleurabiopsie ermöglicht, die wahrscheinlich zur Diagnose führt und gleichzeitig die Morbidität einer Thorakotomie vermeidet. Weitere Indikationen für die thorakoskopische Dekortikation sind Hämothorax und mediastinales Debridement bei Patienten mit deszendierender Mediastinitis.
Eine vorherige Thorakotomie, eine vorherige Talkpleurodese und ein vorheriges Empyem sind relative Kontraindikationen für die Thorakoskopie. Die Unfähigkeit, eine Einzellungenbeatmung zu tolerieren und das Vorhandensein eines Fibrothorax sind Kontraindikationen für die Durchführung einer thorakoskopischen Dekortikation. Patienten, die nach einer Ösophagusperforation ein Empyem entwickeln, sollten nicht thorakoskopisch, sondern durch Thorakotomie behandelt werden.
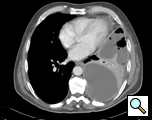
Abbildung 1: CT-Scan mit Empyem
Der CT-Scan des Brustkorbs gibt Aufschluss über die Lage, den Grad der Lokalisation, das Ausmaß des Empyems und das darunter liegende Lungenparenchym (Abbildung 1). Es ist nicht ungewöhnlich, dass ein Organismus in der Pleuraflüssigkeitskultur nicht identifiziert werden kann, weshalb bei der Diagnose eines Empyems eine Breitbandantibiose eingeleitet werden sollte. Dies kann geändert werden, wenn die Kulturdaten einen Organismus erkennen lassen. Die Antibiotika werden für den perioperativen Zeitraum beibehalten.
Der Ernährungszustand des Patienten sollte beurteilt werden, und bei Bedarf wird eine zusätzliche Nahrungszufuhr eingeleitet. Vor der Dekortikation sollte eine Bronchoskopie durchgeführt werden, um eine endobronchiale Obstruktion in dem vom Empyem eingeschlossenen Teil der Lunge auszuschließen.
Operative Schritte
Eine Vollnarkose wird eingeleitet und die Isolierung der Lunge erfolgt über einen doppellumigen Endotrachealtubus oder einen einlumigen Tubus mit Bronchialblocker. Dadurch kann die Lunge während der Dekortikation je nach Bedarf expandiert und kollabiert werden. Die intraoperative Überwachung umfasst eine arterielle Druckleitung, einen großvolumigen intravenösen Zugang, einen Foley-Katheter und eine Pulsoximetrie. Der Patient wird wie bei einer posterolateralen Thorakotomie gelagert.

Abbildung 3. Postoperative Röntgenaufnahme des Brustkorbs nach VATS-Dekortikation, mit platzierten Pleuradrainagen.

Abbildung 2b: Verwendung eines Retraktors, um den Arbeitsport offen zu halten.
Der Kamera-Port wird im 7. oder 6. Interkostalraum in der Linie der Spina iliaca anterior superior oder knapp davor platziert. Die VATS-Dekortikation und/oder Evakuierung des Hämothorax kann über 2 oder 3 Ports durchgeführt werden. Der Arbeitsport sollte über dem 5. Intercostalraum zwischen der mittleren und der vorderen Axillarlinie platziert werden. (Abbildung 2a) Der interkostale Einschnitt sollte 3 Finger Platz bieten. Zum Zurückziehen der Weichteile wird ein Weitlaner verwendet (Abbildung 2b). Ein dritter Port kann posterior platziert werden, um den Zugang zum vorderen Teil der Pleurahöhle zu ermöglichen.
Nach dem Zugang zum Brustkorb wird eine Yankauer-Absaugung verwendet, um den Brustkorb von Erguss oder Blut zu befreien (Video 3, Video 4 unten), und zusammen mit einem Finger werden einfache Lokulationen aufgelöst (Video 5 unten). Die präoperative CT-Aufnahme hilft bei dieser „blinden“ Anfangsdrainage und schafft einen funktionierenden Pleuraraum für die thorakoskopischen Instrumente. Gelatinöse fibrinöse Ablagerungen und Blutgerinnsel werden mit einer gebogenen Ringpinzette entfernt (Video 6, Video 7 unten). Die viszerale Pleuraschale kann mit einer Ringzange, einer Kürette (Video 8 unten) und einem Erdnuss-Dissektor wie bei einer offenen Dekortikation debridiert werden.
Nachdem ein Pleuraraum geschaffen wurde, erfolgt die Entfernung von fibrinösem Material über den seitlichen Teil der Pleurahöhle, beginnend vom Apex der Lunge bis zum Zwerchfell oder umgekehrt. Der Sauger und die Ringklammer werden zusammen verwendet, um das fibrinöse Material aus der Pleurahöhle zu entfernen, und die Kürette, die Erdnuss und die Ringklammer werden verwendet, um die Schwarte auf der Lunge zu sezieren. An der unteren Seite der Pleurahöhle ist es hilfreich, den unteren Lungenlappen zu identifizieren und vom Zwerchfell zu trennen (siehe Video 9 unten). Diese Ebene wird posterior und anterior entwickelt, so dass die Lunge den costodiaphragmatischen Sulcus ausfüllen kann, sobald die Dekortikation abgeschlossen ist. Als nächstes wird der hintere Aspekt des Pleuraraums debridiert und die darunter liegende Lunge dekortikiert. Die Freilegung wird durch Rollen des Patienten nach vorne erleichtert. Schließlich wird der vordere Teil des Pleuraraums debridiert und die Lunge von der Stelle befreit, an der sie mit dem Mediastinum verwachsen ist. Diese Freilegung wird durch das Rollen des Patienten nach hinten verbessert. Auf der linken Seite muss darauf geachtet werden, den Nervus phrenicus zu schützen.
Die intermittierende Beatmung der Lunge wird verwendet, um die Vollständigkeit der Dekortikation zu beurteilen, während die Dissektion fortschreitet. Wenn keine ausreichenden Fortschritte erzielt werden oder die Lunge sich nicht ausreichend ausdehnt, um den Brustkorb zu füllen, sollte eine offene Dekortikation durchgeführt werden. Besondere Vorsicht ist bei der Blutstillung (Video 10, Video 11 unten) sowohl der parietalen als auch der viszeralen Pleura geboten.
Wenn ein angemessenes Débridement erreicht ist, wird eine Spülung durchgeführt und die Lungenausdehnung visualisiert, um sicherzustellen, dass die Pleurahöhle von der Lunge gefüllt wird (Video 12 unten). Thoraxdrainagen können anterior und posterior zur Luft- und Flüssigkeitsdrainage gelegt werden. Wenn ein kleiner Raum über dem Zwerchfell vorhanden ist, wird ein rechtwinkliger Schlauch in dieser Position platziert, um die Drainage zu gewährleisten und eine allmähliche Ausdehnung der Lunge zu ermöglichen.
Die Brustschläuche werden unter Absaugung gehalten, um sicherzustellen, dass die Lunge vollständig ausgedehnt ist und der Pleuraraum ausreichend drainiert wird (Abbildung 3). Sobald die Drainage weniger als 200cc/24h beträgt, können die Schläuche entfernt werden. Bei Patienten mit einem Empyem werden intravenöse Antibiotika während des postoperativen Verlaufs und weitere 14 Tage lang orale Antibiotika nach der Entlassung des Patienten verabreicht. Bei Patienten mit Hämothorax werden die Antibiotika postoperativ für 48 Stunden fortgesetzt.
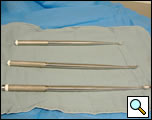
Abbildung 5. Lange Küretten zur Verwendung bei der VATS-Dekortikation.

Abbildung 4b: Offene gebogene Ringzange.
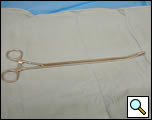
Abbildung 4a. Gebogene Ringzange geschlossen (linkes Feld) und geöffnet (rechtes Feld).
Präferenzkarte
- 30-Grad-Thorakoskop
- Gebogene Thorakoskopische Ringzange (Abbildungen 4a, 4b)
- Yankauer-Sauger
- Erdnuss-Dissektor
- Lange Küretten (Abbildung 5)
Tipps & Fallstricke
- Verwenden Sie einen Sauger / Finger / Mandelschwamm-Stick, um „blind“ einen Arbeitsraum in der Pleurahöhle zu schaffen.
- Vor dem Verlassen des Operationssaals prüfen, ob sich die Lunge wieder so ausdehnt, dass sie den Brustkorb ausreichend ausfüllt.
- Bei Unsicherheit über den Verlauf der Operation, die Blutung, die Größe des Luftlecks und die Wiederausdehnung der Lunge mit einer offenen Dekortikation fortfahren.
Ergebnisse
Die thorakoskopische Dekortikation hat sich inzwischen bei der Behandlung von Empyemen bewährt, und die Zeit, die seit der Entstehung des Empyems und dem chirurgischen Eingriff verstrichen ist, ist wahrscheinlich am aussagekräftigsten für die Fähigkeit, die Operation erfolgreich durchzuführen. Ein CT-Scan ist in dieser Hinsicht nicht nützlich, hilft aber bei der Platzierung des Ports und der Richtung der Dekortikation im Brustkorb. Die Grundsätze der offenen Dekortikation sollten bei der Anwendung der thorakoskopischen Technik befolgt werden. Alle Bereiche mit fibrinösem Material müssen entleert und die darunter liegende Lunge von einer einschränkenden Pleuraschale befreit werden, um eine vollständige Reexpansion zu ermöglichen. Die Erfolgsraten sind hoch und die Dauer der Thoraxdrainage, die Dauer des Krankenhausaufenthalts, die postoperativen Schmerzen und die Genesung sind besser als bei der Thorakotomie. Die Sterblichkeitsraten sind niedrig, ebenso die Rezidivraten und Komplikationen. Konversionen zur offenen Thorakotomie sind häufiger als nach anderen thorakoskopischen Eingriffen, aber dies sollte eher als Ausübung eines gesunden chirurgischen Urteilsvermögens denn als Versagen der Technik angesehen werden.
Die thorakoskopische Dekortikation erweitert die Vielseitigkeit des Thoraxchirurgen im Umgang mit Pleurainfektionen und kann zur Diagnose und Behandlung derselben mit hervorragenden Ergebnissen eingesetzt werden.
Video 1
Video 2
Video 3
Video 4
Video 5
Video 6
Video 7
Video 8
Video 9
Video 10
Video 11
Video 12
- Light RW. Parapneumonische Ergüsse und Empyeme. Proc Am Thorac Soc 2006;3:75-80.
- Cassina PC et al. Video-assisted thoracoscopy in the treatment of pleural empyema: stage-based management and outcome. J Thorac Cardiovasc Surg 1999;117:234-8.
- Lardinois D et al. Delayed referral and gram-negative organisms increase the conversion thoracotomy rate in patients undergoing video-assisted thoracoscopic surgery for empyema. Ann Thorac Surg 2005;79:1851-6.
- Roberts JR. Minimalinvasive Chirurgie bei der Behandlung von Empyemen: intraoperative Entscheidungsfindung. Ann Thorac Surg 2003;76:225-30.
- Navsaria PH, Vogel RJ, Nicol AJ. Thorakoskopische Evakuierung eines retinierten posttraumatischen Hämothorax. Ann Thorac Surg 2004;78:282-6.
- Shimizu K, et al. Successful video-assisted mediastinoscopic drainage of descending necrotizing mediastinitis. Ann Thorac Surg 2006;81:2279-81.
- Hope WW, Bolton WD, Stephenson JE. Nutzen und Zeitpunkt der chirurgischen Intervention bei parapneumonischem Empyem in der Ära der videounterstützten Thorakoskopie. Am Surg 2005;71:512-4.
- Luh SP, et al. Video-assisted thoracoscopic surgery in the treatment of complicated parapneumonic effusions or empyemas: outcome of 234 patients. Chest 2005;127:1427-32.
- Wurnig PN, et al. Video-assisted thoracic surgery for pleural empyema. Ann Thorac Surg 2006;81:309-13.