Mitä on juoksettuminen?
Keittiössä juoksettumisella tarkoitetaan emulsion tai kolloidin hajoamista suuriksi koostumukseltaan erilaisiksi osiksi fysikaalis-kemiallisten prosessien, kuten flokkulaation, kermankerroksen ja koalesenssin, avulla. Juoksettuminen on tahallista ja toivottavaa juuston ja tofun valmistuksessa; tahatonta ja epätoivottavaa kastikkeiden ja vaniljakastikkeiden valmistuksessa. Juoksettumista tapahtuu maidossa luonnostaan, jos maitoa ei käytetä viimeiseen käyttöpäivään mennessä tai jos maito pysyy ulkona lämpimässä lämpötilassa.
Maito koostuu useista yhdisteistä, pääasiassa rasvasta, proteiinista ja sokerista. Maidon proteiini on normaalisti suspendoituneena kolloidiliuoksessa, mikä tarkoittaa, että pienet proteiinimolekyylit kelluvat vapaasti ja itsenäisesti. Nämä kelluvat proteiinimolekyylit taittavat valoa ja vaikuttavat (yhdessä suspendoituneen rasvan kanssa) maidon valkoiseen ulkonäköön. Normaalisti nämä proteiinimolekyylit hylkivät toisiaan, jolloin ne voivat kellua paakkuuntumatta, mutta kun liuoksen pH-arvo muuttuu, ne voivat vetää toisiaan puoleensa ja muodostaa paakkuja. Näin tapahtuu, kun maito juoksettuu: kun pH laskee ja muuttuu happamaksi, proteiinimolekyylit (kaseiini ja muut) vetävät toisiaan puoleensa ja muodostuvat ”juoksutteiksi”, jotka kelluvat läpikuultavassa heraliuoksessa. Tämä paakkuuntumisreaktio tapahtuu nopeammin lämpimissä lämpötiloissa kuin kylmissä lämpötiloissa.
Mitkä ovat maidon sisältämät poduktiot, jotka mahdollistavat sen juoksettumisen?
Maito on emulsio tai kolloidi, joka muodostuu voi-rasvapalleroista vettä, hiilihydraatteja, kivennäisaineita ja proteiineja sisältävässä seosaineseoksessa.
Maidon tärkeimmät ainesosat ovat vesi, rasva, proteiinit, laktoosi (maitosokeri) ja kivennäisaineet (suolat). Maito sisältää myös pieniä määriä muita aineita, kuten pigmenttejä, entsyymejä, vitamiineja, fosfolipidejä (aineita, joilla on rasvan kaltaisia ominaisuuksia) ja kaasuja.
Minkälainen on maidon rasvapitoisuus?
The Dairy Councilin mukaan täysmaidossa on 3,9 % rasvaa (eli sisältää 3,9 g rasvaa 100 g:aa kohden), puolirasvattomassa maidossa 1,7 % rasvaa, 1 %:n rasvapitoisessa maidossa 1 % rasvaa ja rasvattomassa maidossa 0,3 % rasvaa.
Mitä proteiineja maito sisältää?
Suurin osa Yhdysvalloissa juodusta maidosta on peräisin lehmien maitorauhasista. Maidon sisältämät tärkeimmät proteiinit ovat ainutlaatuisia, eikä niitä esiinny muissa kudoksissa kuin maitorauhasissa. Maidon proteiineilla, erityisesti kaseiineilla, on aminohappokoostumus, joka on hyödyllinen nuorten kasvun ja kehityksen kannalta. Maidon muihin proteiineihin kuuluu joukko entsyymejä, ravintoaineiden kuljetukseen osallistuvia proteiineja, taudinkestävyyteen osallistuvia proteiineja (vasta-aineet ja muut), kasvutekijöitä jne. (ks. viite 1). Kaseiini muodostaa 79,5 prosenttia lehmänmaidon sisältämistä proteiineista.
Maito sisältää 3,3 prosenttia kokonaisproteiinia. Maidon proteiinit sisältävät kaikkia ihmisen tarvitsemia 9 välttämätöntä aminohappoa. Maidon proteiinit syntetisoidaan maitorauhasessa, mutta 60 % proteiinien rakentamiseen käytettävistä aminohapoista saadaan lehmän ravinnosta. Maidon kokonaisproteiinipitoisuus ja aminohappokoostumus vaihtelee lehmärodun ja yksittäisen eläimen genetiikan mukaan.(2)
Maidon proteiinipitoisuus on 19,3 % maidon proteiinipitoisuudesta. Useimpien lajien maidossa on 3 tai 4 kaseiinia; eri kaseiinit ovat erilaisia molekyylejä, mutta rakenteeltaan samanlaisia. Kaikki muut maidossa esiintyvät proteiinit ryhmitellään heraproteiinien nimellä. Lehmänmaidon tärkeimmät heraproteiinit ovat beetalaktoglobuliini ja alfalaktalbumiini.
β-laktoglobuliini on lehmän- ja lampaanmaidon tärkein heraproteiini, ja sitä esiintyy myös monissa muissa nisäkäslajeissa; huomattava poikkeus on ihminen.

Kaseiinimolekyyli
Sukulaisperheeseen kuuluvia fosfoproteiineja (αS1, αS2, β, κ).
Kaseiini sisältää runsaasti proliinijäämiä, jotka eivät ole vuorovaikutuksessa. Myöskään disulfidisiltoja ei ole. Tämän seurauksena sillä on suhteellisen vähän tertiäärirakennetta. Se on suhteellisen hydrofobinen, joten se liukenee huonosti veteen. Sitä esiintyy maidossa hiukkassuspensioina, joita kutsutaan kaseiinimiselleiksi,
Kaseiinissa on suuri määrä proliinijäämiä, jotka eivät ole vuorovaikutuksessa keskenään. Myöskään disulfidisiltoja ei ole. Tämän seurauksena sillä on suhteellisen vähän tertiäärirakennetta. Se on suhteellisen hydrofobinen, joten se liukenee huonosti veteen. Sitä esiintyy maidossa hiukkassuspensiona, jota kutsutaan kaseiinimikelliksi,
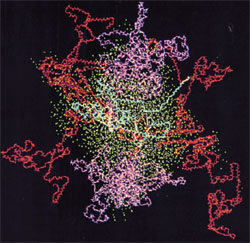
Kuva: Kaseiinimikkeli, kappakaseiini sinisenä, alfakaseiini punaisena, beetakaseiini magenttana, veden happi syaanina. Lähde: Kumosinski, T.F., King, G. ja Farrell, H.M., Jr. (1994). bovine submicellar caseins of the three dimensional molecular models of bovine submicellar caseins with small-angle X-ray scattering.
Lehmänmaidon kaseiinit voivat sisältää erilaisia muotoja. lehmänmaidossa on tyypillisesti jompaakumpaa kahdesta beta-kaseiinityypistä. yksittäisen lehmän geneettisestä profiilista riippuen tuotettu maito sisältää joko A1- beeta-kaseiineja tai A2- beeta-kaseiineja.
Kaikissa kaseiinimolekyyleissä on vähintään yksi esteriin sitoutunut fosfaatti. Yhdessäkään heraproteiinissa tätä ei ole.
Kaseiinin isoelektrinen piste on 4,6. Koska maidon pH on 6,6, kaseiinilla on maidossa negatiivinen varaus.
Kaseiineissa varaukset jakautuvat hyvin epätasaisesti pitkin molekyyliä, kun taas tärkeimmissä heraproteiineissa varaukset ovat tasaisemmin jakautuneet. Tämä selittää yhden maidon kaseiinien tärkeimmistä ominaisuuksista, niiden amfifiilisen luonteen. Varautuneet alueet ovat yleensä vettä rakastavia eli hydrofiilisiä, ja molekyylin varautumattomat alueet ovat hydrofobisempia eli vettä vihaavia. Koska nämä alueet ovat jakautuneet epätasaisesti pitkin molekyyliä, ne ovat alttiimpia.
Proteiineissa, joissa jakaumat ovat tasaisia, hydrofiiliset ja hydrofobiset alueet kumoavat periaatteessa toisensa. Juuri kaseiinimolekyylien amfifiilisen luonteen ansiosta syntyy yksi kaseiinin tärkeimmistä ominaisuuksista, kaseiinimikkeli. Suurin osa maidon kaseiineista esiintyy monimutkaisissa irtonaisissa aggregaatioissa, joita kutsutaan mikkeliksi.
Kaseiinimikelloa stabiloidaan kahdella tavalla. Ensinnäkin kalsiumfosfaattia on korkeina pitoisuuksina maidossa ja itse kaseiinimikellossa. Pitoisuus on sellainen, että fosfaatista muodostuu pieniä aggregaatioita. Osa fosfaatista pääsee suhteellisen vapaasti kulkeutumaan mikkeliin ja sieltä ulos, ja osa fosfaatista on vahvasti sitoutunut proteiiniin. Tämä sitoutunut fosfaatti on pieninä liukenemattoman (kolloidisen) kalsiumfosfaatin aggregaatioina. Nämä pyrkivät sementoimaan mikkelin yhteen ja vakauttamaan sen rakennetta.
K-kaseiini ja maidon juoksettuminen
Toinen vakauttava vaikutus johtuu K-kaseiinin ominaisuudesta. K-kaseiinilla on rakenteessaan hiilihydraattiryhmä, joka on esteröitynyt proteiinin treoniiniin. Tämä hiilihydraattiryhmä sisältää joitakin negatiivisesti varautuneita ryhmiä. Tämän seurauksena K-kaseiini muuttuu hydrofiilisemmäksi molekyylin yhdessä osassa. Mikkelissä K-kaseiini ja jossain määrin myös B-kaseiini sijoittuvat itsestään lähelle mikkelin vesirajapintaa tai ulottuvat siihen. Tämä vakauttaa mikkelin estämällä mikkelien aggregoitumisen steerisen hylkimisen vuoksi (estämällä kaseiinimikkelien läheisen lähestymisen). K-kaseiinin 105. ja 106. aminohapon välinen peptidisidos on herkkä proteolyyttisten entsyymien (mikrobiologinen koagulaattori tai juoksute) hydrolyysille. Tämä on juustomekanismi, joka johtaa juustomassan muodostumiseen (poistamalla proteiinin hiilihydraattia sisältävä osa ja vähentämällä siten steriittistä stabiilisuutta). K-kaseiinin suojan menettäminen mahdollistaa sen, että kaseiinimikellot aggregoituvat ja muodostavat yhtenäisen juustomassan.
Ymmärtääkseen, miten kymosiini hyydyttää maitoa, on tiedettävä jotain maitoproteiineista. Suurin osa maitoproteiinista on kaseiinia, ja kaseiinimolekyylejä on neljää päätyyppiä: alfa-s1, alfa-s2, beeta ja kappa. Alfa- ja beetakaseiinit ovat hydrofobisia proteiineja, jotka kalsium saostaa helposti – maidon normaali kalsiumpitoisuus on paljon suurempi kuin mitä näiden proteiinien saostamiseen tarvitaan. Kappakaseiini on kuitenkin selvästi erilainen molekyyli – se ei saostu kalsiumilla. Kun kaseiinit erittyvät, ne assosioituvat itsestään mikelleiksi kutsutuiksi aggregaateiksi, joissa alfa- ja beetakaseiinit eivät pääse saostumaan, koska ne ovat vuorovaikutuksessa kappakaseiinin kanssa. Pohjimmiltaan kappakaseiini pitää normaalisti suurimman osan maitoproteiinista liukoisessa tilassa ja estää sen spontaanin hyytymisen.
Kymosiini
Kymosiini leikkaa ja inaktivoi kappakaseiinia proteolyyttisesti ja muuttaa sen para-kappakaseiiniksi ja pienemmäksi proteiiniksi nimeltä makropeptidi. Para-kappa-kaseiinilla ei ole kykyä stabiloida mikellarirakennetta ja kalsiumiin liukenemattomat kaseiinit saostuvat muodostaen juustomassan.
Kaseiinimolekyylit voidaan erottaa herasta myös saostamalla kaseiini hapolla (samaan tapaan kuin mitä tapahtuu vatsassa maitoa nautittaessa) tai hajottamalla mikellarirakenne proteiinimolekyylien osittaisella hydrolyysillä proteolyyttisen entsyymin avulla. Monien lajien nuorten poikasten vatsassa on entsyymi nimeltä renniini, joka erityisesti hydrolysoi osan kaseiinimikkelistä, jolloin muodostuu juustomassaa. Lehmänmaidon kaseiinin klassinen saostusmenetelmä, joka tehdään laboratoriossa, on lisätä hitaasti HCl:ää (0,1 N) maidon pH:n laskemiseksi 4,6:een. Kaseiini muodostaa vähitellen saostuman, kun taas muita maitoproteiineja saostuu suhteellisen vähän. Juustoteollisuuden perustana ovat kaseiinin hallitun happosaostuksen ja entsymaattisen hydrolyysin erilaiset yhdistelmät. Usein käytetään erityisiä bakteeriviljelmiä sellaisten olosuhteiden luomiseksi, joissa pH-arvo laskee ja erittyy proteolyyttisiä entsyymejä, jotka muodostavat erityyppisiä juustoja.
Mitä on hera?
Hera on neste, joka jää jäljelle maidon juoksettumisen ja siivilöinnin jälkeen. Heraproteiinit koostuvat α-laktalbumiinista, β-laktoglobuliinista, seerumin albumiinista, immunoglobuliineista,
Vehnäproteiini on maitotuotteissa luonnostaan esiintyvä korkealaatuinen proteiini. Se on ”täydellinen” proteiini, joka sisältää kaikki ihmiskehon tarvitsemat välttämättömät aminohapot, ja se on helposti sulavaa.
Whey-proteiinit, joita kutsutaan myös seerumiproteiineiksi, eivät sisällä fosforia eivätkä hyydy pH-arvossa 4,6.
Whey-proteiinista voidaan valmistaa ricottajuustoa. Perinteisesti lampaanmaidosta saatu hera keitetään, kunnes se on pehmeää kuohkeaa juustomassaa.
PH:n vaikutus
Kun pH laskee ja muuttuu happamammaksi, proteiinimolekyylit (kaseiini) vetävät toisiaan puoleensa ja muuttuvat ”juustomassoiksi”, jotka kelluvat läpikuultavassa heraliuoksessa. Tämä paakkuuntumisreaktio tapahtuu nopeammin lämpimämmissä lämpötiloissa kuin kylmissä lämpötiloissa.
Juustomassa on maitotuote, joka saadaan hyydyttämällä maitoa prosessissa, jota kutsutaan juoksettumiseksi. Hyytyminen voidaan aiheuttaa lisäämällä juoksutetta tai mitä tahansa syötäväksi kelpaavaa hapanta ainetta, kuten sitruunamehua tai etikkaa, ja antamalla sen sitten vaikuttaa.