Keywords
hypermobiliteetti, sidekudosdysplasia, ehlers-danlosin oireyhtymä, Beightonin asteikko, dysautonomia, posturaalinen ortostaattinen takykardiaoireyhtymä, ärtyvän suolen oireyhtymä, syöttösolujen aktivoitumishäiriö, nivel- ja autonominen dysplasia
Esittely
Täysin aliarvioituja ja traagisesti huonosti hoidettuja ovat ne 20 % naisista ja 10 % miehistä, joiden kudokset ovat keskimääräistä notkeampia ja hauraampia . Harvat mahdollisuudet ennaltaehkäisyyn ja hoitoon ovat suuremmat kuin hypermobiliteetin tunnistaminen, joka on helppo seuloa pyytämällä potilasta painamaan peukaloaan kyynärvartta vasten (kuva 1). Tämä varoittava merkki voi viitoittaa tietä yksityiskohtaisempaan arviointiin, joka kuuluu hyvin yleislääkärin tehtäviin, sillä hänen laaja kliininen tietämyksensä sopii hyvin yhteen niiden monijärjestelmäisten ongelmien kanssa, joita löysä sidekudos voi aiheuttaa. Tarkastelen tässä hypermobiliteettihäiriöiden luonnetta, osoitan, että pikemminkin yleinen kuin alakohtainen tietämys voi johtaa elämää muuttaviin hoitomuotoihin näille potilaille, ja osoitan, miten geenitestaus tuo fibromyalgian tai kroonisen väsymysoireyhtymän kaltaiset oirekuvaukset täsmälääketieteen erottelevaan valoon.
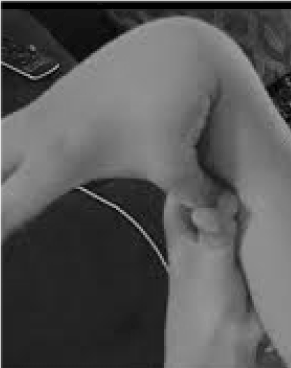
Kuva 1. Hypermobiliteetti.
Monet esteet on voitettava, ennen kuin hypermobiliteettipotilaat voivat kerätä yleislääketieteen edut. Ensimmäinen johtuu liittyy ihotautilääkäreiden Ehlersin ja Danlosin uraauurtavaan mutta lyhytnäköiseen keskittymiseen, joka painoi uskomattoman ja eksoottisen ihon venymisen harhaanjohtavaksi symboliksi sidekudoksen löysyyshäiriöille. Toinen este on kasvava kuilu käytännöllisen ja geneettisen lääketieteen välillä, sillä ensiksi mainittu keskittyy asianmukaisesti yleisiin sairauksiin, kun taas jälkimmäinen on viime aikoihin asti käyttänyt erikoistunutta teknologiaa harvinaisten sairauksien kuvaamiseen. Hämärät nimitykset pelottavine alatyyppeineen ja teknisine termeineen ovat kuin kutsumattoman vieraan maan pieniä maakuntia, joiden kartoittamiseen yksikään maailmanmatkailija ei käytä aikaa. Näiden esteiden torjumiseksi hypermobiliteettihäiriöihin sovelletaan käytännönläheistä lähestymistapaa, jossa keskitytään tunnistamiseen anamneesin ja lääkärintarkastuksen perusteella ja jätetään nimien, alatyyppien ja geneettisten testien tekniset yksityiskohdat erikoislääkäreille, joihin otetaan yhteyttä sen jälkeen, kun on otettu yhteyttä tärkeän ensimmäisen vaiheen eli oletusdiagnoosin jälkeen. Kun joustava potilas on tunnistettu ja lähetetty, hän on edelleen riippuvainen perusterveydenhuollon lääkäristään, sillä vain hän voi sisällyttää suositukset ja testitulokset yleiseen hoitokotiin.
Terminologia
Lisääntynyttä liikelaajuutta useissa nivelkohdissa (nivelissä) esiintyy suuressa määrässä sairauksia kromosomihäiriöistä, kuten Downin oireyhtymässä, häiriöihin, kuten Ehlersin-Danlosin oireyhtymässä (EDS), joka on tunnettu hypermobiliteetistaan. McKusick popularisoi tämän kudosten löysyydestä tunnettujen sairauksien luokan ryhmittelemällä ne perinnöllisiksi sidekudoksen sairauksiksi, mukaan lukien Marfanin oireyhtymä, johon hän keskittyi kardiologina. Vuonna 1977 tohtori Peter Beighton, joka tunnetaan joustavuutta mittaavasta asteikostaan, organisoi kirjallisuuden ja esitti 6-7 EDS-tyyppiä, jotka viimeaikaisissa ohjeissa on nyt yksinkertaistettu klassiseksi, verisuoniperäiseksi ja hypermobiliseksi EDS-tyypiksi. Nyt on selvää, että näillä tyypeillä on huomattavia päällekkäisiä oireita keskenään ja niihin liittyvien sairauksien, kuten osteogeneesi imperfektin (johon liittyy lukuisia murtumia), Marfanin oireyhtymän (suurten verisuonten laajeneminen/dissektio), Sticklerin oireyhtymän (silmä- ja niveltulehdusmuutokset) ja monien muiden sairauksien välillä.
Ed ole niinkään huolissani tietyistä taudeista, vaan pidän hyödyllisempänä keskittyä kahteen tärkeimpään tautiprosessiin, jotka johtuvat sidekudosdysplasiasta, ja niitä havainnollistaa taulukossa 1 lueteltujen monien eri taudinaiheuttajien oireet. Ensimmäinen on nivelkipujen kuluminen (nivelrikko), joka eroaa tulehduksellisen (autoimmuuni- tai tulehduksellisen) niveltulehduksen turvonneista, punoittavista nivelistä, joita esiintyy nivelreumassa, lupuksessa, Sjögrenin oireyhtymässä tai selkärankareumassa. Toinen on autonomisen hermoston epätasapaino (dysautonomia), joka johtuu elastisten verisuonten aiheuttamista hypermobiliteettihäiriöistä . Distensiiviset verisuonet aiheuttavat veren kerääntymistä lantioon ja jalkoihin, jolloin verenpaine laskee ja seisomaan noustessa tulee huimausta tai pyörtymistä (ortostaattinen hypotensio). Vähentynyt verenkierto päähän aktivoi ajan mittaan autonomisen hermoston sympaattisen haaran (adrenaliinin ”pakene tai taistele” -haara), mikä johtaa useisiin ongelmiin: 1) posturaalinen ortostaattinen takykardiaoireyhtymä (postural orthostatic tachycardia syndrome, POTS), johon liittyy takykardiaa, ahdistuneisuutta, kroonista väsymystä ja ”aivosumua” (keskittymiskyvyn ja muistin heikkenemistä), 2) ärtyvän suolen oireyhtymä, joka johtuu suoliston motiliteetin estymisestä (parasympaattinen suppressio) ja jossa ummetus vuorottelee ripulin kanssa, turvotus, refluksi, vatsakipu, nielemishäiriö, pahoinvointi, ja 3) syöttösolujen aktivoitumishäiriö, johon liittyy ohimenevää ihottumaa, nokkosihottumaa/reaktiivista ihoa, astmaa/hengenahdistusta ja ruoka-/lääkeintoleranssia. Olen keksinyt laajemman termin, joka helpottaa minkä tahansa hypermobiliteettihäiriön tunnistamista ja jossa tunnustetaan nivelten/kudosten löysyyden kaksi tärkeintä seurausta: artikulo-autonominen dysplasia tai nivel-väsymyskompleksi.
Taulukko 1. Nivelten ja kudosten löysyys. Tyypilliset löydökset ja niiden yleisyys hypermobiliteettioireyhtymissä. *320 yli 12-vuotiaasta nais- ja 54 miespotilaasta, jotka arvioitiin yksityiskohtaisilla kyselylomakkeilla vuonna 2017; TMJ, temporomandibulaarinen nivel; POTS, posturaalinen ortostaattinen takykardiaoireyhtymä. Oireiluettelo mukautettu osittain lähteestä Wilson GN, Cooley WC: Preventive Health Care for Children with Genetic Condition: Providing a Medical Home. 2nd ed. Cambridge, MA. Cambridge University Press, 2006.
HISTORIA (prosenttiosuudet)*
Infancy: Koliikki (28), syöttämisvaikeudet (19,4); kömpelö, paljon kaatumisia (29,1)
Lapsi/teini-ikäinen: Hidas painonnousu (12); tietoinen notkeudesta (55.6); esitteli niveltemppuja (53.6)
Varhaiset nivelkivut (42.1); teini-ikäisten aktiviteetteja rajoitti kipu-vamma (55.4); varhaiset silmälasit (46.8)
Ortodontiat (61.4 %) iensairaudet (11.3); huono kiille/monet reikiintymät (31.6)
Nivelongelmat: Poksahtelu (81.6); subluksaatiot (62); TMJ popping, catching, kipu (51.2)
kipu vähintään 2 nivelessä (80.3); nivelleikkaukset (33); monet nyrjähdykset (26); murtumat >2 (31.5)
välilevyn välilevyn välilevyn tyräytyminen (29.3)
Luurangan ongelmat: Skolioosi (31); pectus (2.2); kävely-varpaat sisään/ulos (9.3); lattajalat (15.5)
iho: Helpot mustelmat (61); venyvä iho (15); samettinen (18); epätavalliset arvet (36.3)
juovat ennen raskautta (73); hidas paraneminen (32.4)
Virtsa- ja sukupuolielimet (naiset): (61.2); endometrioosi (11.3); munasarjakystat (55)
munasarjojen polykystinen oireyhtymä (8.5); virtsarakko-ongelmat (46.1); nivustyrä/femoraalinen tyrä (11.5)
hermolihas: Migreeni (51,7); päivittäinen päänsärky (62,3); tarvitsi päänsärkylääkettä (45)
Chiarin epämuodostuma (10,6); neurokirurgia (2,9); puutuminen/kouristelu (48,7); huono tasapaino (48,6)
neuropaattiset ampumakivut (37,3); lihassäryt/kouristukset (51,7); lihasheikkous (32,4)
GI/suolistonet:
sappirakon ongelmat (12,9); nielemisvaikeudet (23); usein esiintyvä pahoinvointi (44,9)
Sydän: Mitraaliläpän prolapsi (8,7); aneurysma (0,9); muu rytmihäiriö kuin takykardia (6,8)
POTS: Huimaus seistessä (69,8); pyörtyminen (34,5); krooninen väsymys (81,8); univaikeudet (43,5)
aivosumu (huono muisti tai keskittymiskyky ajoittain-70,8); lämpö/kylmäyliherkkyys (77,5); epänormaali hikoilu (25); takykardia (72,8); ahdistuneisuuspaniikkikohtaukset (61,3); suola-alttius (51,2)
Laboratorio/kuvantaminen: Alhainen luuntiheys (2.1); alhainen D-vitamiinipitoisuus (28.7); alhainen B12-vitamiinipitoisuus (2.7); kilpirauhasen vajaatoiminta (11.5); alhainen ferritiini (1.7); alhainen rautapitoisuus (6.7); kohonnut ydinvasta-ainepitoisuus (7.1)
Keskimääräinen määrä löydöksiä 80:stä: naiset >12 (35.4 löydöksiä) miehet >12 (21.5 löydöksiä)
Fyysinen (prosentteina)
Kehitt: Pituus >90. persentiili (55.2); raskas-BMI >28 (21.3); laiha-BMI <19 (14.2)
Marfanoidinen habitus (44); araknodaktylia (46.4); Walker-Murdoch-merkki läsnä (40.2)
Kasvot: Pitkä (25.7); ahtaat alakasvot (5.4); siniharmaa kovakalvo (1.6); korkea suulaki (53.5)
Nahka: Pehmeä (81.4); läpikuultava (23.8); elastisen kohoava >1 tuuman poimu leuan ympärillä kyynärvarren puolivälissä (51.3)
Poimut koostuvat uloimmasta (epidermisestä) kerroksesta (35.4); epätavalliset arvet (42,1 %)
Beighton-pisteet: 0-3 pistettä (8,4); 4-6 pistettä (32,6); 7-8 pistettä (38,8); 9:stä 9 pistettä (20,2)
Muut maneerit: Yhdistä kädet olkapään yli-selän takana (68)
ylöspäin suuntautuva rukousmerkki selän takana (71.3); tuo käsi selän ympäri koskettamaan napaa (19.5)
Luusto: Niskan kyfoosi (41.2); skolioosi (22.3); lordoosi (32.8); litteät jalat (39.6)
kävely – varpaat sisään tai ulos (28.3)
Neurologinen: Lihasheikkous (11.2); vähentynyt lihasmassa (8.8)
huono tasapaino tandemkävelyllä (33.4)
Löydösten keskimääräinen lukumäärä 40:stä: naiset >12 (17.9 löydöstä) miehet >12 (15.7 löydöstä)
Articulo-Autonomic Dysplasia (AAD)
Termi ”articulo-autonomic dysplasia” tai AAD voi yhtenäistää lähestymistapaa sidekudoksen veltostumishäiriöihin/hypermobiliteettihäiriöihin ja torjua kolme ongelmaa, jotka vaikeuttavat niiden tunnistamista: 1) monet lääkärit ja geneetikot pitävät sidekudosdysplasioita harvinaisina ja äärimmäisinä sairauksina, vaikka todellisuudessa niitä esiintyy noin yhdellä prosentilla väestöstä. 2) EDS-diagnostiikkaohjeet, vaikka niissä yksinkertaistetaankin tärkeimmät EDS-tyypit klassiseksi, vaskulaariseksi ja hypermobiliteetiksi, aiheuttavat edelleen sekaannusta viittaamalla moniin vähäisempiin tyyppeihin, jotka muodostavat päällekkäisen oirekuvion. 3) EDS:ään ja siihen liittyviin häiriöihin liittyvää melkeinpä pakollista dysautonomiaa (taulukko 1) on jätetty pois diagnoosikriteerinä, mikä on kuin kuvailisi elefanttia, mutta ei mainitsisi sen runkoa. AAD tarkoittaa väistämätöntä fysiologista yhteyttä löysäkudoksen ja dysautonomian välillä samalla tavalla kuin metaboliset tai hepatorenaaliset oireyhtymät kuvaavat sitä, miten lihavuus johtaa maksasairauteen/diabetekseen tai maksan vajaatoiminta aiheuttaa munuaissairauden.
Kuten useimmat lääketieteelliset kuviot tai oireyhtymät, EDS mukaan lukien, AAD on oirekompleksi, jolla on monia perimmäisiä syitä. ”Articulo” viittaa niveleen, tunnustaen, että minkä tahansa nivelkomponentin – ihon, hermon, lihaksen, luun, sidekudoksen, verisuonen – vaivaaminen aiheuttaa samanlaisen nivelkudoksen löysyyden kuvion, johon liittyy autonominen epätasapaino. Iho on hauras, luun tiheys on alentunut ja se on altis murtumille, lihakset ovat heikot ja niihin liittyy kipua (myalgia), neuropatiaa, johon liittyy puutumista tai pistelyä, karpaalitunnelia tai alueellisia kipuoireyhtymiä, autonomisia muutoksia, mukaan luettuina takykardia, ahdistuneisuus, unen palautumattomuus, suoliston liikkumattomuus, nokkosihottuma, ihottuma, ruoka- ja lääkitys-intoleranssit, ja näitä muutoksia esiintyy vaihtelevassa laajuudessa, jopa tietyntyyppisissä EDS-taudityypeissä. En ole havainnut suuria eroja potilaiden välillä, jotka sopivat tiettyihin EDS-tyyppeihin, mistä esimerkkinä ovat useammin esiintyvät ihomuutokset tyypin I klassisessa cEDS:ssä ja suurempi nivelten joustavuus tyypin III hypermobilisessa hEDS:ssä. Oireiden esiintymistiheys 374:llä systemaattisella kyselyllä rekisteröidyllä potilaalla ei vaihdellut merkittävästi niiden potilaiden välillä, jotka diagnosoin cEDS:ksi tai hEDS:ksi, eivätkä edes ne kahdeksan potilasta, jotka tunnistettiin mahdolliseksi vaskulaariseksi vEDS:ksi, koska heillä oli kollageenin tyyppi III -geenin mutaatioita, eronneet merkittävästi toisistaan (aneurysmia, joka esiintyi yhdellä näistä kahdeksasta potilaasta, esiintyi yhtä harvoin muissa EDS-luokissa). Tärkeintä on EDS:n spektrin käsite, jota mielestäni parhaiten edustaa AAD.
EDS:n ja siihen liittyvien sidekudosdysplasioiden aiheuttaman AAD-oireyhtymän tunnistaminen ehkäisee surullisia potilasmatkoja erikoislääkäriltä toiselle, oireita aiheuttavia diagnooseja, kuten huimausta, pyörtymistä, fibromyalgiaa tai kroonista väsymystä, ja traagista kärsimystä, vaikka monia ennaltaehkäiseviä strategioita ja hoitomuotoja on saatavilla. Lisäksi dysautonomian tunnistaminen selittää POTS:n aiheuttaman ahdistuksen ja masennuksen, joka usein liittyy krooniseen kipuun tai toimintakyvyn rajoittamiseen , käyttäytymiserot, jotka voidaan tunnistaa pikemminkin lääketieteellisen kuin psykiatrisen sairauden seurauksiksi.
Geneettiset testit tukevat artikulo-autonomisen dysplasian käsitettä
Seurauksena niiden luonnehtimisesta periytyviksi sidekudoksen häiriöiksi , EDS:n ja siihen liittyvien häiriöiden äärimmäisempien muotojen todettiin osoittavan autosomaalista dominoivaa periytymistä, mikä tarkoittaa, että sairastuneilla yksilöillä on yksi normaali ja yksi epänormaali geenin muoto (alleeli). Dominoiva periytyminen on järkevää, koska epänormaalin alleelin tuottama viallinen proteiini, joka on analoginen vääntyneen tiilen kanssa, sekoittuisi toisen alleelin normaaliin tiileen ja muodostaisi aaltoilevan rakenteen. Nivelen tai nivelen tunnistaminen monikomponenttiseksi rakenteeksi, jota ympäröivä iho rajoittaa, jota sisäpuolinen luu ja rusto tukevat ja joka toimii sisäisen hermon, lihaksen, jänteen, nivelen limakalvon ja verisuonten välityksellä, merkitsee puolestaan sitä, että mikä tahansa näistä elementeistä voi muuttua niin, että syntyy dysplasia, joka on muiden perinnöllisten sairauksien aiheuttamista epämuodostumista poikkeava kudoshäiriö. DNA:n kloonauksen ja sekvensoinnin kehittyminen vahvistaisi autosomaalisen dominoivan periytymisen ja sellaisten geenien kyvyn, jotka muuttavat mitä tahansa nivelrakenteen elementtiä, aiheuttaa AAD:n oirekuvan.
Geneettinen testaus alkoi keskittymällä ”ehdokasgeeniin”, joka valittiin potilaan oireiden perusteella, kuten Marfanin oireyhtymän fibrilliini-1-geenin testaus osoittaa. Geenin DNA:n AGCT-kirjainten, nukleotidien ”tekstin”, sekvensointi saattoi paljastaa substituutioita tai ”kirjoitusvirheitä”, jotka muuttivat koodatun proteiinin aminohappoa ja sen aiottua toimintaa. Sitten tuli uusi teknologia nimeltä NextGen eli nopea rinnakkainen DNA-sekvensointi, joka vastaa kirjan kaikkien sivujen lukemista kerralla eikä päästä päähän. Tämä mahdollisti geeniryhmien (paneelien), kuten kardiomyopatiaa tai sidekudosdysplasiaa aiheuttavien geeniryhmien tai jopa kaikkien 23 000 geenin sekvensoinnin jokaisessa ihmissolussa (genomissamme) 2-3 kuukaudessa. Proteiineja koodaavien tai eksonisten geenialueiden sekvensointi, jota kutsutaan koko eksomin sekvensoinniksi (whole exome sequencing, WES), voidaan tilata monilta yrityksiltä, ja omassa käytännössäni se saatiin alle 200-300 dollarin omavastuukustannuksilla puolelle potilaistani (listahinta on 9000 dollaria, ja vakuutukselta laskutettava summa on noin 20 000 dollaria).
Vaikka WES: ssä yksityiskohtaisesti eriteltyjen keskimääräisten 12,000 DNA-varianttien tulkinta on edelleen ongelma, jota vähentää varianttien kasvava epidemiologia normaaleissa ja sairauspopulaatioissa, AAD-oireita aiheuttavien geenimuutosten saannot 620-potilaiden keskuudessa, joille tehtiin WES-menetelmä minun käytännössäni, ovat yli 60%. Yli 80 mutaation kollageenigeenien lisäksi, mukaan lukien kollageenityyppi I:n mutaatiot, jotka yleensä liittyvät osteogenesis imperfectaan, kollageenityyppi V:n mutaatiot, jotka usein liittyvät klassiseen EDS:ään, kollageenityyppien VI, IX ja XII mutaatiot, jotka on alun perin kuvattu myopatioiden yhteydessä, ja pelätty kollageenityyppi III, joka liittyy verisuoniperäiseen EDS-tautiin, on myös toistuvia mutaatioita geeneissä, joilla on vaikutusta iho-, hermo-, lihaskudos-, fibrillaari- ja verisuonten osatekijöihin, jotka vahvistavat käsitystä, jonka mukaan sairauden AAD:n yhteydessä minkä tahansa nivelen osatekijöiden muutokset tuottavat taulukossa 1 kuvatun merkkipiirroksen ja oirekuvan. Nyt EDS:n ja siihen liittyvien, AAD-käsitteen piiriin kuuluvien häiriöiden tunnistaminen voi tukea kliinistä vaikutelmaa objektiivisella DNA-todisteella, joka mahdollistaa potilaan ja perheen neuvonnan.
Yliliikkuvuushäiriöiden/AAD:n diagnosointi ja hoito
Nivelkipujen/nivelten hauraushäiriöiden ja autonomisten (suoliston, sydämen, immuunijärjestelmän häiriöt) pääoireiden varoittaminen voi johtaa nopeisiin testeihin, joilla voidaan todeta hypermobiliteetti, kuten kuviossa 1 esitetään. Peukalo kyynärvarteen -merkki voi edeltää koko Beightonin asteikkoa ja antaa yhden pisteen molemmin puolin sormien painamisesta taaksepäin yli 90 asteen kulmaan kädessä, peukaloiden koskettamisesta kyynärvarsiin, kyynärpään hyperextendoimisesta kädet ojennettuina, polvien hyperextendoimisesta niin, että muodostuu taaksepäin suuntautuva jalkakäyrä, ja yhden pisteen kyvystä koskettaa kämmeniä lattiaan . Taulukossa 1 esitettyjen oireiden kaltaisella lyhyellä tutkimuksella voidaan vahvistaa epäilys, jota voidaan mahdollisesti tukea sisällyttämällä fyysisiin tutkimuksiin joitakin taulukon 1 alaosassa lueteltuja arviointeja. On huomattava, että kaikki AAD-potilaat eivät ole pitkiä tai laihoja ja että huomattava osa heistä on ylipainoisia kivun ja väsymyksen aiheuttamien toimintarajoitusten vuoksi. Monilla on kimmoisa iho, joka tutkitaan vetämällä leuan ympärillä tai kyynärvarressa olevia poimuja ylöspäin, erityisesti silloin, kun nämä ovat ohuita, pinnallisia epidermiksen poimuja. Valkoisen kudoksen kertyminen tai keloidien muodostuminen arpien ympärille on yleistä, ja Beightonin tai muiden taulukossa 1 lueteltujen hypermobiliteettitoimenpiteiden arviointi voi olla hyödyllistä. Kävelyssä voidaan havaita vino asento, johon liittyy kaulan kaareutuminen eteenpäin, skolioosi ja lordoosi sekä litteät jalat tai varpaat ulospäin (enemmän kuin sisäänpäin). Joillakin potilailla lihasvoima on heikentynyt ja tasapaino on huono tandemkävelyssä, mutta yleislääkärin, jolla on vain vähän aikaa, on kiinnitettävä huomiota vain muutamaan näistä fyysisistä oireista; loput selviävät lähetteellä.
Tärkeimpiä ovat ortopedit, jotka tuntevat EDS:n nivelrikon ja sen liitännäismuutokset, kuten degeneratiiviset nivelmuutokset, ruston rappeutumisen, plica-kaistaleet ja kuolleen luun alueet. Kokenut ja konservatiivinen ortopedi, joka tunnistaa nivelten ”kiristämiseen” tai korvaamiseen tähtäävien leikkausten huonot tulokset, on toivottava. Kardiologi voi dokumentoida POTS:n käyttämällä kallistuspöytätestiä sydämen sykkeen ja verenpaineen ortostaattisten muutosten havaitsemiseksi ja tehdä myös sähkö- ja kaikukardiografisia tutkimuksia aortan laajentuman tai aneurysman poissulkemiseksi. Neurologi voi arvioida tavallista migreeniä tai päivittäistä päänsärkyä, Chiari-muodonmuutosta, jota esiintyy löysän aivokudoksen liukumisen ja tyrähtämisen yhteydessä, neuropatiaa, joka johtuu supistumisesta löysissä nivelissä, ja lihasmuutoksia, joita kuvataan oirekuvauksella fibromyalgia ja korostetaan usein esiintyvillä myopaattisilla geenimuutoksilla, jotka ovat synnyttämässä uutta termiä myopaattinen EDS . Allergologit, jotka tuntevat syöttösolujen aktivoitumisen, ja gastroenterologit, jotka voivat dokumentoida suolen heikon liikkuvuuden, ovat arvokkaita lisäyksiä erikoislääkäriryhmään, eikä kukaan ole arvokkaampi kuin perusterveydenhuollon lääkäri monien mahdollisesti tarvittavien suositusten ja lääkkeiden hallinnassa. Vaikka se voi tuntua oudolta geneetikon suusta sanottuna, mielestäni hoitoon johtavat erikoisalojen ulkopuoliset arvioinnit ovat tärkeämpiä kuin geneettinen arviointi ja testaus, mutta jälkimmäisistä voi olla apua psykiatrista sairautta koskevien olettamusten hälventämisessä.
Hoito alkaa liikuntaohjelmalla, josta voi olla hyötyä sekä nivelten hypermobiliteetista johtuvasta niveltulehduksesta että sen aiheuttamasta heijastuvasta dysautonomiasta. Huomion kiinnittäminen nivelkipuihin (kasvukivut esiintyvät yöllä) tai vammoihin / luuston epämuodostumiin voi käynnistää ennaltaehkäisyn tekemällä potilaan tietoiseksi tilastaan (huomaa taulukossa 1, että monet eivät tunnista joustavuuttaan epänormaaliksi). Kulumisvammoja voidaan ehkäistä tukemalla herkkiä niveliä, tukemalla selkää vyötärönauhoilla ja valitsemalla niveliä suojaavia aktiviteetteja, kuten uinti lenkkeilyn sijaan. Potilaiden tulisi pysyä aktiivisina ja harrastaa kohtalaista painonnostoa ja muita kohtuullisia aktiviteetteja nivelten ympärillä olevien lihasten rakentamiseksi, jotta vältetään kroonista väsymystä tai fibromyalgiaa pahentavat passiivisuuden syklit. Asianmukainen fysioterapia, kivunhoito, liikunnanohjaus ja anekdoottiset lääkkeet, kuten glukosamiini- ja kondroitiinivalmisteet, ovat auttaneet monia, mutta rentouttavia lääkkeitä, jotka poistavat nivelten lihasten suojan, ja steroidipistoksia, jotka peittävät alleen vammat, edistävät osteoporoosia/rappeutumista ja antavat vain tilapäistä helpotusta, olisi vältettävä.
Dysautonomian hoidon peruspilari on nesteytys (8-10 lasillista nestettä päivässä), suola (puuttuu labiili hypertensio) ja proteiinipitoinen ruokavalio, joilla kaikilla pyritään lisäämään veren nestemäärää ja parantamaan aivoverenkiertoa. Lisäravinnehoitoon voivat kuulua C-vitamiini (2 g päivässä) D-vitamiini (>2000 yksikköä päivässä, enemmän kuin monivitamiinien 400-800), B12-vitamiini (1-2,5 mg päivässä). Alhaiseen suoliston motiliteettiin tai gastropareesiin auttaa nesteiden välttäminen ennen aterioita, pienemmät ja tiheämmät ateriat, probiootit, entsyymivalmisteet ja monien ilmoitusten mukaan gluteenin ja maitotuotteiden vähentäminen, jotka ovat yleisiä ärsyttäjiä. Kardiologit tarjoavat POTS:n hoitoon kardiologeja (esim. beetasalpaajat, Midodrine, Florinef), neurologit tai kivunhoitoasiantuntijat (esim. Gabapentiini, Lyrica) tai allergologit antihistamiiniprotokollia syöttösolujen tukahduttamiseksi (esim. Zyrtec, Zantac, Cromolyn, Singulair), minkä lisäksi on saatavana monia lääkitysvaihtoehtoja. WES:n kaltaisten genomitestien, jotka ulottuvat sidekudosdysplasiaa aiheuttavien geenien ulkopuolelle, etuja ovat uudet löydökset, kuten lihaksiin liittyvät geenit, joiden nyt tiedetään aiheuttavan EDS:ää, ja satunnaisten tai toissijaisten löydösten, kuten rinta-munasarjasyöpägeenien mutaatioiden, dokumentointi. Vakavampiin oireisiin liittyvien geenien löytäminen antaa potilaille mahdollisuuden tietää jälkeläisiin kohdistuvat riskit ja valita arvojensa kanssa yhteensopivat prenataalisen tai preimplantaatiodiagnostiikan strategiat.
Tapauksen esittely
Eve tuli lääkärin vastaanotolle 18-vuotiaana huimaantuneena, pyörtyneenä, ahdistuneena ja vatsaansa myöten pahoinvoivana niin uupuneena, että hän vetäytyi eläkkeelle perjantai-iltaisin lepäilemään viikonlopun ajan. Hän oli ollut terve, aktiivinen voimistelu- ja huutosakin harrastaja, rohkea ja älykäs tyttö, jonka sinnikkyys loukkaantumisista huolimatta sai valmentajilta suosionosoituksia. Sitten tuli influenssa, josta hän ei koskaan toipunut, pahoinvointi, joka oli niin kova, ettei hän pystynyt syömään, laihtuminen, pyörtyminen luokassa, herääminen yöllä sydämen tykyttelyyn, herääminen aamulla ilman palauttavaa unta. Eve kävi monilla lääkäreillä, jopa päivystyksessä, kun sydämentykytys ja paniikki veivät häneltä hengen. Mikään ei ollut vialla, paitsi stressi, sanottiin, kaikki oli hänen mielessään. Lääkkeet rauhoittivat, mutta eivät parantaneet, ja väsymys ja sekavuus heikensivät hänen työtehtäviään, ja hän mietti, oliko hän tulossa hulluksi. Tunnistamatta jäi hänen pehmeä ja hauras ihonsa, kovat ja runsaat kuukautiset, päivittäiset päänsäryt ja, mikä silmiinpistävintä, hypermobiliteetti, jonka hän ja hänen perheensä olettivat olevan normaalia: ”Niin, me olemme taipuvaisia ja kaksinivelisiä, eikö kaikki olekin.” Eve olisi vastannut, jos häneltä olisi kysytty.
Onneksi Eve etsi uuden perusterveydenhuollon lääkärin, joka pystyi dokumentoimaan monet taulukossa I luetelluista oireista. Eevellä oli varhaisia koliikki- ja refluksitauteja, joihin liittyi imetysvaikeuksia, hän oli hyvin taipuisa, äiti kutsui häntä ”luuttomaksi” vauvaksi, ja kun hän oli vanhempi, hän istui polvillaan jalat ojennettuina takanaan (W-asento) sanomalla, että se oli mukavampaa. Aluksi hän käveli hitaasti, kaatui usein ja vaikutti kömpelöltä, mutta pian hän oli aktiivinen ja kiipeili kaikkialle, sai vanhempansa nyrpistelemään laittamalla jalan hänen kaulansa ympärille tai tekemällä spagaatin helposti. Ala-asteelle siirryttäessä hän alkoi kuitenkin valittaa nivelvaivoista, ja hänen jalkojaan särki öisin, ja polvet ja nilkat vaivasivat häntä liikunnan jälkeen. Lastenlääkäri vakuutti vanhemmille, että hänellä oli vain ”kasvukipuja”, mutta vanhemmat huolestuivat enemmän, kun hän yritti pelata jalkapalloa ja käänteli jatkuvasti nilkkojaan, ja eräässä nyrjähdyksessä hän joutui käyttämään kenkiä kahden kuukauden ajan sen jälkeen, kun todettiin rasitusmurtuma.
Eve joutui lopettamaan jalkapallon, mutta huomasi, että hän pärjäsi erinomaisesti voimistelussa iän karttuessa, ja hän valitsi lattiatelinevoimistelun harjoitukset, koska hänellä oli huono tasapaino palkeilla ja hänen olkapäänsä venähtivät tangoilla. Hän huomasi, että hänen nivelensä poksahtelivat liikkeessä, ja usein hän poksutteli niitä tahallaan, koska se näytti lievittävän jännitystä ja kipua. Hän kokeili cheerleadingia ja onnistui manöövereissä, mutta huomasi olevansa liian herkkä kuumuudelle. Muut tytöt kutsuivat häntä ”tomaattinaamaksi”, koska hän ylikuumeni harjoitusten aikana, ja hän väsyi helposti ja tarvitsi usein lepopäivän harjoitusten jälkeen. Hänen ruoansulatusongelmansa nousivat uudelleen esiin, ja hänellä oli usein ummetusta ja vatsakipuja, ja hän tunsi itsensä usein paisuneeksi ja tarvitsi laksatiiveja. Kuudennella luokalla hän jätti koulua väliin suolisto-ongelmiensa ja nivelkipujensa vuoksi ja tunsi itsensä usein väsyneeksi ja huimaavaksi. Hän ei tuntenut oloaan levänneeksi aamuisin ja otti usein päiväunia viikonloppuisin, mikä poikkesi hänen aiemmasta aktiivisesta ja innokkaasta elämäntyylistään. Hän tunsi itsensä usein ahdistuneeksi, eikä pystynyt jäljittämään sitä mihinkään tiettyyn koulu- tai perhestressiin, ja hän alkoi saada aamulla päänsärkyä, jonka hän luuli johtuvan huonosta unesta. Hänen vanhempansa veivät hänet jälleen lastenlääkärille, ja heille sanottiin jälleen, ettei mitään muuta vikaa ollut kuin tavallinen koulustressi.
Kun Eve oli 14-vuotias, hän sairastui pahaan flunssan kaltaiseen sairauteen, ja hän oli kuukauden poissa koulusta, koska hänellä oli voimakasta väsymystä, päänsärkyä, pahoinvointia, oksentelua ja laihtumista. Hänellä oli kauheaa huimausta ja jonkin verran rintakipua, ja hän tunsi sydämensä hakkaavan ajoittain (hänellä oli sydämentykytyksiä). Hänen vanhempansa kysyivät neuvoa toiselta lastenlääkäriltä, ja tämä lähetti Eevan kardiologille, joka arveli, että Evan takykardia johtui sairauteen liittyvästä stressistä ja ahdistuksesta. Hän antoi Eevelle propranololia, beetasalpaajaa, hidastamaan sydämen sykettä, mutta Eevan väsymys lisääntyi entisestään, ja hän oli nyt suurimman osan päivästä vuodepotilaana. Hänen nivelkipunsa lisääntyivät sairauden jälkeen, ja hän makasi sängyssä suurimman osan päivästä, oli surullinen ja muuttui ahdistuneeksi, kun hänen vanhempansa yrittivät viedä häntä ulos tai ajelulle. He veivät hänet takaisin toiselle lastenlääkärille, joka lähetti hänet psykiatriaan, ja Zoloft aloitettiin auttamaan ahdistukseen ja masennukseen. Muutaman päivän kuluttua Eve sai ihottumaa ja nokkosihottumaa, ja hänen oli lopetettava lääkitys. Hänellä oli edelleen huimausta, ja hän kävi vielä kahdella erikoislääkärillä, gastroenterologilla, joka arveli, että hänellä saattoi olla keliakia, ja korva-nenä-kurkkutautilääkärillä, joka diagnosoi huimauksen ja lähetti hänet neurologiaan. Hän kertoi kyseiselle lääkärille takaraivosta lähtevistä päänsäryistä, ja hänelle tehtiin selinmakuulla pään magneettikuvaus, joka oli normaali.
Erikoislääkärin tekemä todennäköinen AAD-diagnoosi johti erilaiseen kierrokseen erikoislääkärin lähetteillä, mukaan luettuna neurologia, jossa pystyasennossa tehty pään magneettikuvaus osoitti Chiari-muodonmuutoksen aiheuttaman tyrän. Kardiologi dokumentoi epänormaalin kallistuspöytäkokeen sekä alhaisen suolen liikkuvuuden ja osoitti, että hänen ahdistuneisuutensa ja stressi-väsymyksensä johtuivat dysautonomiasta. Ravitsemukselliset nesteytys-, suola- ja proteiinipitoiset strategiat sekä beetasalpaaja- ja antihistamiinihoito paransivat hänen väsymystään ja suolisto-oireitaan ja vähensivät hänen päänsärkyään. Päätettiin, että 4-5 mm:n Chiari-tyrä ei ollut niin suuri, että se olisi vaatinut leikkausta, ja hänen psykiatrinen hoitonsa katsottiin lääketieteellisen häiriön toissijaisten oireiden hoitamiseksi. Jotkut hänen kliiniseen diagnoosiinsa epäilevästi suhtautuneista erikoislääkäreistä vakuuttuivat geneettisistä testeistä, joissa todettiin muutos tyypin V kollageenin alfa-1-ketjun geenissä (lyhenne COL5A1), joka on yleinen löydös EDS-potilailla. Eve oli perinyt mutaation äidiltään, jolla oli ollut lievempiä AAD-oireita ja joka pystyi nyt hallitsemaan niitä paremmin.
Even terveys ja elinvoima palautuivat useiden kuukausien aikana, ja hän ”sai elämänsä takaisin”, kuten hän ja hänen vanhempansa sanoisivat. Hänellä oli edelleen ajoittain nivelkipuja, ahdistuneisuutta ja väsymystä, mutta ”viisas liikunta” lihassuojan rakentamiseksi nivelten ympärille, ravitsemukselliset lähestymistavat dysautonomiaan ja biofeedback-lähestymistavat ahdistuneisuuden torjumiseksi muuttivat elämää . Nämä hoidot olivat kaikki sen ansiota, että hänen perhelääkärinsä oli tunnistanut ne, sillä hän pystyi nyt koordinoimaan Eevan ja hänen äitinsä hoitoa ja tarjoamaan resursseja sekä EDS:n että sen taustalla olevien geenimuutosten ymmärtämiseksi. Seuraavalle sukupolvelle siirryttäessä Eevelle pystyttiin kertomaan, että hänellä oli 50 prosentin riski periytyä COL5A-mutaatiosta ja että hänellä oli riski ennenaikaiseen synnytykseen ja synnytyksen jälkeiseen verenvuotoon kaikissa tulevissa raskauksissa .
- Remvig L, Jensen DV, Ward RC (2007) Epidemiology of general joint hypermobility and basis for the proposed criteria for benign joint hypermobility syndrome: review of the literature . J Rheumatol 34: 804-809.
- Steinman B, Royce PM, Superti-Furga A (1993) The Ehlers-Danlos syndrome. In: Connective Tissue and its Heritable Disorders. B Steinman, PM Royce (Eds) Wiley-Liss: New York s. 351-407.
- McKusick VA (1956) Heritable disorders of connective tissue. CV Mosby: St. Louis.
- Bloom L, Byers P, Francomano C, Tinkle B, Malfait F (2017) The International Consortium on the Ehlers-Danlos Syndromes. Am J Med Genet Part C Semin Med Genet 175: 5-7.
- Gazit Y1, Nahir AM, Grahame R, Jacob G (2003) Dysautonomia nivelten hypermobiliteettioireyhtymässä. Am J Med 115: 33-40.
- Pizzo PA1 (2013) Oppitunteja kivunlievityksestä – henkilökohtainen jatkokokemus. N Engl J Med 369: 1092-1093.
- Pyeritz RE (2008) Pieni molekyyli suureen sairauteen. N Engl J Med 358: 2829-2831.
- 8. Wyandt HE, Wilson GN, Tonk VS. Luku 11: Geenien ja genomin sekvensointi: Geneettisen vaihtelun tulkinta nukleotiditasolla. In: Human Chromosome Variation: Heteromorphism, Polymorphism, and Pathogenesis, Ed.2. Springer Nature, Singapore
- Mefford HC (2012) Diagnostic exome sequencing–are we there yet? N Engl J Med 367: 1951-1953.
- http://hypermobility.org/help-advice/hypermobility-syndromes/beighton-score/
- Castori M, Morlino S, Celletti C (2013) Rewriting the natural history of pain and related symptoms in the joint hypermobility syndrome/Ehlers-Danlos syndrome, hypermobility type. Am J Med Genet A 12: 2989-3004.
- Simpson MR (2006) Benign joint hypermobility syndrome: evaluation, diagnosis, and management. J Am Osteopath Assoc 106: 531-536.
- Kirk JA, Ansell BM, Bywaters EG (1967) The hypermobility syndrome. Yleistyneeseen nivelten hypermobiliteettiin liittyvät tuki- ja liikuntaelinvaivat. Ann Rheum Dis 26: 419-425.
- Wilson GN (2014) Presymptomatic and preimplantation genetic diagnosis: Neurologia, NextGenetics ja seuraava sukupolvi. JAMA Neurol 71: 403-404.
- Castori M, Morlino S, Celletti C (2012) Kivun ja väsymyksen hoito nivelten hypermobiliteettioireyhtymässä (eli Ehlers-Danlosin oireyhtymässä, hypermobiliteettityyppi): periaatteet ja ehdotus monialaisesta lähestymistavasta. Am J Med Genet A 158: 2055-2070.
- Castori M, Morlino S, Celletti C (2013) Rewriting the natural history of pain and related symptoms in the joint hypermobility syndrome/Ehlers-Danlos syndrome, hypermobility type. Am J Med Genet A 161A: 2989-3004.
- Bathen T, Hangmann AB, Hoff M (2013) Ehlers-Danlosin oireyhtymän hypermobiliteettityypin/ hypermobiliteettioireyhtymässä esiintyvän työkyvyttömyyden monialainen hoito: pilottitutkimus, jossa käytettiin fysioterapian ja kognitiivisbehavioraalisen terapian yhdistelmää 12 naisella. Am J Med Genet A 161A: 3005-3011.
- EDS (2018) Ehlers-Danlosin oireyhtymän kansallinen säätiö.
- OMIM (2018) Online Mendelian Inheritance in Man.
- Wilson GN (2014) Sidekudosdysplasian eksomianalyysi: kliinisen genetiikan kuolema ja uudelleensyntyminen? Am J Med Genet A 164A: 1209-1212.