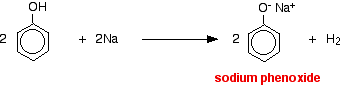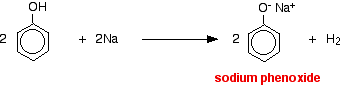Fenolin happamuus
Yhdisteet, kuten alkoholit ja fenoli, jotka sisältävät hiilivetyyn kiinnittyneen -OH-ryhmän, ovat hyvin heikkoja happoja. Alkoholit ovat niin heikosti happamia, että tavanomaisissa laboratoriotarkoituksissa niiden happamuus voidaan käytännössä jättää huomiotta. Fenoli on kuitenkin sen verran hapan, että sillä on tunnistettavasti happamia ominaisuuksia – vaikka se onkin edelleen hyvin heikko happo. Vetyioni voi irtautua -OH-ryhmästä ja siirtyä emäkseen. Esimerkiksi vesiliuoksessa:

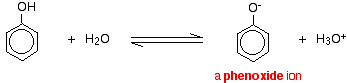
Fenoli on hyvin heikko happo, ja tasapainoasento on hyvin vasemmalla. Fenoli voi menettää vetyionin, koska muodostuva fenoksidi-ioni on jossain määrin stabiloitunut. Happiatomin negatiivinen varaus on delokalisoitunut renkaan ympärille. Mitä vakaampi ioni on, sitä todennäköisemmin se muodostuu. Yksi happiatomin yksinäisistä pareista on päällekkäin bentseenirenkaan delokalisoituneiden elektronien kanssa.
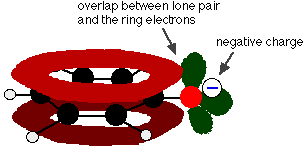
Tämä päällekkäisyys johtaa delokalisaatioon, joka ulottuu renkaasta ulos happiatomin yli. Tämän seurauksena negatiivinen varaus ei ole enää kokonaan paikallistettu hapelle, vaan se on hajaantunut koko ionin ympärille.
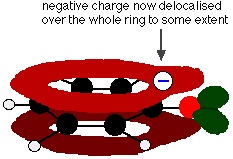
Varauksen hajaantuminen tekee ionista vakaamman kuin se olisi, jos kaikki varaus olisi jäänyt hapelle. Happi on kuitenkin ionin elektronegatiivisin alkuaine, ja delokalisoituneet elektronit vetäytyvät sitä kohti. Tämä tarkoittaa, että hapen ympärillä on edelleen paljon varausta, joka pyrkii vetämään vetyionin takaisin. Siksi fenoli on vain hyvin heikko happo.
Miksi fenoli on paljon vahvempi happo kuin sykloheksanoli? Vastataksemme tähän kysymykseen meidän on arvioitava tapaa, jolla happisubstituentti vuorovaikuttaa bentseenirenkaan kanssa. Kuten aiemmassa elektrofiilisten aromaattisten substituutioreaktioiden käsittelyssä todettiin, happisubstituentti lisää renkaan reaktiivisuutta ja suosii elektrofiilihyökkäystä orto- ja para-kohdissa. Ehdotettiin, että hapen sitoutumattoman elektroniparin resonanssidelokalisaatio aromaattisen renkaan pi-elektronijärjestelmään on vastuussa tästä substituenttivaikutuksesta. Samanlainen joukko fenolaattianionin konjugaattiemäksen resonanssirakenteita esiintyy fenolirakenteiden alapuolella.
Resonanssistabilisaatio näissä kahdessa tapauksessa on hyvin erilainen. Resonanssin tärkeä periaate on, että varausten erottuminen vähentää kanonisten tekijöiden merkitystä resonanssihybridissä ja vähentää kokonaisstabilisaatiota. Kaikki fenolihybridiin vaikuttavat rakenteet kärsivät varausten erottumisesta, mikä johtaa tämän yhdisteen hyvin vaatimattomaan stabiloitumiseen. Toisaalta fenolaattianioni on jo valmiiksi varattu, ja kanoniset osatekijät vaikuttavat varauksen hajauttamiseen, mikä johtaa tämän lajin huomattavaan stabiloitumiseen. Yksinkertaisten alkoholien konjugaattiemäkset eivät stabiloidu varauksen delokalisaation avulla, joten näiden yhdisteiden happamuus on samanlainen kuin vedellä. Oikealla on esitetty energiadiagrammi, joka osoittaa resonanssin vaikutuksen sykloheksanolin ja fenolin happamuuteen. Koska fenolaattikonjugaattiemäksen resonanssistabilointi on paljon suurempi kuin itse fenolin stabilointi, fenolin happamuus suhteessa sykloheksanoliin kasvaa. Tukea sille, että fenolaatin negatiivinen varaus on delokalisoitunut bentseenirenkaan orto- ja para-hiilille, saadaan elektronia vetävien substituenttien vaikutuksesta näissä paikoissa.

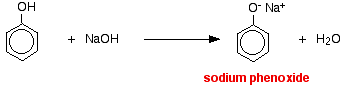
Tässä reaktiossa vetyionin on poistanut vahvasti emäksinen hydroksidi-ioni natriumhydroksidiliuoksessa.
Hapot reagoivat reaktiivisempien metallien kanssa muodostaen vetykaasua. Fenoli ei ole poikkeus – ainoa ero on hidas reaktio, koska fenoli on niin heikko happo. Fenolia lämmitetään kuivassa putkessa, kunnes se on sulaa, ja siihen lisätään pieni pala natriumia. Vetykaasun vapautuessa tapahtuu jonkin verran poreilua. Putkeen jäävä seos sisältää natriumfenoksidia.