Pomocí zakřivených šipek
Nyní se vrátíme k našemu starému známému \(CH_3CNO\), který jsme si představili, když jsme poprvé mluvili o rezonančních strukturách. Tuto sloučeninu použijeme k další ilustraci toho, jak se pohyblivé elektrony „tlačí“, aby se dostaly z jedné rezonanční struktury do druhé.
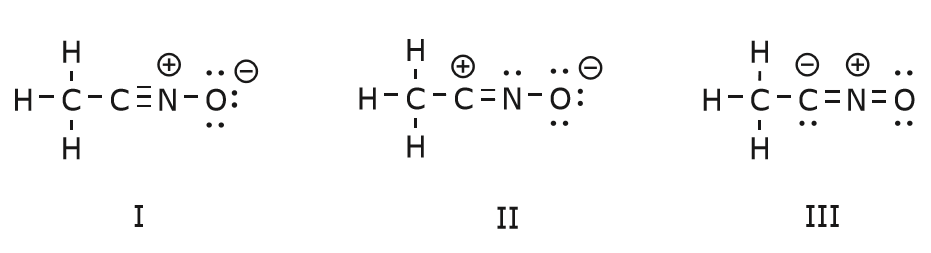
Pohyb elektronů, který probíhá, aby se ze struktury I dostaly do struktury II, začíná trojnou vazbou mezi uhlíkem a dusíkem. Přesuneme jednu ze dvou vazeb \(\pi\), které tvoří součást trojné vazby, směrem ke kladnému náboji na dusíku, jak je znázorněno na obrázku:
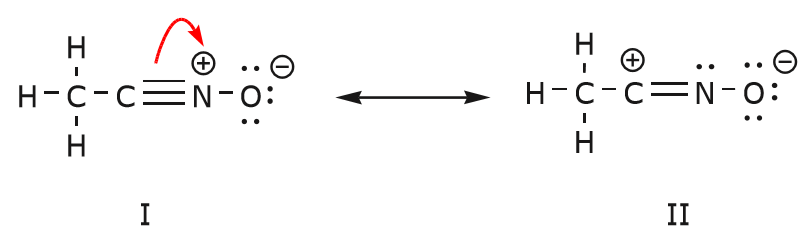
Při tomto postupu věnujeme velkou pozornost novému stavu dotčených atomů a provedeme všechny nezbytné úpravy nábojů, vazeb a nesdílených elektronů, abychom zachovali platnost výsledných vzorců. V tomto případě například uhlík, který tvoří součást trojné vazby ve struktuře I, musí ve struktuře II získat kladný náboj, protože ztratil jeden elektron. Dusík je nyní naopak neutrální, protože získal jeden elektron a tvoří tři vazby místo čtyř.
Ze struktury I do struktury III můžeme také dospět posunutím elektronů následujícím způsobem. Šipky byly v tomto příkladu očíslovány, aby bylo zřejmé, který pohyb začíná jako první, ale to není součástí konvencí používaných ve formalismu zakřivených šipek.
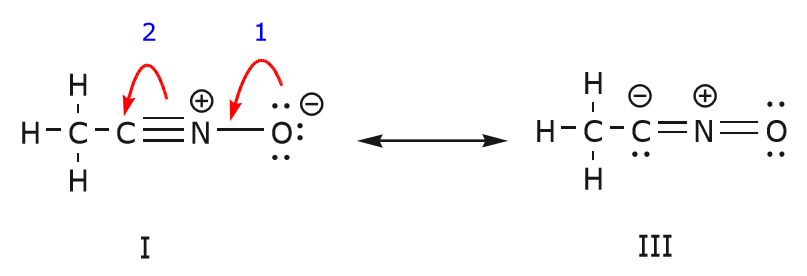
Pokud přesuneme pár nesdílených elektronů z kyslíku směrem k atomu dusíku, jak je znázorněno v kroku 1, jsme nuceni vytlačit elektrony z dusíku směrem k uhlíku, jak je znázorněno v kroku 2. Jinak bychom skončili s dusíkem s 5 vazbami, což je nemožné, i když jen na okamžik. Opět si všimněte, že v kroku 1 šipka vychází z nesdíleného elektronového páru z kyslíku a pohybuje se směrem ke kladnému náboji na dusíku. Mezi dusíkem a kyslíkem vzniká nová vazba \(\pi\). Současně se elektrony \(\pi\), které byly v kroku 2 přesunuty směrem k uhlíku, stanou párem nesdílených elektronů ve struktuře III. Nakonec se změní i hybridizační stav některých atomů. Například atom uhlíku ve struktuře I je sp hybridizovaný, ale ve struktuře III je \(sp^3\) hybridizovaný.
Možná si budete chtít ještě chvíli pohrát a zjistit, zda můžete dospět ze struktury II do struktury III atd. Upozorňujeme však, že někdy je to složitější, než se může na první pohled zdát.
Další pravidla pro přesun elektronů pro zápis rezonančních struktur:
- Elektronové páry se mohou přesouvat pouze do sousedních pozic. Sousedními pozicemi se rozumí sousední atomy a/nebo vazby.
- Lewisovy struktury, které vzniknou přesunem elektronů, musí být platné a musí obsahovat stejný čistý náboj jako všechny ostatní rezonanční struktury.
Následující příklad ilustruje, jak lze přesunout osamělý pár elektronů z uhlíku a vytvořit novou vazbu \(\pi\) se sousedním uhlíkem a jak lze přesunout elektrony \(\pi\) mezi uhlíkem a kyslíkem a vytvořit tak pár nesdílených elektronů na kyslíku. V žádném z těchto příkladů nebylo porušeno žádné z předchozích pravidel.
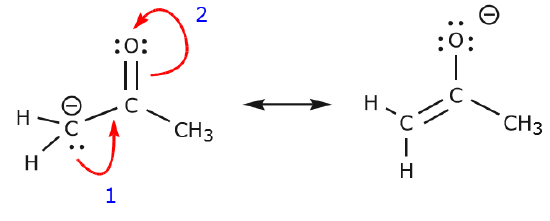
Nyní se podívejme na několik příkladů, JAK NEPŘESOUVAT ELEKTRONY. Na stejném příkladu, ale s pohybem elektronů jiným způsobem, si ukážeme, jak by takový pohyb vedl k neplatným Lewisovým vzorcům, a proto je nepřípustný. Nejenže přesouváme elektrony nesprávným směrem (od elektronegativnějšího atomu), ale výsledná struktura porušuje několik konvencí. Za prvé, centrální uhlík má pět vazeb, a proto porušuje pravidlo oktetu. Za druhé, celkový náboj druhé struktury se liší od první. Abychom se vyhnuli uhlíku s pěti vazbami, museli bychom zničit jednu z jednoduchých vazeb C-C, čímž bychom zničili molekulovou kostru.
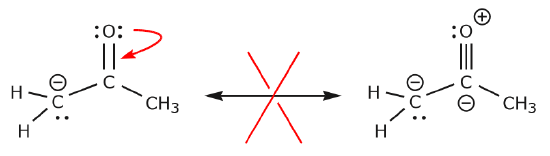
V níže uvedeném příkladu se elektrony přesouvají směrem k oblasti s vysokou elektronovou hustotou (záporný náboj), nikoli ke kladnému náboji. Kromě toho je ve výsledné struktuře porušeno pravidlo oktetu pro uhlík, který sdílí více než osm elektronů.
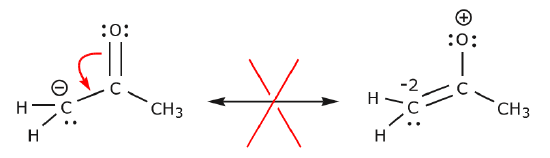
Další příklady dále ilustrují pravidla, o kterých jsme hovořili.
(a) Nesdílené elektronové páry (osamělé páry) nacházející se na daném atomu se mohou přesunout na sousední pozici pouze za účelem vytvoření nové vazby \(\pi\) s dalším atomem.
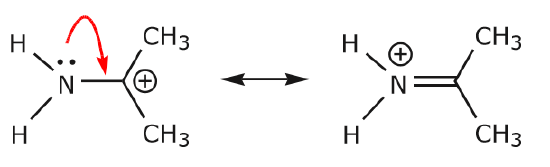
(b) Pokud na dalším atomu (uhlík nahoře) není kladný náboj, budou muset být ostatní elektrony přemístěny, aby bylo zachováno pravidlo oktetu. V rezonančních strukturách jsou to téměř vždy elektrony \(\pi\) a téměř nikdy sigma elektrony.
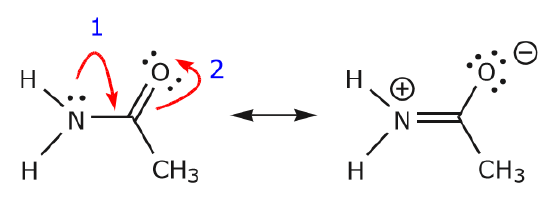
Když se elektrony z osamělého páru dusíku přesunou směrem k sousednímu uhlíku, aby vytvořily novou vazbu \(\pi\), elektrony \(\pi\) tvořící vazbu C=O musí být přemístěny směrem ke kyslíku, aby neskončily s pěti vazbami na centrální uhlík.
c) Jak je vidět výše, elektrony \(\pi\) se mohou přesunout k jednomu ze dvou atomů, které sdílejí, a vytvořit tak nový osamělý pár. Ve výše uvedeném příkladu se elektrony \(\pi\) z vazby C=O přesunuly směrem ke kyslíku a vytvořily nový osamělý pár. Dalším příkladem je:
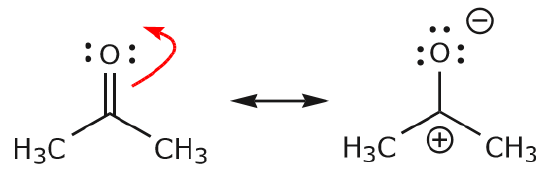
(d) Elektrony \(\pi\) se také mohou přesunout do sousední polohy a vytvořit novou vazbu \(\pi\). Opět je třeba dodržet pravidlo oktetu:
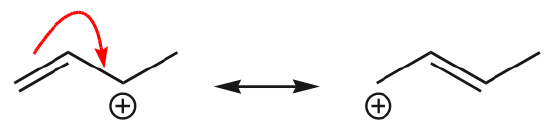
Jeden z nejčastějších příkladů této vlastnosti lze pozorovat při zápisu rezonančních forem pro benzen a podobné kruhy.
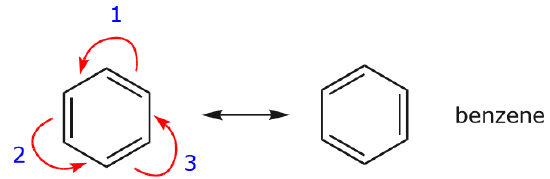
.