Chemiosmoza, siła napędowa protonów i fosforylacja oksydacyjna
W każdym przeniesieniu elektronu przez ETS, elektron traci energię, ale przy niektórych przeniesieniach, energia jest przechowywana jako energia potencjalna przez użycie jej do przepompowania jonów wodoru (H+) przez błonę. W komórkach prokariotycznych H+ są pompowane na zewnątrz błony cytoplazmatycznej (zwanej przestrzenią peryplazmatyczną u bakterii gram-ujemnych i gram-dodatnich), a w komórkach eukariotycznych są pompowane z macierzy mitochondrialnej przez wewnętrzną błonę mitochondrialną do przestrzeni międzybłonowej. Nierównomierne rozmieszczenie H+ w błonie powoduje powstanie gradientu elektrochemicznego, ponieważ jony H+ są naładowane dodatnio (elektrycznie), a ich stężenie jest wyższe (chemicznie) po jednej stronie błony. Ten gradient elektrochemiczny utworzony przez nagromadzenie H+ (znanego również jako proton) po jednej stronie błony w porównaniu z drugą jest określany jako siła napędowa protonu (PMF). Ponieważ zaangażowanymi jonami są H+, tworzy się również gradient pH, przy czym strona błony o wyższym stężeniu H+ jest bardziej kwaśna. Poza wykorzystaniem PMF do wytwarzania ATP, jak omówiono w tym rozdziale, PMF może być również wykorzystywany do napędzania innych energetycznie niekorzystnych procesów, w tym transportu składników odżywczych i rotacji flagelli w celu motoryki.
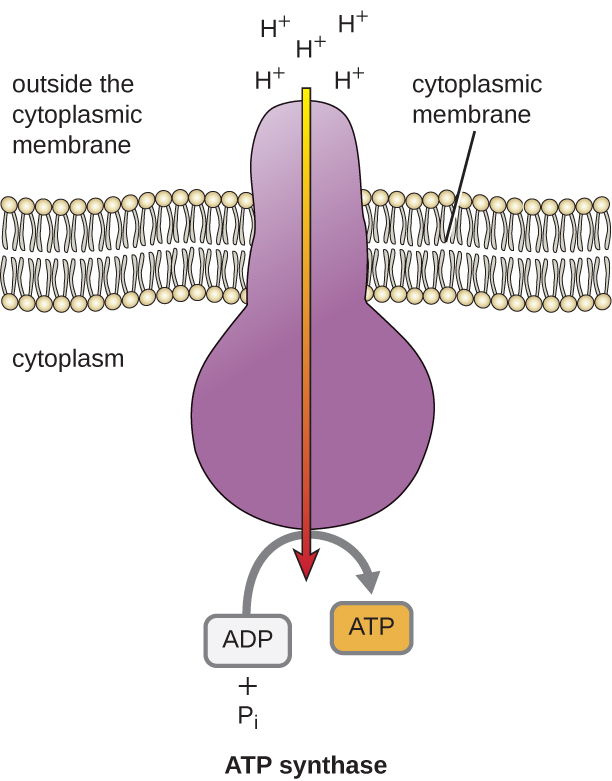
Energia potencjalna tego gradientu elektrochemicznego generowanego przez ETS powoduje dyfuzję H+ przez błonę (błonę plazmatyczną w komórkach prokariotycznych i błonę wewnętrzną w mitochondriach w komórkach eukariotycznych). Ten przepływ jonów wodorowych przez błonę, zwany chemiosmozą, musi zachodzić przez kanał w błonie za pośrednictwem związanego z błoną kompleksu enzymatycznego zwanego syntazą ATP (rysunek \). Tendencja do przemieszczania się w ten sposób jest jak woda zgromadzona po jednej stronie tamy, przemieszczająca się przez tamę po jej otwarciu. Syntaza ATP (jak połączenie wlotu i generatora tamy hydroelektrycznej) jest złożonym białkiem, które działa jak maleńki generator, obracając się siłą dyfundujących przez enzym H+, w dół ich gradientu elektrochemicznego od miejsca, gdzie jest wiele wzajemnie odpychających się H+ do miejsca, gdzie jest mniej H+. W komórkach prokariotycznych H+ przepływa z zewnątrz błony cytoplazmatycznej do cytoplazmy, natomiast w mitochondriach eukariotycznych H+ przepływa z przestrzeni międzybłonowej do macierzy mitochondrialnej. Obrót części tej molekularnej maszyny regeneruje ATP z ADP i fosforanu nieorganicznego (Pi) przez fosforylację oksydacyjną, drugi mechanizm wytwarzania ATP, który zbiera energię potencjalną zmagazynowaną w gradiencie elektrochemicznym.
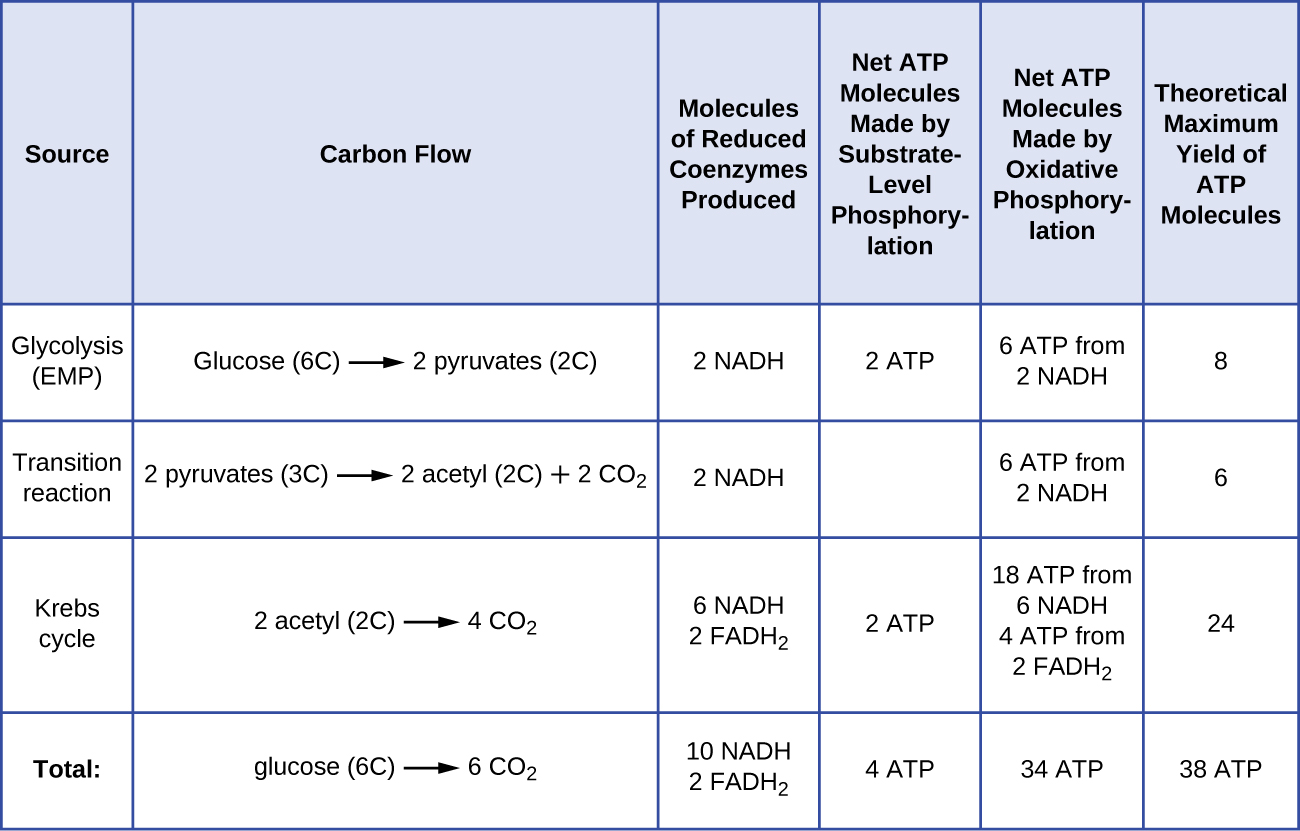
Liczba cząsteczek ATP generowanych z katabolizmu glukozy jest różna. Na przykład, liczba jonów wodorowych, które kompleksy systemu transportu elektronów mogą przepompować przez błonę, jest różna u różnych gatunków organizmów. W oddychaniu tlenowym w mitochondriach, przejście elektronów z jednej cząsteczki NADH generuje wystarczającą siłę napędową protonów do wytworzenia trzech cząsteczek ATP w procesie fosforylacji oksydacyjnej, podczas gdy przejście elektronów z jednej cząsteczki FADH2 generuje wystarczającą siłę napędową protonów do wytworzenia tylko dwóch cząsteczek ATP. Tak więc 10 cząsteczek NADH powstających w glukozie podczas glikolizy, reakcji przemiany i cyklu Krebsa dostarcza energii wystarczającej do wytworzenia 30 cząsteczek ATP, podczas gdy dwie cząsteczki FADH2 powstające w glukozie podczas tych procesów dostarczają energii wystarczającej do wytworzenia czterech cząsteczek ATP. Ogólnie rzecz biorąc, teoretyczna maksymalna wydajność ATP wytworzonego podczas pełnego tlenowego oddychania glukozy wynosi 38 cząsteczek, z czego cztery powstają w wyniku fosforylacji na poziomie substratu, a 34 w wyniku fosforylacji oksydacyjnej (rysunek). W rzeczywistości całkowita wydajność ATP jest zwykle mniejsza, waha się od jednej do 34 cząsteczek ATP, w zależności od tego, czy komórka wykorzystuje oddychanie tlenowe czy beztlenowe; w komórkach eukariotycznych pewna ilość energii jest zużywana na transport półproduktów z cytoplazmy do mitochondriów, co wpływa na wydajność ATP.
Rysunek ™(™PageIndex{2}}) podsumowuje teoretyczną maksymalną wydajność ATP z różnych procesów podczas pełnego tlenowego oddychania jednej cząsteczki glukozy.
Ćwiczenie ™(™PageIndex{1}})
Jakie są funkcje siły napędowej protonów?
.