Chemiosmose, Protonenmotivkraft und oxidative Phosphorylierung
Bei jedem Transfer eines Elektrons durch das ETS verliert das Elektron Energie, aber bei einigen Transfers wird die Energie als potentielle Energie gespeichert, indem sie dazu verwendet wird, Wasserstoffionen (H+) durch eine Membran zu pumpen. In prokaryotischen Zellen wird H+ an die Außenseite der Zytoplasmamembran gepumpt (bei gramnegativen und grampositiven Bakterien als periplasmatischer Raum bezeichnet), und in eukaryotischen Zellen werden sie von der mitochondrialen Matrix über die innere mitochondriale Membran in den Intermembranraum gepumpt. Es kommt zu einer ungleichmäßigen Verteilung von H+ über die Membran, wodurch ein elektrochemisches Gefälle entsteht, da H+-Ionen positiv geladen sind (elektrisch) und auf einer Seite der Membran eine höhere Konzentration (chemisch) vorhanden ist. Dieses elektrochemische Gefälle, das durch die Anhäufung von H+ (auch als Protonen bezeichnet) auf einer Seite der Membran im Vergleich zur anderen Seite entsteht, wird als Protonenmotivkraft (PMF) bezeichnet. Da es sich bei den beteiligten Ionen um H+ handelt, entsteht auch ein pH-Gradient, wobei die Seite der Membran, die die höhere H+-Konzentration aufweist, saurer ist. Neben der Verwendung der PMF zur Herstellung von ATP, wie in diesem Kapitel erörtert, kann die PMF auch dazu verwendet werden, andere energetisch ungünstige Prozesse anzutreiben, einschließlich des Nährstofftransports und der Rotation der Geißeln für die Motilität.
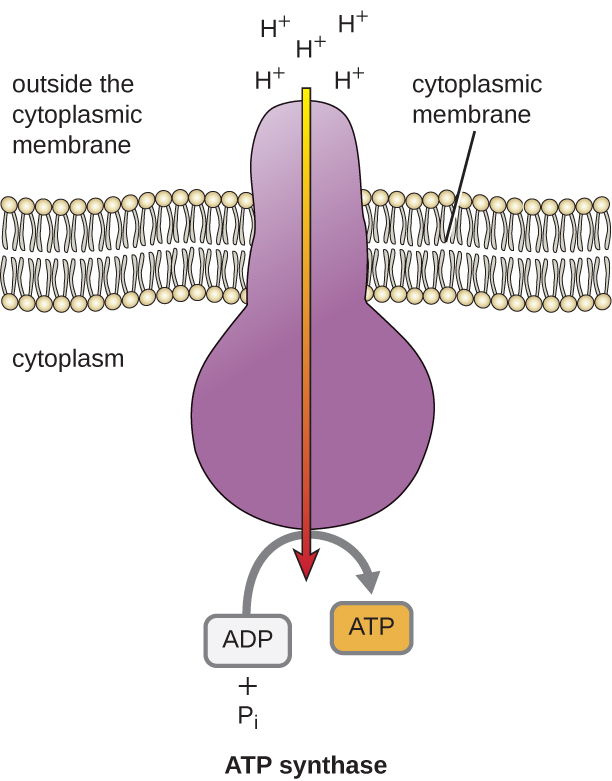
Die potentielle Energie dieses elektrochemischen Gradienten, der durch die ETS erzeugt wird, bewirkt, dass H+ durch eine Membran diffundiert (die Plasmamembran in prokaryotischen Zellen und die innere Membran in Mitochondrien in eukaryotischen Zellen). Dieser Fluss von Wasserstoffionen durch die Membran, Chemiosmose genannt, muss durch einen Kanal in der Membran über einen membrangebundenen Enzymkomplex namens ATP-Synthase erfolgen (Abbildung \(\PageIndex{1}\)). Die Tendenz zur Bewegung auf diese Weise ist vergleichbar mit dem Wasser, das sich auf einer Seite eines Dammes angesammelt hat und durch den Damm fließt, wenn er geöffnet wird. Die ATP-Synthase (wie eine Kombination aus Einlass und Generator eines Staudamms) ist ein komplexes Protein, das als winziger Generator fungiert und sich durch die Kraft der H+, die durch das Enzym diffundieren, den elektrochemischen Gradienten hinunterbewegt, von dort, wo es viele sich gegenseitig abstoßende H+ gibt, zu dort, wo es weniger H+ gibt. In prokaryotischen Zellen fließt H+ von der Außenseite der Zytoplasmamembran in das Zytoplasma, während in eukaryotischen Mitochondrien H+ vom Intermembranraum in die mitochondriale Matrix fließt. Die Drehung der Teile dieser molekularen Maschine regeneriert ATP aus ADP und anorganischem Phosphat (Pi) durch oxidative Phosphorylierung, einen zweiten Mechanismus zur Herstellung von ATP, der die in einem elektrochemischen Gradienten gespeicherte potenzielle Energie nutzt.
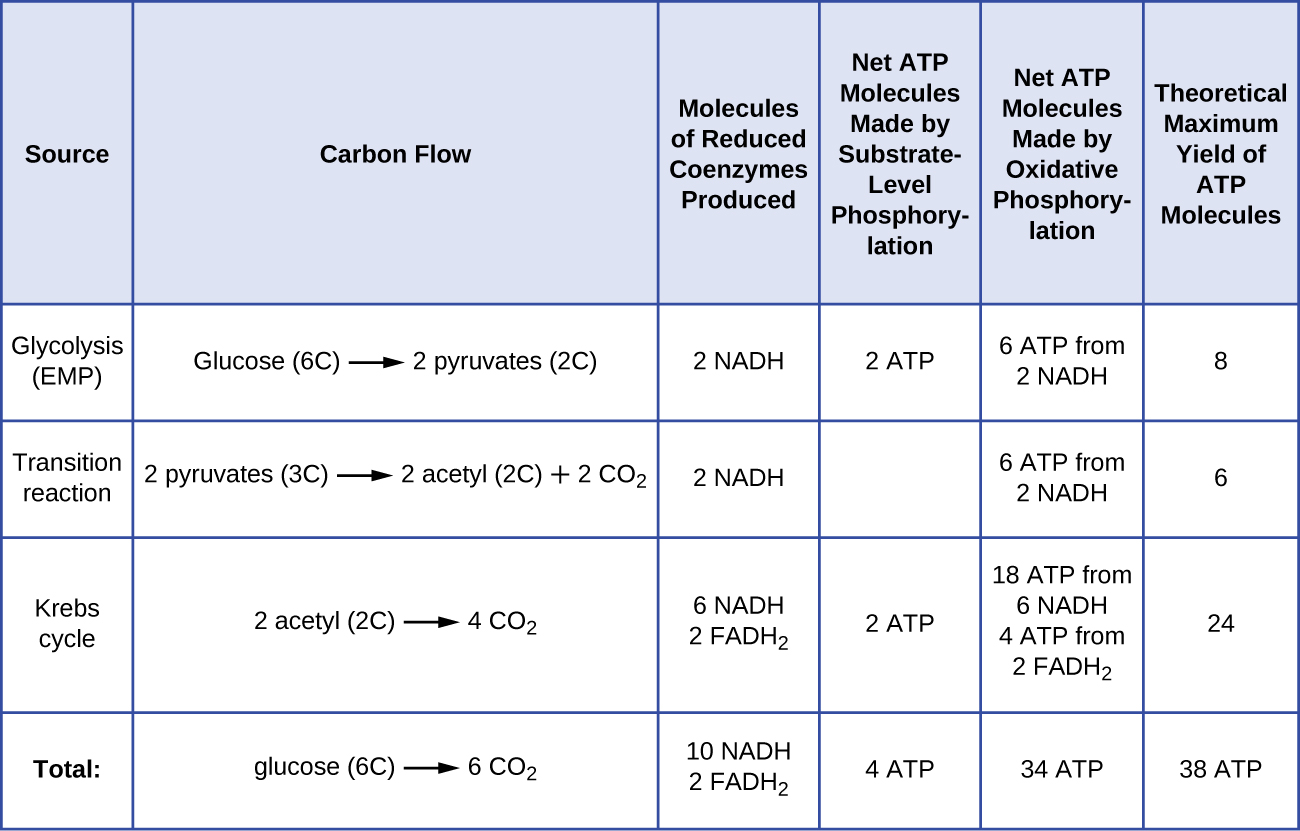
Die Anzahl der ATP-Moleküle, die beim Abbau von Glukose entstehen, variiert. So variiert beispielsweise die Anzahl der Wasserstoffionen, die die Komplexe des Elektronentransportsystems durch die Membran pumpen können, zwischen verschiedenen Organismenarten. Bei der aeroben Atmung in den Mitochondrien erzeugt der Durchgang von Elektronen aus einem Molekül NADH genug Protonenmotivkraft, um drei ATP-Moleküle durch oxidative Phosphorylierung zu erzeugen, während der Durchgang von Elektronen aus einem Molekül FADH2 genug Protonenmotivkraft erzeugt, um nur zwei ATP-Moleküle zu erzeugen. Die 10 NADH-Moleküle, die bei der Glykolyse, der Übergangsreaktion und dem Krebs-Zyklus pro Glukose entstehen, liefern also genug Energie, um 30 ATP-Moleküle herzustellen, während die zwei FADH2-Moleküle, die bei diesen Prozessen pro Glukose entstehen, genug Energie liefern, um vier ATP-Moleküle herzustellen. Insgesamt beträgt die theoretische Maximalausbeute an ATP, das während der vollständigen aeroben Atmung von Glukose gebildet wird, 38 Moleküle, von denen vier durch Phosphorylierung auf Substratebene und 34 durch oxidative Phosphorylierung gebildet werden (Abbildung \(\PageIndex{2}\)). In Wirklichkeit ist die Gesamtausbeute an ATP in der Regel geringer und liegt zwischen einem und 34 ATP-Molekülen, je nachdem, ob die Zelle aerobe oder anaerobe Atmung betreibt; in eukaryotischen Zellen wird etwas Energie für den Transport von Zwischenprodukten aus dem Zytoplasma in die Mitochondrien aufgewendet, was die ATP-Ausbeute beeinträchtigt.
Abbildung \(\PageIndex{2}\) fasst die theoretischen Maximalerträge von ATP aus verschiedenen Prozessen während der vollständigen aeroben Atmung eines Glukosemoleküls zusammen.
Übung \(\PageIndex{1}\)
Was sind die Funktionen der Protonenmotivkraft?