Chemiosmose, force motrice du proton, et phosphorylation oxydative
Dans chaque transfert d’un électron à travers le STE, l’électron perd de l’énergie, mais avec certains transferts, l’énergie est stockée sous forme d’énergie potentielle en l’utilisant pour pomper des ions hydrogène (H+) à travers une membrane. Dans les cellules procaryotes, les H+ sont pompés vers l’extérieur de la membrane cytoplasmique (appelée espace périplasmique chez les bactéries gram-négatives et gram-positives), et dans les cellules eucaryotes, ils sont pompés de la matrice mitochondriale à travers la membrane mitochondriale interne vers l’espace intermembranaire. Il y a une distribution inégale de H+ à travers la membrane qui établit un gradient électrochimique parce que les ions H+ sont chargés positivement (électrique) et qu’il y a une concentration plus élevée (chimique) d’un côté de la membrane. Ce gradient électrochimique formé par l’accumulation de H+ (également appelé proton) d’un côté de la membrane par rapport à l’autre est appelé force motrice protonique (FMP). Comme les ions impliqués sont H+, un gradient de pH est également établi, le côté de la membrane ayant la plus forte concentration de H+ étant plus acide. Au-delà de l’utilisation de la PMF pour fabriquer de l’ATP, comme discuté dans ce chapitre, la PMF peut également être utilisée pour piloter d’autres processus énergétiquement défavorables, notamment le transport des nutriments et la rotation des flagelles pour la motilité.
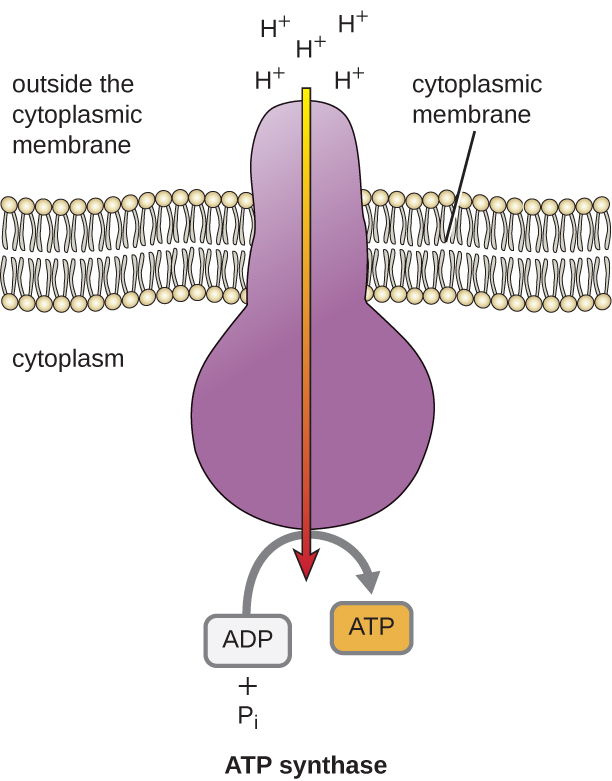
L’énergie potentielle de ce gradient électrochimique généré par l’ETS entraîne la diffusion des H+ à travers une membrane (la membrane plasmique dans les cellules procaryotes et la membrane interne des mitochondries dans les cellules eucaryotes). Ce flux d’ions hydrogène à travers la membrane, appelé chimiosmose, doit se produire à travers un canal dans la membrane via un complexe enzymatique lié à la membrane appelé ATP synthase (Figure \(\PageIndex{1}\)). La tendance à se déplacer de cette manière est comparable à l’eau accumulée sur un côté d’un barrage, qui se déplace à travers le barrage lorsqu’il est ouvert. L’ATP synthase (comme une combinaison de la prise d’eau et du générateur d’un barrage hydroélectrique) est une protéine complexe qui agit comme un minuscule générateur, tournant sous l’effet de la force des H+ diffusant à travers l’enzyme, le long de leur gradient électrochimique, de l’endroit où il y a beaucoup de H+ se repoussant mutuellement à celui où il y a moins de H+. Dans les cellules procaryotes, le H+ circule de l’extérieur de la membrane cytoplasmique vers le cytoplasme, tandis que dans les mitochondries eucaryotes, le H+ circule de l’espace intermembranaire vers la matrice mitochondriale. La rotation des pièces de cette machine moléculaire régénère l’ATP à partir de l’ADP et du phosphate inorganique (Pi) par phosphorylation oxydative, un second mécanisme de fabrication de l’ATP qui récolte l’énergie potentielle stockée dans un gradient électrochimique.
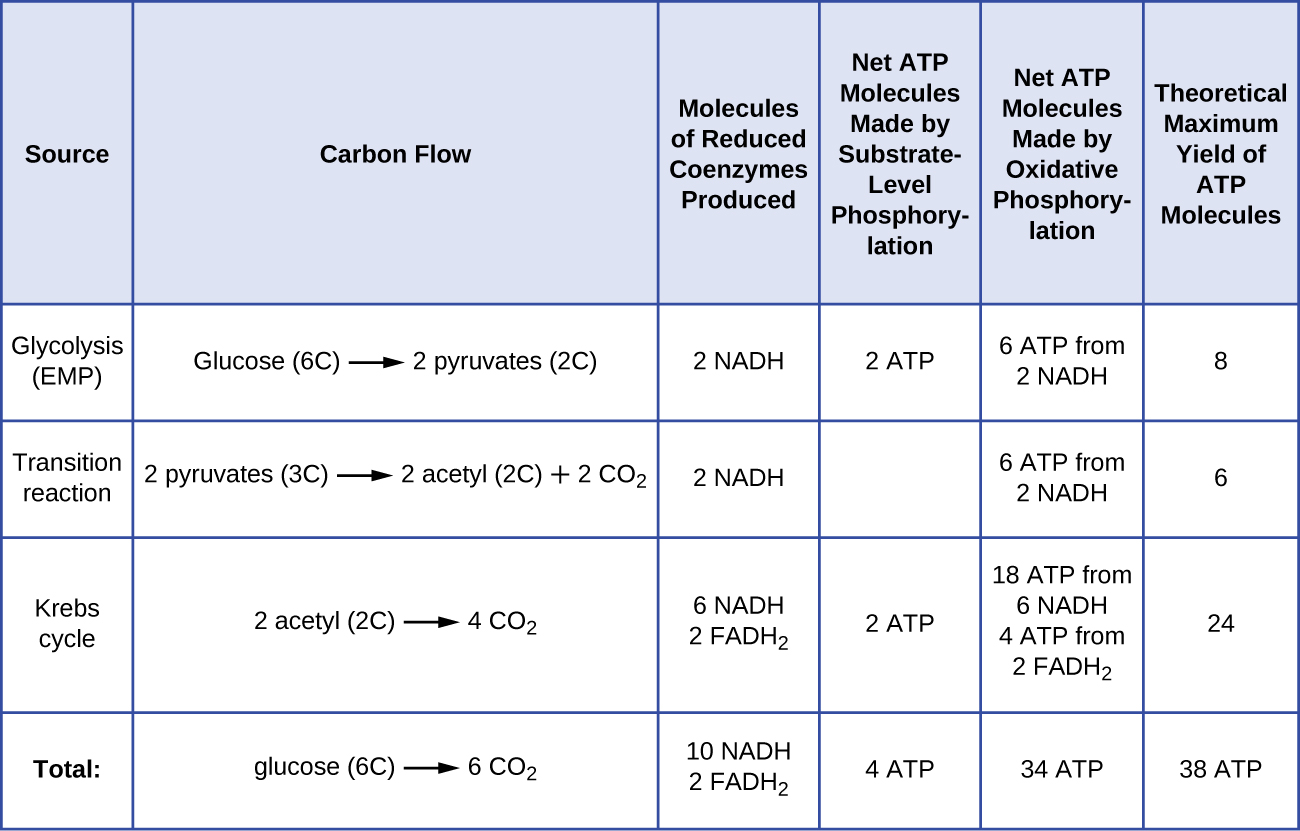
Le nombre de molécules d’ATP générées par le catabolisme du glucose varie. Ainsi, le nombre d’ions hydrogène que les complexes du système de transport d’électrons peuvent pomper à travers la membrane varie entre les différentes espèces d’organismes. Lors de la respiration aérobie dans les mitochondries, le passage des électrons d’une molécule de NADH génère une force motrice protonique suffisante pour produire trois molécules d’ATP par phosphorylation oxydative, tandis que le passage des électrons d’une molécule de FADH2 génère une force motrice protonique suffisante pour produire seulement deux molécules d’ATP. Ainsi, les 10 molécules de NADH fabriquées par glucose au cours de la glycolyse, de la réaction de transition et du cycle de Krebs transportent suffisamment d’énergie pour fabriquer 30 molécules d’ATP, tandis que les deux molécules de FADH2 fabriquées par glucose au cours de ces processus fournissent suffisamment d’énergie pour fabriquer quatre molécules d’ATP. Globalement, le rendement théorique maximal d’ATP produit au cours de la respiration aérobie complète du glucose est de 38 molécules, dont quatre sont produites par phosphorylation au niveau du substrat et 34 par phosphorylation oxydative (figure \(\PageIndex{2}\)). En réalité, le rendement total en ATP est généralement inférieur, allant de une à 34 molécules d’ATP, selon que la cellule utilise la respiration aérobie ou la respiration anaérobie ; dans les cellules eucaryotes, une certaine énergie est dépensée pour transporter les intermédiaires du cytoplasme vers les mitochondries, ce qui affecte le rendement en ATP.
La figure \(\PageIndex{2}\) résume les rendements maximaux théoriques d’ATP de divers processus pendant la respiration aérobie complète d’une molécule de glucose.
Exercice \(\PageIndex{1}\)
Quelles sont les fonctions de la force motrice du proton ?