Using Curved Arrows
ここで、最初に共鳴構造の話をしたときに紹介した旧知の仲である♪ \(CH_3CNO 001) に戻ってみましょう。
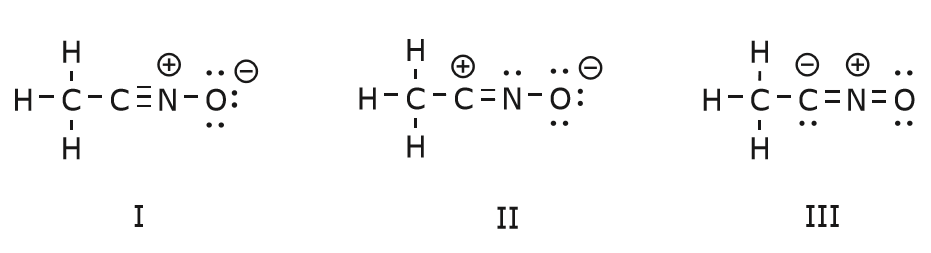
構造 I から構造 II に到達するために起こる電子の移動は、炭素と窒素の間の三重結合から始まります。
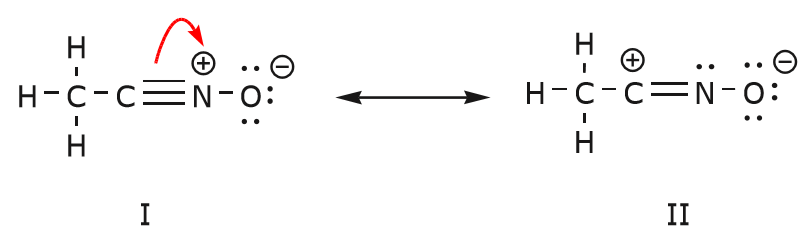
このとき、影響を受ける原子の新しい状態に細心の注意を払い、電荷、結合、共有されていない電子に必要な調整を行い、結果の式の妥当性を維持するようにするのです。 例えばこの場合、構造Iで三重結合の一部を形成していた炭素は、構造IIでは電子を1つ失っているため、正の電荷を持たなければならない。 一方、窒素は電子を1つ得たので中性になり、4つの結合ではなく3つの結合を形成します。
また、次のように電子を押し出すことで、構造Iから構造IIIに到達することができます。 この例では、どの動きが先に始まるかを示すために矢印に番号を振っていますが、これは曲線矢印形式主義で使用される規則の一部ではありません。
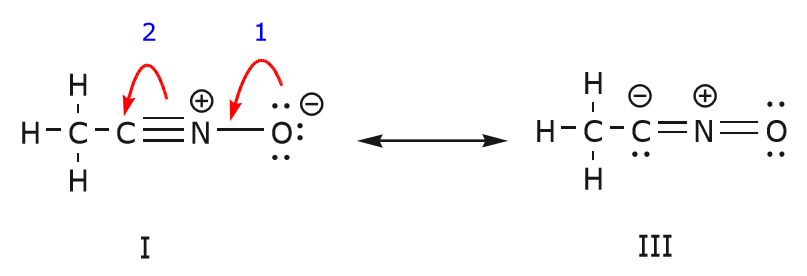
ステップ 1 で示すように、酸素から窒素原子に向かって非共有電子のペアを移動すると、ステップ 2 で示すように窒素から炭素に向かって電子を置換せざるを得ません。 そうしないと、5つの結合を持つ窒素になってしまい、一瞬とはいえ不可能です。 ステップ1では、矢印は酸素の共有されていない電子対から出発して、窒素の正電荷に向かって移動していることに注意してください。 窒素と酸素の間に新たな結合が形成される。 同時に、ステップ2で炭素の方に移動していた電子は、構造IIIで非共有電子のペアになります。 最後に、いくつかの原子の混成状態も変化する。 例えば、構造Iの炭素原子はsp hybridizedですが、構造IIIでは \(sp^3) hybridizedになります。
もう少し遊んでみて、構造IIから構造IIIにたどり着けるかどうかなどを見てみるとよいかもしれません。
Additional rules for moving electrons to write Resonance Structures:
- Electron pairs can only move to adjacent positions.ただし、電子ペアは隣接する位置にしか移動できません。
- 電子を移動させた結果のルイス構造は有効でなければならず、他のすべての共鳴構造と同じ正味電荷を含まなければなりません。
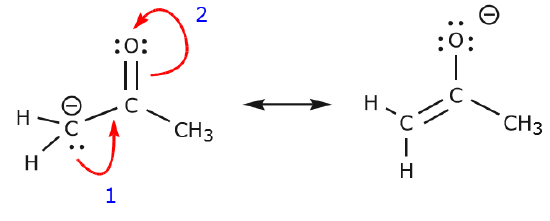
次の例は、炭素の孤立電子対を移動して、隣接する炭素に新しい(⾵印)結合を作ることができ、炭素と酸素の間の(⾵印) 電子を移動して酸素上の非共有電子対にできるかを説明しています。
では、「電子を動かしてはいけない例」をいくつか見てみましょう。 同じ例を使っていますが、電子を別の方法で動かすと、そのような動きが無効なルイス式になり、したがって容認できないことを説明しています。 電子を間違った方向(より電気陰性度の高い原子から離れる方向)に動かしているだけでなく、結果として得られる構造もいくつかの規則に違反しています。 まず、中心の炭素は5つの結合を持つため、オクテット則に違反する。 次に、2番目の構造の全体の電荷は、1番目の構造とは異なっている。 5 つの結合を持つ炭素を避けるためには、C-C 単結合の 1 つを破壊しなければならず、その過程で分子骨格が破壊されます。
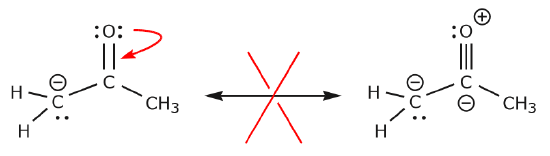
以下の例では、電子は正の電荷に向かうのではなく、高い電子密度(負の電荷)の領域に移動しているのです。 さらに、結果として得られる構造では、炭素は 8 個以上の電子を共有しており、オクテット ルールに違反しています。
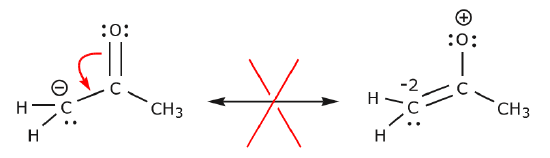
追加の例では、これまで話してきたルールをさらに説明します。
(a) ある原子にある非共有電子対 (ローンペア) は、次の原子に新しい \pi 式結合を作るためにのみ隣接する位置に移動できます。
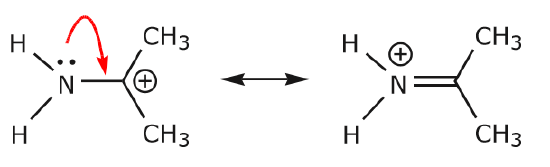
(b) 次の原子 (上の炭素) に正の電荷がなければ、他の電子は octet 規則を保つために移動しなければならないでしょう。
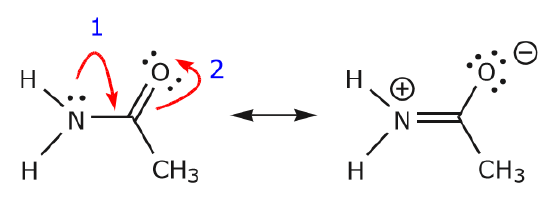
As the electrons from the nitrogen lone pair move towards the neighboring carbon to make a new \pi bond, the C=O bond making the \pi electrons towards the oxygen to avoid up to five bonds to the central carbon.共鳴構造では、ほとんどいつもΣ電子であり、ほとんどありえない。
c) 上で見たように、(Ⓐ)電子は共有する2つの原子のうちの1つに向かって移動し、新しいローンペアを形成することができます。 上の例では、C=O結合から出た(arrange)電子が酸素の方に移動して、新しいローン・ペアを形成しています。 他にも、
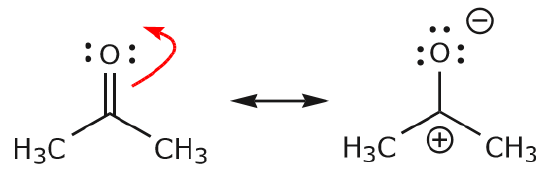
(d) 電子も隣の位置に移動して、新たな♪(♪)結合を作ることができるのです。
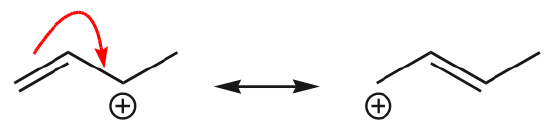
この特徴の最も一般的な例は、ベンゼンや同様の環の共鳴形を書くときに観察されます。