
ALLISON SIEBECKER, ND, MSOM, LAC
STEVEN SANDBURG-LEWIS, ND, DHANP
我々の大きな目標の1つは、過敏性腸症候群(IBS)に有効な治療について医者を啓蒙することです。 前回は小腸内細菌過繁殖(SIBO)について、IBSの主な原因であるこの菌の基本を説明しました。 今回はその続編として、診断や検査の解釈の細かなポイント(症例を交えて)、食事療法、プロバイオティクス、修復、予防について解説します。
SIBOの診断
SIBOを診断できる検査は、培養による内視鏡と水素・メタン呼気試験の2つです。 便検査や尿中有機酸検査では、SIBOの診断はできない。 SIBOを評価する最も一般的な方法は、最も正確で詳細な情報が得られ、かつ非侵襲的で安価な水素/メタン呼気検査である。 これに対し、内視鏡検査は、直接測定が可能な反面、いくつかの制限があります。 1 遠位型SIBOが最も一般的であると考えられているため、これは大きな制約となります。2 さらに、ほとんどの嫌気性菌は培養できないため、培養ではSIBOに存在する嫌気性菌を正確に反映できません3。 同様に、尿中のヒプラート、p-ヒドロキシ安息香酸、およびその他の細菌代謝物の存在によって間接的に細菌の過剰増殖を示すことができる有機酸試験も、過剰増殖の場所を遠位小腸と近位大腸で区別することはできず、呼気試験で得られる詳細も提供できません4。
細菌の過剰増殖は、過剰な量の水素および/またはメタンガスを発生させる。7 呼気検査はこれらのガスを測定するため、間接検査となるが、どのガスが存在するか、またSIBOの部位と重症度を特定することができる。 この情報は、治療や予後の判定に不可欠な場合が多いのです。
空腹時のベースライン検体を採取した後、非吸収性の合成糖であるラクチュロースの溶液を摂取し、細菌発酵の基質とするものである。 ラクチュロースを消化する酵素を産生するのは、ヒトではなく細菌のみである。 ラクチュロースは小腸を通過するのに約2時間かかる。 この間、15~20分ごとに呼気の連続検体を採取し、小腸の細菌量を、3時間目には大腸の細菌量を反映させる。 2 グルコースも検査基質として使用されることがありますが、近位小腸での吸収が速いため、遠位SIBOを特定することはできません。 検査の準備は検査室によって異なりますが、一般的な準備食は白米、魚/鶏肉/肉、卵、ハードチーズ、透明なビーフまたはチキンスープ(ボーンブロスやブイヨンではない)、油、塩、コショウに限定されています。 予備食の目的は、発酵性食品の存在を減らすことで、検査液に対する明確な反応を得ることである。 場合によっては、ベースラインのガスを十分に陰性化するために2日間の準備食を必要とすることがある。 抗生物質を継続的に服用している患者でSIBOが疑われる場合、抗生物質を中止することなく初回の呼気検査を実施することができる。 (www.siboinfo.com/testing を参照。) 測定器が異なるため、すべての検査機関がメタンを検査するわけではありません。 メタンと水素では治療法が異なるため、メタン検査は重要です。
検査の解釈は医師によって大きく異なる場合があります。 ある医師・研究所では陽性とされた患者が、別の医師・研究所では陰性とされる可能性が非常に高いのです。 機械メーカーが提示する陽性の基準は以下の通りです。8
– ラクチュロース摂取後120分以内に、水素発生量が20ppm以上、以前の最低値より上昇
– 摂取後120分以内に、メタン発生量が12ppm以上、以前の最低値より上昇。 lactulose
– ラクチュロース摂取後120分以内に、水素とメタン生成の合計が15ppm以上となり、最低先行値より上昇すること
QuinTronが提供する正のppmレベル以上の気体の絶対レベルがあることを発見しました。 ベースラインまたはその前の最低値から上昇することなく、臨床的なSIBOとよく相関する。 これは特にメタンガスに当てはまり、ベースラインの上昇(> 12 ppm)が検査期間中、上昇したままというパターンがある(図1)。 このような場合、メタンガスは5ppmしか上昇しないこともあるが、ppmレベルは常に陽性カットオフを上回っている。 ベースライン検体(ラクチュロース摂取前)の水素またはメタンの上昇の解釈は議論の余地があるが、ベースライン後にガスレベルが低下し、最初の2時間は減少し続けるか低いままであり、不適切な準備食を示す場合を除き(図3および3.)、高いベースライン値を陽性検査とみなすことが望ましい(図2.5)。
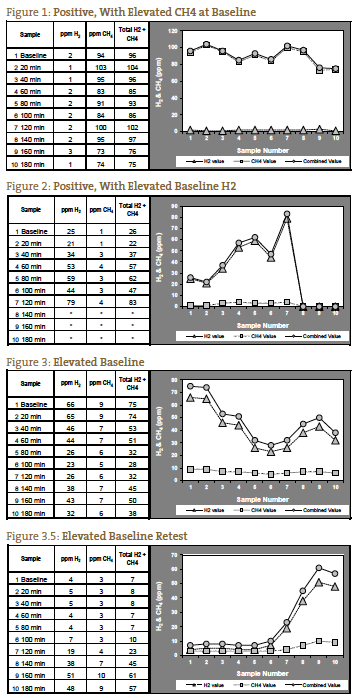
SIBOの古典的な陽性は、最初のピークがSIBOを、第2のピークが通常の豊富な大腸菌を表す、ダブルピークと考えられてきた(図4)。 私たちの経験では、これはまれな症例である。
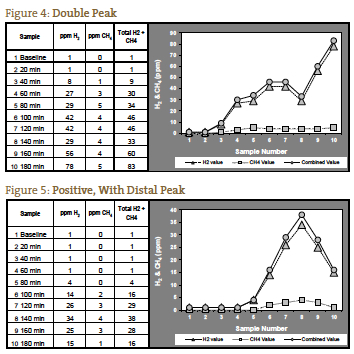
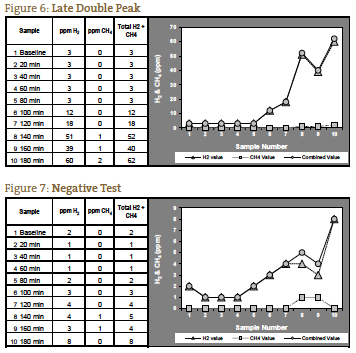
測定ガスが120分を過ぎても上昇しない場合は、通過時間が長くなっている可能性があり、これは重度の便秘の患者さんで見受けられます。 このような便秘型SIBOの症状像が予想される患者さんでは、140分後の有意な上昇は陽性と解釈してよいでしょう(図6)。 図7は陰性である。グラフの左側のスケールは、ガス濃度が低いことを反映して小さくなっていることに注意。 図 1 から図 7 は NCNM の研究室から提供された事例である。
呼吸テストは、子供が収集装置に息を吹き込む指示に適切に従える限り、小児例で使用することができる。 3歳未満の場合、家庭用キットと採取方法が異なるため、検査はオフィス/ラボで行うのが最適です。 11 ラクチュロースは処方薬であるため、ラクチュロースキットは処方医のみが注文することができます。 これは、すべての穀物、でんぷん質の野菜、乳糖、蜂蜜以外の甘味料を除去することによって、多糖類、オリゴ糖、二糖類を減少させることによって行われる。 豆類はまず排除します。 私たちは、特定炭水化物ダイエット(SCD)またはその亜種である腸と心理症候群ダイエット(GAPS)を中核とした食事に、低FODMAPダイエット(表1)から推奨される果物や野菜を取り入れることが効果的であることを発見しています。 (低FODMAP食は、食品中の発酵性炭水化物のレベルを調査した結果生まれたIBS治療食であり、IBSの成功率は76%である。12 FODMAP食は特にSIBO向けに作られたものではないため、穀物、でんぷん、でんぷん質野菜、ショ糖などの多糖類および二糖類の供給源を排除していない。 SIBOではこれらの多糖類や二糖類を除去することが不可欠です。 SIBOでは、吸収の良い炭水化物、通常は宿主の餌となる食品が、代わりに増加した小腸細菌の餌となり、症状を引き起こし、細菌の増殖を促進する1(図8)
どんな食事も、時間をかけて試行錯誤しながら個別に調整する必要がある。 6275>
低炭水化物ダイエットは体重を減らすダイエットである。 特に、境界型や低体重の人には注意が必要である。 SIBOダイエットが過度の体重減少につながる場合、この食事戦略を変更して、より多くの炭水化物を摂取できるようにする必要がある。 このような状況では、白米、ブドウ糖、その他の炭水化物源とともに、前回の記事で述べた他の3つの治療法のうち1つ以上を検討すべきである。
Probiotics
SIBOでは乳酸菌が培養されており13、細菌過剰を助長することが懸念されるので、Probioticsは議論の多い介入と言える。 特に、遊走運動複合体(MMC)の機能不全による運動量の低下がある場合は、その傾向が顕著である。 この懸念にもかかわらず、SIBOに直接焦点を当てた数少ないプロバイオティクス研究では、Bacillus clausiiの単独投与による除菌率が47%、Lactobacillus casei Shirotaの単独投与による成功率が64%、15 Lactobacillus caseiとL. plantarum、Streptococcus faecalis、Bifidobacter brevisの単独投与による臨床改善率が82%と、良い結果を示しています16。 Lactobacillus johnsoniiを含むプロバイオティックヨーグルトは、4週間の補給でサイトカイン反応を正常化し、SIBOに見られる低悪性度の慢性炎症を軽減した17。私たちは、さまざまな多菌種および単独のプロバイオティック、さらに自家製の無乳糖ヨーグルトや培養野菜を使ってSIBO患者に良い結果を見ている
SIBOにおけるプロバイオティックサプリメントの使用でポイントとなるのが、主成分がプレバイオティックにならないことである。 プレバイオティクスは細菌にとって発酵性の餌であり、SIBO活動中の症状を悪化させ、SIBO後の細菌の増殖を促す可能性があります。 プロバイオティクスサプリメントに含まれる一般的なプレバイオティクスは以下の通りです。 FOS(フラクトオリゴ糖)、MOS(マンナンオリゴ糖)、GOS(ガラクトオリゴ糖)、イヌリン、およびアラビノガラクタン。 プレバイオティクスは、基本成分として使用される少量であれば、個々に耐えられる可能性があります。
腸管透過性
SIBO後の粘膜治癒率を調査した研究では、腸管透過性が、抗生物質の治療成功後4週間で75%~100%で正常化することがわかりました18,19。
粘液性のハーブは、Glycyrrhiza glabra (licorice), Ulmus fulva (slippery elm), Aloe vera, Althea officinalis (marshmallow) など、伝統的に粘膜治癒に用いられていますが、細菌の再繁殖を促すムコ多糖を含むことから、SIBO後の使用は議論の余地があると言われています。 私たちは、コロストラム (2-6 g QD), L- グルタミン (375-1500+ mg QD), 亜鉛カルノシン (75-150 mg QD), ビタミン A と D (しばしばタラ肝油 (1 tbsp QD) として与えられる) などの栄養素を使用してきました。 クルクミン(400mg~3g QD)、レスベラトロール(250mg~2g QD)、グルタチオン、経口リポソーマル(50~425mg QD)またはグルタチオン前駆体N-アセチルシステイン(200~600mg QD。 サプリメントは1~3ヶ月間投与されるが、長期的に継続することもある。 クルクミンとレスベラトロールの高用量は、腸の透過性を高めるメディエーターであるNF-Κβをダウンレギュレートする目的で2週間投与し、その後はより穏やかな維持レベルにします20、21、22
予防
Supplements
塩酸(HCl)23の分泌を促す、塩酸ベータインまたはハーブ苦味サプリメントは、摂取したバクテリアの負荷軽減に用いることができるかもしれません。
食事の間隔
プロキネティック剤(2013年1月の記事で紹介)に加えて、食事の間隔を4~5時間あけ、水以外は摂取しないことで、夜間や食間に小腸内の細菌を遊走運動複合体(MMC)が一掃することができます24。 低炭水化物SIBO食で低血糖が改善されない場合は、この戦略を変更して、より頻繁に食事ができるようにする必要があります。
検査の解釈と治療戦略に関する現在の展望は、1月18~19日にポートランドで開催される2014 SIBOシンポジウムで議論され、ライブおよび録画のウェビナー(www.sibosymposium.com)。
 Allison Siebecker, ND, MSOM, LAcは、National College of Natural Medicine(オレゴン州ポートランド)を卒業し、小腸菌過剰増殖(SIBO)治療を専門に、上級胃腸科の准教授を務めている人物です。 現在、SIBOに関する本を執筆中。 彼女の教育的なSIBOのウェブサイトは、www.siboinfo.com。
Allison Siebecker, ND, MSOM, LAcは、National College of Natural Medicine(オレゴン州ポートランド)を卒業し、小腸菌過剰増殖(SIBO)治療を専門に、上級胃腸科の准教授を務めている人物です。 現在、SIBOに関する本を執筆中。 彼女の教育的なSIBOのウェブサイトは、www.siboinfo.com。
 Steven Sandberg-Lewis, ND, DHANP, 1978年にNational University of Natural Medicine (NUNM) を卒業して以来、自然療法医として活動しています。 1985年からはNUNMの教授として、様々なコースを教えていますが、主に消化器病学とGI physical medicineに重点を置いています。 特に、博士課程の学生の間では、彼のクリニックローテートは人気がある。 6275>
Steven Sandberg-Lewis, ND, DHANP, 1978年にNational University of Natural Medicine (NUNM) を卒業して以来、自然療法医として活動しています。 1985年からはNUNMの教授として、様々なコースを教えていますが、主に消化器病学とGI physical medicineに重点を置いています。 特に、博士課程の学生の間では、彼のクリニックローテートは人気がある。 6275>
機能性医学セミナーでの国際的な人気講師であり、ウェビナーを開催し、NDNRとタウンゼント・レターに記事を書き、消化器の健康と病気の問題について頻繁にインタビューを受けている。 著書に『Functional Gastroenterology』(医学書院)がある。 Assessing and Addressing the Causes of Functional Digestive Disorders, Second Edition, 2017」(amazon.co.jp)で販売されている。 2010年にはNUNMにSIBOセンターを共同設立し、全米で4つしかない小腸菌過繁殖の診断、治療、教育、研究センターの1つとなっている。 2014年、ポートランド月刊誌の年間医療問題で「トップドック」の一人に選ばれ、2015年にはOANP/NUNMの殿堂入りを果たした。
消化器内科の中でも、炎症性腸疾患(顕微鏡的大腸炎を含む)、過敏性腸症候群(感染後IBSを含む)、小腸細菌過剰増殖(SIBO)、食道ヘルニア、胃食道逆流症および胆道逆流症(GERD)、胆道ジスキニー、慢性状態の吐き気・嘔吐について特に関心と専門性を持っています。
サンドバーグ-ルイス博士に紹介される患者の多くは、診断や効果的な解決を拒んできた消化器系の疾患を持っています。 これらの患者はしばしば、以前に受けた治療のコースの代わりに、自然療法による治療の選択肢を望んでいます。 彼は消化管の病気を理解するだけでなく、機能を評価することができ、消化器系のバランスを取り戻すための治療法を見つけることがよくあります。 趣味はマンドリン、ギター、声楽、クロスカントリースキー、執筆、講演など。
1. Lin HC. 小腸菌の過繁殖:過敏性腸症候群を理解するためのフレームワーク。 JAMA. 2004;292(7):852-858.
2. Shah ED, Basseri RJ, Chong K, Pimentel M. Abnormal breath testing in IBS: a meta-analysis.IBS の呼気検査異常のメタ分析。 小腸の細菌過繁殖の診断テストの系統的レビュー。 また、”li “は “li “であり、”li “は “li “である。 尿中有機酸の臨床応用. 第2部. ディスバイオーシスマーカー。 2008;13(4):292-306.
5.Altern Med Rev. Riordan SM, Kim R. Bacterial overgrowth as a cause of irritable bowel syndrome(過敏性腸症候群の原因としての細菌の過剰繁殖). Curr Opin Gastroenterol。 2006;22(6):669-673.
6. 小出 晃、山口 孝、小高 孝、他:「過敏性腸症候群の原因としての細菌の過剰繁殖」. 過敏性腸症候群患者における腹部単純X線写真による腸内ガスの定量的解析. Am J Gastroenterol. 2000;95(7):1735-1741.
7. Eisenmann A, Amann A, Said M, et al. Hydrogen breath testsの実施と解釈. また,このような場合にも,「水素とメタン」というキーワードは有効です. Milwaukee, WI: QuinTron Instrument Company, Inc; 2013.
9. Quigley EM, Quera R. Small intestinal bacterial overgrowth: roles of antibiotics, prebiotics, and probiotics.小腸細菌の過繁殖:抗生物質、プレバイオティクス、プロバイオティクスの役割. Gastroenterology. 2006;130(2 Suppl 1):S78-S90.
10. 腸内細菌が産生するガスであるメタンは、腸管通過を遅らせ、小腸の収縮活性を増大させる。 Am J Physiol Gastrointest Liver Physiol. 2006;290(6):G1089-G1095.
11. QuinTronのカタログとインフォメーション。 Milwaukee, WI: QuinTron Instrument Company Inc; 2012:22.
12. Staudacher HM, Whelan K, Irving PM, Lomer MC. 過敏性腸症候群患者における発酵性炭水化物(FODMAP)の低い食事に関する助言と標準的な食事に関する助言に続く症状反応の比較。 J Hum Nutr Diet. 2011;24(5):487–495.
13. Bouhnik Y, Alain S, Attar A, et al. 小腸細菌過剰増殖症候群患者における上部腸管を汚染する細菌集団. Am J Gastroenterol. 1999;94(5):1327–1331.
14. Gabrielli M, Lauritano EC, Scarpellini E, et al. Bacillus clausii as a treatment of small intestinal bacterial overgrowth(小腸内細菌過剰増殖症候群の治療法としてのバチルス・クラウジー)。 Am J Gastroenterol. 2009;104(5):1327-1328.
15. Barrett JS, Canale KE, Gearry RB, et al. 過敏性腸症候群患者における腸内発酵パターンに対するプロバイオティクスの効果. World J Gastroenterol. 2008;14(32):5020-5024.
16. Soifer LO, Peralta D, Dima G, Besasso H. 腸内細菌過剰増殖と慢性腹部機能膨満を有する患者の治療におけるプロバイオティクス対抗生物質の比較臨床効果:パイロットスタディ。 Acta Gastroenterol Latinoam. 2010;40(4):323-327.
17. Schiffrin EJ, Parlesak A, Bode C, et al. 腸内細菌過剰増殖のある高齢者におけるプロバイオティクスヨーグルト:内毒素血症と自然免疫機能. Br J Nutr. 2009;101(7):961-966.
18. Lauritano EC, Valenza V, Sparano L, et al. 小腸内細菌過剰増殖と腸管透過性. Scand J Gastroenterol. 2010;45(9):1131-1132.
19. Riordan SM, McIver CJ, Thomas DH, et al. Luminal bacteria and small-intestinal permeability(小腸内細菌と小腸透過性). Scand J Gastroenterol. 1997;32(6):556-563.
20. Ruland J. ホームオスタシスへの回帰:NF-κB応答のダウンレギュレーション. Nat Immunol. 2011;12(8):709-714.
21. アル・サディRM、マーTY. IL-1βは腸管上皮のタイトジャンクションの透過性を上昇させる。 J Immunol. 2007;178(7):4641-4649.
22. Csaki C, Mobasheri A, Shakibaei M. Synergistic chondroprotective effects of curcumin and resveratrol in human articular chondrocytes: inhibition of IL-1beta-induced NF-kappaB-mediated inflammation and apoptosis. Arthritis Res Ther. 2009;11(6):R165.
23. Bowman G. The Gut, the Brain and the Functional GI Disorders(腸,脳,機能性胃腸障害). Functional Gastroenterologyセミナー. レベル1. NCNM; Winter, 2010:19.
24. ピメンテルM. 新しいIBSの解決法. シャーマン・オークス、カリフォルニア:ヘルス・ポイント・プレス;2006.
.