
ALLISON SIEBECKER, ND, MSOM, LAC
STEVEN SANDBURG-LEWIS, ND, DHANP
Unul dintre obiectivele noastre majore este educarea medicilor cu privire la tratamentele eficiente pentru sindromul intestinului iritabil (IBS). În ultimul nostru articol despre supracreșterea bacteriană a intestinului subțire (SIBO), am explicat elementele de bază ale acestei cauze majore a SII. Ca o continuare, vom discuta acum punctele fine ale diagnosticului și interpretării testelor (cu exemple de cazuri), precum și dieta, probioticele, repararea și prevenirea.
Diagnosticarea SIBO
Există 2 teste care pot diagnostica SIBO: endoscopia cu cultură și testul respirației cu hidrogen/metan. Nici testarea scaunului și nici testarea acizilor organici din urină nu pot diagnostica SIBO. Cea mai frecventă metodă de evaluare a SIBO este testarea respirației cu hidrogen/metan, deoarece oferă cele mai precise și detaliate informații, fiind în același timp non-invazivă și ieftină. În comparație, endoscopia, deși oferă o măsurare directă, are mai multe limitări. Este invazivă, costisitoare și poate preleva doar probe din intestinul subțire proximal, deoarece endoscopia nu se extinde de obicei dincolo de duoden.1 Aceasta este o limitare semnificativă, deoarece se consideră că SIBO distal este cel mai frecvent.2 În plus, culturile nu pot reflecta cu exactitate bacteriile anaerobe prezente în SIBO, deoarece majoritatea bacteriilor anaerobe nu pot fi cultivate.3 În mod similar, testarea acizilor organici, care poate indica indirect o creștere excesivă bacteriană prin prezența hipuratului urinar, a p-hidroxibenzoatului și a altor metaboliți bacterieni, nu poate distinge localizarea creșterii excesive între intestinul subțire distal și intestinul gros proximal și nici nu oferă detaliile oferite de un test respirator.4 Testele de scaun pot sugera doar o creștere bacteriană excesivă a intestinului gros, deși pot arăta malabsorbția grăsimilor care rezultă adesea din SIBO.
Creșterea bacteriană excesivă produce cantități excesive de hidrogen și/sau gaz metan.5, 6 Aceste gaze nu sunt produse de oameni, ci sunt subproduse metabolice ale fermentării carbohidraților de către bacteriile intestinale.7 Testul respirator măsoară aceste gaze și, prin urmare, este un test indirect; cu toate acestea, el specifică ce gaze sunt prezente, precum și localizarea și severitatea SIBO. Aceste informații sunt adesea esențiale pentru tratament și pentru evaluarea prognosticului. Mai mult decât atât, majoritatea studiilor de cercetare privind SIBO utilizează testul respirației.
După recoltarea unei probe de bază la post, se ingerează o soluție de lactuloză, un zahăr sintetic neabsorbabil, ca substrat pentru fermentația bacteriană. Numai bacteriile, nu și oamenii, produc enzimele pentru a digera lactuloza. Lactoza are nevoie de aproximativ 2 ore pentru a traversa intestinul subțire. În acest interval de timp se prelevează probe de respirație în serie la fiecare 15-20 de minute, pentru a reflecta cantitatea de bacterii din intestinul subțire, și pentru o a treia oră, care reflectă intestinul gros. Deși timpul de tranzit al lactulozei prin intestinul subțire este dezbătut în literatura de specialitate, se convine în general asupra unui minim de 90 de minute pentru a reflecta în mod corespunzător SIBO.2 Glucoza poate fi, de asemenea, utilizată ca substrat de testare, dar, din cauza absorbției sale rapide în intestinul subțire proximal, nu reușește să identifice SIBO distal.2 Dacă testarea glucozei este negativă, este necesară în continuare o testare a lactulozei pentru a testa SIBO distal.
Testul necesită o dietă de pregătire de 24 de ore și un post de o noapte. Pregătirea pentru test variază de la un laborator la altul, dar o dietă tipică de pregătire se limitează la orez alb, pește/pasăre/carne, ouă, brânzeturi tari, bulion limpede de vită sau de pui (nu bulion de oase sau bulion), ulei, sare și piper. Scopul dietei de pregătire este de a obține o reacție clară la soluția de testare prin reducerea prezenței alimentelor fermentabile. În unele cazuri, pot fi necesare 2 zile de dietă de pregătire pentru a reduce suficient de mult gazele de bază la negativ. Antibioticele nu ar trebui să fie utilizate timp de cel puțin 2 săptămâni înainte de un test inițial, deși unele surse recomandă 4 săptămâni.7 Dacă un pacient ia antibiotice în mod continuu și se suspectează SIBO, testarea inițială a respirației poate fi efectuată fără întreruperea antibioticelor.
Testarea poate fi efectuată într-o unitate cu un aparat de testare a respirației sau la domiciliu cu un kit care se trimite prin poștă pentru analiză. (Consultați www.siboinfo.com/testing.) Nu toate laboratoarele testează pentru metan, deoarece instrumentarul variază. Testarea metanului este importantă deoarece tratamentul poate fi diferit pentru metan față de hidrogen.
Interpretarea testului poate varia foarte mult între practicieni.2 Nu există criterii agreate, situație pe care sperăm să o vedem remediată. Este foarte posibil ca un pacient să fie considerat pozitiv de către un medic/laborator și negativ de către altul. Criteriile furnizate de producătorul aparatului pentru un test pozitiv sunt următoarele:8
– O creștere față de cea mai mică valoare precedentă a producției de hidrogen de 20 părți pe milion (ppm) sau mai mare în decurs de 120 de minute de la ingerarea lactulozei
– O creștere față de cea mai mică valoare precedentă a producției de metan de 12 ppm sau mai mare în decurs de 120 de minute de la ingerarea lactoză
– O creștere față de cea mai mică valoare precedentă a sumei combinate a producției de hidrogen și metan de 15 ppm sau mai mare în decurs de 120 de minute de la ingerarea lactulozei
Am constatat că un nivel absolut de gaze la sau peste nivelurile pozitive de ppm furnizate de QuinTron, fără o creștere față de valoarea inițială sau față de cea mai mică valoare anterioară, se corelează bine cu SIBO clinic. Acest lucru este valabil în special pentru gazul metan, care poate avea un tipar cu un nivel de bază ridicat (> 12 ppm) care rămâne ridicat pe durata testului (Figura 1). În astfel de cazuri, metanul poate crește doar cu 5 ppm, dar nivelul ppm este în mod constant peste pragul pozitiv. Interpretarea hidrogenului sau a metanului ridicat pe proba de bază (înainte de ingestia de lactoză) este controversată, dar noi preferăm să considerăm o valoare de bază ridicată ca fiind un test pozitiv9, 10 (figura 2), cu excepția cazului în care nivelurile de gaz scad după valoarea de bază și continuă să scadă sau rămân scăzute în primele 2 ore, ceea ce indică o dietă de pregătire necorespunzătoare (figurile 3 și 3.5).
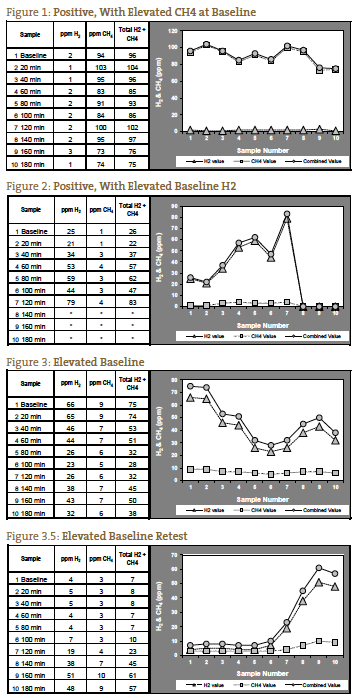
Posibilitatea clasică pentru SIBO a fost considerată a fi un vârf dublu, cu primul vârf reprezentând SIBO și al doilea vârf reprezentând abundența normală a bacteriilor din intestinul gros (figura 4). Aceasta este o prezentare puțin frecventă în experiența noastră. Mai des observăm 1 vârf care crește și mai mult în a treia oră, reprezentând SIBO distal urmat de bacteriile normale din intestinul gros (figura 5).
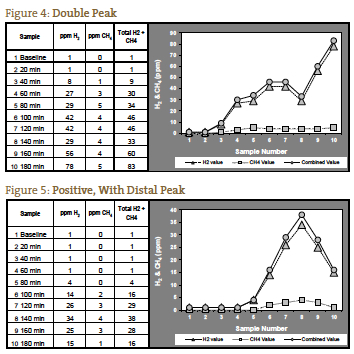
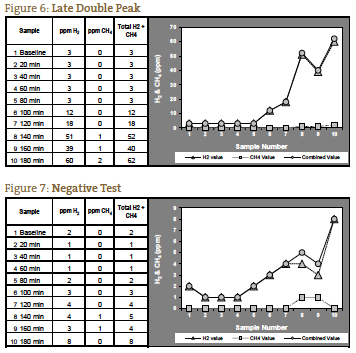
Dacă gazele măsurate nu cresc decât după 120 de minute, este posibil ca acest lucru să se datoreze unui timp de tranzit prelungit, ceea ce am observat la pacienții cu constipație severă. La un astfel de pacient cu tabloul simptomatic așteptat pentru SIBO de tip constipație, o creștere semnificativă la 140 de minute poate fi interpretată ca un test pozitiv (figura 6). Figura 7 reprezintă un test negativ; rețineți că scara din stânga graficului este redusă pentru a reflecta nivelurile mai scăzute de gaz. Figurile de la 1 la 7 sunt exemple de cazuri furnizate de laboratorul NCNM.
Testarea respirației poate fi utilizată în cazurile pediatrice, atâta timp cât copilul poate urma în mod corespunzător instrucțiunile de a sufla în dispozitivul de colectare. Pentru cei sub 3 ani, testarea se face cel mai bine în cabinet/laborator, din cauza diferențelor dintre metodele de colectare și kiturile de acasă. Doza de lactuloză pediatrică este de 1g/kg de greutate corporală, cu un maxim de 10 g (cei de peste 22 de lire sterline primesc doza maximă de 10 g pentru adulți).11 Kiturile de lactuloză pot fi comandate numai de către medicii prescriptori, deoarece lactuloza este un produs care se eliberează pe bază de prescripție medicală.
Tratament dietetic
Dietă folosită pentru tratarea SIBO reduce încărcătura bacteriană și fermentarea carbohidraților, precum și ajută la vindecarea țesuturilor. Ele fac acest lucru prin diminuarea polizaharidelor, oligozaharidelor și dizaharidelor prin eliminarea tuturor cerealelor, legumelor cu amidon, lactozei și îndulcitorilor, alții decât mierea. Leguminoasele sunt eliminate inițial. Am constatat că utilizarea dietei Specific Carbohydrate Diet™ (SCD) sau a variantei sale, dieta Gut and Psychology Syndrome™ (GAPS), ca dietă de bază, cu încorporarea recomandărilor privind fructele și legumele din dieta Low FODMAP™ (Tabelul 1), reprezintă o abordare eficientă. (A se vedea Tabelul 2 pentru resurse pentru dieta SIBO.) Dieta Low FODMAP este o dietă de tratament pentru SIBO care rezultă din investigarea nivelurilor de carbohidrați fermentescibili din alimente; are o rată de succes de 76% pentru SIBO.12 Dieta FODMAP nu este concepută special pentru SIBO și, prin urmare, nu elimină sursele de polizaharide și dizaharide, cum ar fi cerealele, amidonul, legumele cu amidon și zaharoza. Eliminarea acestor polizaharide și dizaharide este esențială în SIBO. În SIBO, carbohidrații bine absorbiți, alimente care, de obicei, merg să hrănească gazda, hrănesc în schimb bacteriile crescute din intestinul subțire, creând simptome și alimentând mai multă creștere bacteriană1 (Figura 8).
Orice dietă va trebui să fie individualizată prin încercări și erori în timp. Furnizarea unei diagrame alimentare sau a unei anumite rețete de dietă oferă doar un punct de plecare.
Dietele cu conținut scăzut de carbohidrați sunt diete pentru pierderea în greutate. O atenție deosebită trebuie acordată celor care sunt la limită sau subponderali. Dacă o dietă SIBO duce la o pierdere excesivă în greutate, această strategie dietetică va trebui să fie modificată pentru a permite mai mulți carbohidrați. În aceste circumstanțe, una sau mai multe dintre celelalte 3 opțiuni de tratament descrise în articolul nostru anterior trebuie luate în considerare, împreună cu orezul alb, glucoza și alte surse de carbohidrați.
Probioticele
Probioticele sunt o intervenție controversată în SIBO, deoarece lactobacilii au fost cultivați în SIBO13 și există îngrijorare cu privire la adăugarea la supraîncărcarea bacteriană. Acesta este în special cazul în care există o motilitate scăzută din cauza unui complex motor migrator disfuncțional (MMC). În ciuda acestei preocupări, puținele studii probiotice care s-au concentrat direct pe SIBO au arătat rezultate bune, cu o rată de eradicare de 47% în cazul Bacillus clausii ca unic tratament14 , o rată de succes de 64% în cazul Lactobacillus casei Shirota ca unic tratament15 și o îmbunătățire clinică de 82% în cazul Lactobacillus casei și L. plantarum, Streptococcus faecalis și Bifidobacter brevis ca unic tratament16. Iaurtul probiotic care conține Lactobacillus johnsonii a normalizat răspunsurile la citokine, reducând inflamația cronică de grad scăzut întâlnită în SIBO, după 4 săptămâni de suplimentare.17 Am observat rezultate bune la pacienții noștri cu SIBO folosind diverse probiotice cu tulpini multiple și unice, precum și iaurt de casă fără lactoză și legume de cultură.
Un punct cheie pentru utilizarea suplimentelor probiotice în SIBO este evitarea prebioticelor ca ingrediente principale. Prebioticele sunt alimente fermentescibile pentru bacterii care pot exacerba simptomele în timpul SIBO activ și pot încuraja creșterea bacteriană post-SIBO. Prebioticele comune care se găsesc în suplimentele probiotice includ: FOS (fructo-oligozaharide), MOS (mannan-oligozaharide), GOS (galacto-oligozaharide), inulină și arabinogalactan. Prebioticele pot fi tolerate individual în cantitățile mici utilizate ca ingrediente de bază.
Permeabilitatea intestinală
Studiile care au examinat rata de vindecare a mucoasei post-SIBO au constatat că permeabilitatea intestinală s-a normalizat la 75%-100% dintre pacienții cu SIBO în termen de patru săptămâni după un tratament antibiotic reușit.18,19 Pentru cei a căror permeabilitate nu se normalizează, suplimentele pot ajuta în procesul de vindecare.
Herbaceele mucilaginoase sunt utilizate în mod tradițional pentru vindecarea mucoaselor, inclusiv Glycyrrhiza glabra (lemn dulce), Ulmus fulva (ulm alunecos), Aloe vera și Althea officinalis (nalbă); cu toate acestea, utilizarea lor post-SIBO este controversată din cauza conținutului lor de mucopolizaharide care ar putea încuraja regenerarea bacteriană. Printre nutrienții specifici pe care i-am folosit se numără colostrul (2-6 g QD), L-glutamina (375-1500+ mg QD), carnosina de zinc (75-150 mg QD), vitaminele A și D, adesea administrate sub formă de ulei de ficat de cod (1 lingură QD), curcumină (400 mg până la 3 g QD), resveratrol (250 mg până la 2 g QD), glutation, sub formă de lipozomal oral (50-425 mg QD) sau de precursor al glutationului N-acetilcisteină (200-600 mg QD). Suplimentele se administrează timp de 1 până la 3 luni, sau pot fi continuate pe termen lung. Doze mai mari de curcumină și resveratrol sunt administrate timp de 2 săptămâni în scopul de a reduce reglarea NF-Κβ, un mediator al permeabilității intestinale crescute, urmate de niveluri de menținere mai moderate.20, 21,22
Prevenție
Suplimente
Suplimentele de acid clorhidric betaina sau suplimentele pe bază de plante amare, care încurajează secreția de acid clorhidric (HCl)23 pot fi utilizate pentru a diminua încărcătura de bacterii ingerate. Atunci când se ia în considerare suplimentarea cu HCl, testarea pH-ului Heidelberg este standardul de aur.
Spațierea meselor
În plus față de agenții procinetici (discutați în articolul nostru din ianuarie 2013), spațierea meselor la o distanță de 4 până la 5 ore între ele, ingerând nimic altceva decât apă, permite complexului motor migrator (MMC) să măture intestinul subțire de bacterii noaptea și între mese.24 Am constatat că acest lucru este foarte util din punct de vedere clinic. Dacă o dietă SIBO săracă în carbohidrați nu corectează hipoglicemia, această strategie va trebui modificată pentru a permite mese mai frecvente.
Perspectivele actuale privind interpretarea testelor și strategiile de tratament vor fi discutate la Simpozionul SIBO 2014, 18-19 ianuarie în Portland OR, și vor fi, de asemenea, disponibile prin intermediul unui webinar live și înregistrat (www.sibosymposium.com).
 Allison Siebecker, ND, MSOM, LAc este absolventă a Colegiului Național de Medicină Naturală (Portland, Oregon), unde este specializată în tratarea supracreșterii bacteriene a intestinului subțire (SIBO) și este profesor adjunct de gastroenterologie avansată. În prezent, ea scrie o carte despre SIBO. Vizitați site-ul ei educațional despre SIBO la adresa www.siboinfo.com.
Allison Siebecker, ND, MSOM, LAc este absolventă a Colegiului Național de Medicină Naturală (Portland, Oregon), unde este specializată în tratarea supracreșterii bacteriene a intestinului subțire (SIBO) și este profesor adjunct de gastroenterologie avansată. În prezent, ea scrie o carte despre SIBO. Vizitați site-ul ei educațional despre SIBO la adresa www.siboinfo.com.
 Steven Sandberg-Lewis, ND, DHANP, a practicat medicina naturistă încă de la absolvirea Universității Naționale de Medicină Naturală (NUNM) în 1978. A fost profesor la NUNM din 1985, predând o varietate de cursuri, dar concentrându-se în principal pe gastroenterologie și medicină fizică GI. Rotațiile sale în clinică sunt deosebit de populare în rândul doctoranzilor de la NUNM. În plus față de supervizarea rotațiilor clinice, el menține, de asemenea, un cabinet cu jumătate de normă la 8Hearts Health and Wellness din Portland, Oregon.
Steven Sandberg-Lewis, ND, DHANP, a practicat medicina naturistă încă de la absolvirea Universității Naționale de Medicină Naturală (NUNM) în 1978. A fost profesor la NUNM din 1985, predând o varietate de cursuri, dar concentrându-se în principal pe gastroenterologie și medicină fizică GI. Rotațiile sale în clinică sunt deosebit de populare în rândul doctoranzilor de la NUNM. În plus față de supervizarea rotațiilor clinice, el menține, de asemenea, un cabinet cu jumătate de normă la 8Hearts Health and Wellness din Portland, Oregon.
Este un conferențiar internațional popular la seminariile de medicină funcțională, prezintă webinarii, scrie articole pentru NDNR și Townsend Letter și este frecvent intervievat pe teme de sănătate și boli digestive. Este autorul manualului medical Functional Gastroenterology (Gastroenterologie funcțională): Assessing and Addressing the Causes of Functional Digestive Disorders, ediția a doua, 2017, care este disponibilă pe amazon.com. În 2010, el a co-fondat Centrul SIBO de la NUNM, care este unul dintre cele patru centre din SUA pentru diagnosticarea, tratamentul, educația și cercetarea supracreșterii bacteriene a intestinului subțire. În 2014 a fost numit unul dintre „Top Docs” în ediția anuală de sănătate a revistei Portland Monthly, iar în 2015 a fost inclus în OANP/NUNM Hall of Fame.
În cadrul gastroenterologiei, are un interes și o expertiză specială în ceea ce privește bolile inflamatorii intestinale (inclusiv colita microscopică), sindromul colonului iritabil (inclusiv IBS post-infecțios), supracreșterea bacteriană a intestinului subțire (SIBO), hernia hiatală, refluxul gastroesofagian și biliar (GERD), dischinezia biliară și stările cronice de greață și vărsături.
Mulți dintre pacienții trimiși la Dr. Sandberg-Lewis au afecțiuni digestive care au sfidat diagnosticarea și rezolvarea eficientă. Adesea, acești pacienți doresc opțiuni de tratament naturist în locul tratamentelor la care au fost supuși anterior. El înțelege bolile tractului gastrointestinal, dar poate, de asemenea, să evalueze funcția și adesea să găsească tratamente de succes pentru a recăpăta un echilibru în sistemul digestiv.
Dr. Sandberg-Lewis locuiește în Portland împreună cu soția sa, Kayle. Printre interesele sale se numără mandolina, chitara și vocea; schiul de fond; scrisul și conferințele.
1. Lin HC. Small intestinal bacterial overgrowth: un cadru pentru înțelegerea sindromului intestinului iritabil. JAMA. 2004;292(7):852-858.
2. Shah ED, Basseri RJ, Chong K, Pimentel M. Testarea anormală a respirației în IBS: o meta-analiză. Dig Dis Sci. 2010;55(9):2441-2449.
3. Khoshini R, Dai SC, Lezcano S, Pimentel M. A systematic review of diagnostic tests for small intestinal bacterial overgrowth. Dig Dis Sci. 2008;53(6):1443-1454.
4. Lord RS, Bralley JA. Aplicații clinice ale acizilor organici urinari. Partea 2. Markeri de disbioză. Altern Med Rev. 2008;13(4):292-306.
5. Riordan SM, Kim R. Bacterial overgrowth as a cause of irritable bowel syndrome. Curr Opin Gastroenterol. 2006;22(6):669-673.
6. Koide A, Yamaguchi T, Odaka T, et al. Analiza cantitativă a gazelor intestinale folosind radiografia abdominală simplă la pacienții cu sindrom de intestin iritabil. Am J Gastroenterol. 2000;95(7):1735-1741.
7. Eisenmann A, Amann A, Said M, et al. Implementation and interpretation of hydrogen breath tests. J Breath Res. 2008;2(4):046002.
8. Protocoale și ajutor de interpretare, testele de respirație cu hidrogen/metan. Milwaukee, WI: QuinTron Instrument Company, Inc; 2013.
9. Quigley EM, Quera R. Small intestinal bacterial overgrowth: roluri ale antibioticelor, prebioticelor și probioticelor. Gastroenterologie. 2006;130(2 Suppl 1):S78-S90.
10. Pimentel M, Lin HC, Enayati P, et al. Metanul, un gaz produs de bacteriile enterice, încetinește tranzitul intestinal și mărește activitatea contractilă a intestinului subțire. Am J Physiol Gastrointest Liver Physiol. 2006;290(6):G1089-G1095.
11. Catalogul și informațiile QuinTron. Milwaukee, WI: QuinTron Instrument Company Inc; 2012:22.
12. Staudacher HM, Whelan K, Irving PM, Lomer MC. Compararea răspunsului la simptome în urma sfaturilor pentru o dietă cu conținut scăzut de carbohidrați fermentescibili (FODMAPs) față de sfaturile dietetice standard la pacienții cu sindrom de intestin iritabil. J Hum Nutr Diet. 2011;24(5):487–495.
13. Bouhnik Y, Alain S, Attar A, et al. Populațiile bacteriene care contaminează intestinul superior la pacienții cu sindromul de supracreștere bacteriană a intestinului subțire. Am J Gastroenterol. 1999;94(5):1327–1331.
14. Gabrielli M, Lauritano EC, Scarpellini E, et al. Bacillus clausii ca tratament al supracreșterii bacteriene intestinale mici. Am J Gastroenterol. 2009;104(5):1327-1328.
15. Barrett JS, Canale KE, Gearry RB, et al. Efectele probiotice asupra modelelor de fermentație intestinală la pacienții cu sindrom de intestin iritabil. World J Gastroenterol. 2008;14(32):5020-5024.
16. Soifer LO, Peralta D, Dima G, Besasso H. Eficacitatea clinică comparativă a unui probiotic vs. un antibiotic în tratamentul pacienților cu supracreștere bacteriană intestinală și distensie funcțională abdominală cronică: un studiu pilot. Acta Gastroenterol Latinoam. 2010;40(4):323-327.
17. Schiffrin EJ, Parlesak A, Bode C, et al. Iaurtul probiotic la vârstnicii cu hipercreștere bacteriană intestinală: endotoxemie și funcții imune înnăscute. Br J Nutr. 2009;101(7):961-966.
18. Lauritano EC, Valenza V, Sparano L, et al. Small intestinal bacterial overgrowth and intestinal permeability. Scand J Gastroenterol. 2010;45(9):1131-1132.
19. Riordan SM, McIver CJ, Thomas DH, et al. Luminal bacteria and small-intestinal permeability. Scand J Gastroenterol. 1997;32(6):556-563.
20. Ruland J. Întoarcerea la homeostazie: reglarea în jos a răspunsurilor NF-κB. Nat Immunol. 2011;12(8):709-714.
21. Al-Sadi RM, Ma TY. IL-1beta determină o creștere a permeabilității joncțiunii strânse epiteliale intestinale. J Immunol. 2007;178(7):4641-4649.
22. Csaki C, Mobasheri A, Shakibaei M. Synergistic chondroprotective effects of curcumin and resveratrol in human articular chondrocytes: inhibition of IL-1beta-induced NF-kappaB-mediated inflammation and apoptosis. Arthritis Res Ther. 2009;11(6):R165.
23. Bowman G. The Gut, the Brain and the Functional GI Disorders (Intestinele, creierul și tulburările gastrointestinale funcționale). Seminar de gastroenterologie funcțională: Nivelul 1. NCNM; iarna, 2010:19.
24. Pimentel M. O nouă soluție pentru IBS. Sherman Oaks, CA: Health Point Press; 2006.
.