A Plaquenil (Sanofi-Aventis) márkanév alatt forgalmazott hidroxiklorokvin egy maláriaellenes gyógyszer, amelyet széles körben alkalmaznak különböző autoimmun betegségek, köztük a szisztémás lupus erythematosus és a rheumatoid arthritis kezelésében.1 Egyes becslések szerint csak Amerikában több mint 150 000 beteg részesül hosszú távú terápiában ezzel a gyógyszerrel.2 A HCQ alkalmazásával összefüggő retinatoxicitás viszonylag ritka, becslések szerint öt év után 1 százalék, és a terápia folytatásával emelkedik.3 A retinopátia, amelyet bikaszemként írnak le, azonban nem kezelhető, és hajlamos a gyógyszer abbahagyása után is előrehaladni. Ennek megfelelően az utóbbi években egyre nagyobb hangsúlyt fektettek a multimodális képalkotó technikákat alkalmazó hatékonyabb szűrési intézkedésekre, hogy a toxicitás korai jeleit még a jellegzetes előrehaladott elváltozások klinikai manifesztálódása előtt felismerjék. Ez az áttekintés összefoglalja a HCQ retinopátia klinikai megjelenését, az American Academy of Ophthalmology által jelenleg ajánlott szűrési irányelveket és a kiegészítő képalkotó vizsgálatok hozzájárulását az időben történő diagnózis felállításához.
Klinikai megjelenés & Vizsgálat
A HCQ-toxicitás legkorábbi szakaszában a betegek gyakran tünetmentesek, a látásélesség megőrzése mellett. Az éleslátó egyének azonban éjszakai látási nehézségekről, vakulásról vagy paracentrális szkotómákról számolhatnak be, amelyek zavarják az olvasást.4-6 A szkotóma jellemzően jóval azelőtt válik nyilvánvalóvá a beteg számára, hogy a vizsgálaton változások észlelhetők lennének. Bár a korai toxicitás egyes eseteiben leírták a finom foveális depigmentáció felismerését, ez csak kiegészítő képalkotó vizsgálatokkal történő megerősítés után történt.7
Másrészt a látható bikaszem retinopátia, amelyet a retina pigment epithelium degenerációjának gyűrűje jellemez, gyakran a foveális központot kímélve, késői lelet, amely előrehaladott károsodásra utal (lásd az 1. ábrát). Így az ophthalmoscopia önmagában nem elegendő a HCQ-toxicitás szűrésére.7,8 Ennek ellenére a részletes elülső és hátsó szegmentumvizsgálat a szaruhártya verticillata, valamint az egyidejű makulabetegség (azaz az életkorral összefüggő makuladegeneráció) felmérése érdekében továbbra is fontos e betegek hosszú távú megfigyelésében.
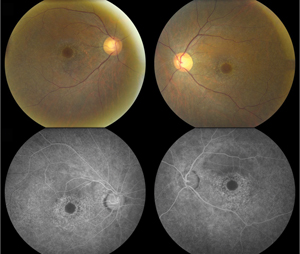
1. ábra. A fundusfelvételek (fent) a retina pigmenthámjának kiterjedt paracentrális depigmentációját mutatják, amely kétoldalt kíméli a központi foveát, ami megfelel a bikaszemes makulopátiának. A fluoreszcein angiográfia (alul) parafovealis granuláris hiperfluoreszcenciát mutat, amely korrelál a foltos RPE-szakadással és az azt követő ablakdefektussal.
Szűrési irányelvek
2002-ben az AAO közzétette a HCQ retinopátia szűrésére vonatkozó első preferált gyakorlati mintákat, válaszul az akkoriban javasolt változatos kezelési módokra.9 Ezeket az ajánlásokat 2011-ben felülvizsgálták, hogy tükrözzék az újabb képalkotó diagnosztikai technikák fokozott érzékenységét.4
Ha a beteget a retinopátia szempontjából alacsony kockázatúnak ítélték, a kezdeti alapvizsgálatot követő ötéves terápiától kezdődően javasoltak követéses vizsgálatokat. Ha a beteg magas kockázatúnak minősült, éves nyomon követést javasoltak. Magas kockázatúnak tekintették azt, akinél a HCQ-használat időtartama meghaladta az öt évet, a kumulatív fogyasztás meghaladta az 1000 grammot, a napi adagolás meghaladta a 6,5 mg/kg/napot, a megnövekedett életkor (nem határozták meg a határértéket), az egyidejűleg fennálló máj-/vese betegség vagy más etiológiájú, már meglévő makulopátia.4
A szemészeti vizsgálat és az automatizált küszöbértékű Humphrey látótérvizsgálat mellett fehér 10-2 mintával (amelyet alacsony rendellenességi küszöbbel kell értelmezni, és szabálytalanságok észlelése esetén meg kell ismételni a vizsgálatot), az alábbi kiegészítő objektív képalkotó vizsgálatok közül legalább egy javasolt: 1) spektrális tartományú optikai koherencia tomográfia; 2) szemfenéki autofluoreszcencia; vagy 3) multifokális elektroretinográfia, a kiindulási időpontban és a HCQ-használat öt éve után évente minden egyes vizsgálat alkalmával.4 Figyelemre méltó, hogy a fluoreszcein angiográfiát nem ajánlották ezekben az irányelvekben. Bár az FA képes feltárni a granuláris hiperfluoreszcencia bull’s-eye mintázatát, és képes lehet a finom RPE-hibák megvilágítására, nem bizonyult olyan érzékenynek, mint a fent említett vizsgálatok, és invazivitása miatt további morbiditással jár.4
Spectral-Domain OCT
A retina nagy felbontású, keresztmetszeti képeit in vivo létrehozva az SD-OCT jelentős strukturális elváltozásokat mutathat ki a látható HCQ retinopátia kialakulása előtt. A HCQ-toxicitásban korábban leírt OCT-leletek közé tartozik a külső határmembrán elvesztése, a külső ellipszoid zóna megszakadása, a külső magréteg parafoveális elvékonyodása és az RPE károsodása.6,7,10 E különböző változások ellenére számos tanulmány alátámasztotta azt az elképzelést, hogy a HCQ-toxicitásban gyakori a relatív “foveális rezisztencia”, amit a subfoveális külső retinarétegek megőrzése mutat, ami az előrehaladott betegségben is megfigyelhető intakt központi látásélességért felelős.6 6 Ez a foveális kímélet szolgál a HCQ retinopátia Eric Chen, MD és munkatársai által leírt “repülő csészealj” jelének alapjául, ahol a tojásdad megjelenést az intakt központi foveális külső retinális struktúrák hozzák létre, ellentétben a szomszédos perifoveális fotoreceptor ellipszoid sáv elvesztésével és az ONL atrófiájával (lásd a 2. ábrát).11
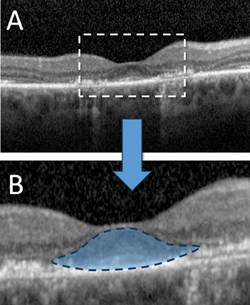
2. ábra. Spektrális tartományú optikai koherencia tomográfia, amely előrehaladott hidroxiklorokvin retinopátiát mutat a külső határhártya parafovealis elvesztésével, a külső ellipszoid zóna felbomlásával, a külső magréteg elvékonyodásával és az alatta lévő retinális pigmenthámréteg felbomlásával (A). A subfovealis struktúrák viszonylagos kímélete az előrehaladott toxicitás jellegzetes “repülő csészealj” jelét eredményezi (B).11
Míg a szakirodalom nagy része a HCQ retinopátia során a külső retina elváltozásaira összpontosít, a toxicitás legkorábbi SD-OCT-leletei valójában a belső retinára lokalizálódhatnak. Dr. Sirichai Pasadhika és munkatársai a perifoveális belső retina, különösen a belső plexiform és ganglionsejtes réteg szelektív elvékonyodását figyelték meg SD-OCT-n a hosszú ideig (több mint öt évig) HCQ-val kezelt betegeknél, a külső retina/RPE strukturális változásainak vagy más klinikailag nyilvánvaló toxicitásnak a hiányában.12 Érdekes módon a retina idegrost rétegének elvékonyodását nem találták ezeknél a betegeknél, ami a szerzők szerint csak akkor fordul elő, ha már jelentős retinális ganglionsejt-degeneráció következett be. Egy külön vizsgálatban, amelynek célja a krónikusan kezelt, a toxicitás szemészeti bizonyítékával rendelkező és nem rendelkező betegek összehasonlítása volt, a klinikailag nyilvánvaló retinatoxicitással rendelkező betegeknél a belső, külső és teljes vastagságú retina jelentős elvékonyodását figyelték meg, míg a szemfenéki elváltozások nélküli csoportban csak a belső retina szelektív elvékonyodását észlelték.13 Az RNFL elvékonyodása ismét hiányzott a krónikus HCQ-expozícióval rendelkező, szemfenéki elváltozások nélküli betegeknél; azonban a gyógyszer toxicitással összefüggő szemfenéki elváltozásokkal rendelkező csoportban peripapilláris RNFL elvékonyodás volt megfigyelhető. Ulviye Yigit és szerzőtársai nemrégiben megerősítették ezeket az eredményeket, mivel a HCQ-terápia során a belső retina jelentős elvékonyodását mérték, különösen a para- és perifoveális területeken, klinikai szemfenéki elváltozások hiányában.14 Az ő vizsgálatukban egyedülálló volt, hogy a HCQ-kezelésben kevesebb mint öt éve részesülő betegeket vontak be (átlagos időtartam: 2,5 év).
Még több, nagyobb betegszámot érintő vizsgálatot kell végezni annak pontosabb meghatározása érdekében, hogy milyen SD-OCT-alapú mutatókat lehet megbízhatóan értékelni a korai HCQ-toxicitásban. Tekintettel azonban gyors képfelvételi idejére, noninvazív jellegére és széles körű elérhetőségére számos klinikán, a gyakorló orvosok többsége továbbra is az SD-OCT-t részesíti előnyben a látótérvizsgálat elsődleges kiegészítőjeként a HCQ-szűrés során.
Fundus autofluoreszcencia
A FAF-képalkotás segíthet megvilágítani a hosszú távú HCQ-terápia következtében az alapul szolgáló RPE toxikus elváltozásait. A megnövekedett FAF-jel jellemzően a lipofuszcin, különösen az A2E fluorofór felhalmozódását jelzi az RPE-ben, amely vagy a fotoreceptor külső szegmensek fokozott fagocitózisával járó rendellenes anyagcseréből, vagy a fagocitotikus folyamatok öröklött/szerzett hibájából ered.15,16 A kialudt FAF-jel ezzel szemben az RPE-sejtek elhalását jelzi.17
A megnövekedett FAF-intenzitású pericentrális gyűrű korai leletét, amely hiperfluoreszcens izzásként jelenik meg, HCQ-toxicitás esetén az RPE-degeneráció kialakulása előtt lehet megfigyelni, és úgy gondolják, hogy a külső szegmensek törmelékének felhalmozódásából származó korai fotoreceptorkárosodás területeit jelzi.4,18,19 Ez azonban meglehetősen finom lehet, és a képzetlen szemlélő könnyen figyelmen kívül hagyhatja. Ha megfigyelték, egyidejűleg mfERG- vagy SD-OCT-rendellenességeket is észleltek, ami a FAF-lelet patofiziológiai alapjára utal.7,18 Ennek ellenére a FAF hasznosságát a korai szubklinikai toxicitás kimutatásában alátámasztó bizonyítékok összességében még mindig hiányoznak, így elsődleges szűrőeszközként kevésbé megbízható.
A szűrésnél fontosabb, hogy a FAF valódi értéke abban rejlik, hogy képes a HCQ retinopátia ismert eseteiben a progresszió nyomon követésére, például amikor a betegnél már abbahagyták a gyógyszer szedését, de még mindig szükség van rendszeres követéses vizsgálatokra. Ebben az összefüggésben a FAF érzékeny indikátora az RPE degenerációjának a toxicitás előrehaladtával, különösen előrehaladott stádiumban. Az RPE sorvadásával a FAF intenzitása a pericentralis makulában foltos vagy pöttyös megjelenésűvé változik, és végül a sejtek elhalását követően FAF-jel nélküli sötét területekké olvad össze (lásd a 3. ábrát).
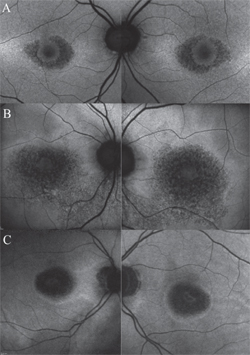
3. ábra. Fundus autofluoreszcencia-mintázatok a hidroxiklorokvin retinopátia különböző stádiumaiban. Klasszikus bikaszemszerű makulopátia megjelenése (A). Az RPE sorvadásával a FAF intenzitása a pericentralis makulában foltos vagy foltos megjelenésűvé változik (B), és végül a sejtek elhalását követően a FAF-jel nélküli sötét területekké egyesül (C). Ezeket a sötét területeket egy fokozott autofluoreszcenciájú perem határolhatja (A-C), ami jelzi, hogy mely RPE-sejtek fognak legközelebb degenerálódni.
Ezeket a sötét régiókat egy fokozott autofluoreszcenciájú perem határolhatja, ami azt jelzi, hogy mely RPE-sejtek fognak legközelebb degenerálódni.17 Meg kell jegyezni, hogy nem minden, más technikákkal (pl. SD-OCT-vel) igazolt, előrehaladott retina-atrófiával járó esetnek van markáns megjelenése a FAF-on. Ez a megállapítás kiemeli az AAO azon irányelvének fontosságát, hogy a HCQ toxikus hatásainak azonosításakor egynél több képalkotó modalitást kell használni.
Multifokális elektroretinográfia
A hagyományos teljes térbeli elektroretinográfia a retina globális működésének vizsgálatát jelenti a fotikus ingerlésre adott válaszként. Mivel nem érzékeny a makulára lokalizált funkcionális változásokra, a HCQ-toxicitás eseteiben csak akkor mutatna rendellenességeket, amikor a diffúz retinakárosodás már bekövetkezett, ami korlátozza hasznosságát a szűrőprogramokban.4,9
Ezzel szemben a multifokális ERG, amely képes lokalizált központi retinahibák rögzítésére, kiváló jelöltként vált elfogadottá a finom változások kimutatására a toxicitás korai szakaszában.20 Dr. Raj Maturi és munkatársai számoltak be először a centrális 16˚ mfERG amplitúdójának jelentős csökkenéséről egy manifeszt HCQ retinopátiában szenvedő betegnél, normális teljes mező ERG mellett.21 Hasonló eredményeket kaptak a HCQ-használókat jellemző későbbi vizsgálatok is. Timothy Y.Y. Lai, MMedSc, MRCS és munkatársai a hosszú távon HCQ-t kapó betegek retinafunkciójának hosszanti hanyatlását figyelték meg, és azt javasolták, hogy a sorozatos mfERG segíthet a toxicitással összefüggő korai retinaváltozások kimutatásában.22 Egy utóvizsgálatban kimutatták, hogy az mfERG-válaszok korreláltak a HVF 10-2 átlagos eltérési értékeivel, és így kiegészíthetik a látótérvizsgálatot azáltal, hogy a retina funkció objektív mérését biztosítják a HCQ-t használó betegeknél.23
A HCQ-toxicitásban szenvedő betegeknél megfigyelhető legjellemzőbb hullámforma a paracentrális amplitúdóvesztés, ami a retina csökkent funkcióját jelzi az érzékeny perifoveában. Egy másik vizsgálatban Dr. Maturi és munkatársai azt javasolták, hogy a meghosszabbodott implicit idő, amikor a paracentrális amplitúdóveszteséggel együtt látható, a HCQ-toxicitás specifikusabb jellemzője lehet.24 Továbbá a paracentrális veszteség mellett három további konfigurációt mutattak ki az abnormális mfERG-amplitúdóváltozásokból: 1) centrális foveális veszteség; 2) perifériás veszteség; és 3) generalizált veszteség.24 Az mfERG-változások mintázatainak osztályozására szolgáló rendszerüket azóta más csoportok is megerősítették.20,22
Azért, hogy növeljék a standard mfERG-értelmezéssel szembeni érzékenységet a korai HCQ-toxicitás kimutatásában, Jonathan S. Lyons, MD, és Matthew L. Severns, PhD, egy új algoritmust dolgozott ki az mfERG-adatok táblázatba rendezésére, amelyet “gyűrűarány-módszernek” neveztek el (lásd a 4. ábrát).20,25 Tekintettel arra, hogy bármelyik beadott mfERG amplitúdója akár 30%-kal is eltérhet egy későbbi vizsgálathoz képest,26 a gyűrűarányt úgy tervezték, hogy csökkentse ezt a háttérzajt és normatívabb értékeket hozzon létre a klinikai döntéshozatal elősegítése érdekében. Ehhez a 61 hatszögletű mfERG adatait öt koncentrikus gyűrűs zónára (R1-R5) strukturálták.
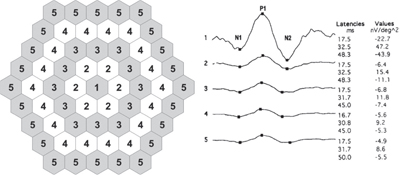
4. ábra. A multifokális elektroretinogram értelmezésének gyűrűarányos módszere. A 61 hatszögű ingerületmintarendszer bal oldali ábrája mutatja az egyes gyűrűkhöz tartozó hatszögeket. A jobb oldalon egy normális beteg gyűrűátlagolt hullámformái láthatók. (A kép hitelesítését lásd a végjegyzetekben.)
A mfERG gyűrűarányait a központi gyűrűamplitúdó (R1) és az egyes perifériás gyűrűamplitúdók arányaként határozzák meg, ami szemenként öt mérést eredményez: R1, R1/R2, R1/R3, R1/R4 és R1/R5. Mivel a normális szemben az R1 a legnagyobb gyűrűamplitúdó, a normális gyűrűarányok több mint 1,0; mivel azonban a HCQ-toxicitásban a depressziós mfERG-amplitúdójú területek jellemzően pericentrális gyűrű alakúak, és a központi makulaterület általában a betegség késői szakaszáig megkímélt, ezek a betegek jellemzően nagyobb gyűrűarányt mutatnak, mint ami várható lenne (az egészséges személyek egy részhalmazából létrehozott elfogadott normák 99 százalékos határértékei felett).20
Míg az mfERG-vizsgálat nagy ígéretet mutatott, mint objektív mérőeszköz a korai HCQ-toxicitás kimutatására, valamint az ismert betegségben bekövetkező makuláris változások progressziójának nyomon követésére, a vizsgálatot korlátozza a beteg együttműködésétől való függősége, az alkalmazáshoz és értelmezéshez szükséges speciális személyzeti képzés és az általános költségek. Talán a legfontosabb, hogy nem olyan könnyen elérhető és nem olyan könnyű megbízhatóan elvégezni, mint az SD-OCT-t vagy a FAF-t, ami a mai napig korlátozza széles körű alkalmazását.
Nem létezik egyetlen “legjobb teszt”
A képalkotó rendszerek mind a kutatási, mind a klinikai gyakorlat fórumaiba történő fokozott integrációja ellenére továbbra sincs konszenzus arról, hogy melyik teszt az arany standard a korai HCQ-toxicitás kimutatására. A szakirodalomban ez a nézeteltérés nyilvánvaló, mivel a különböző támogatók a látómezők, a FAF, az mfERG vagy az SD-OCT mellett érveltek, mint a legérzékenyebb/specifikusabb módszer mellett. David J. Browning, MD, PhD egy nemrégiben készült, 219 betegre kiterjedő retrospektív, magánpraxisban végzett vizsgálatában arra a következtetésre jutott, hogy a felülvizsgált, a kiegészítő FAF-ot, SD-OCT-t vagy mfERG-t hangsúlyozó irányelvek valójában növelték a szűrés költségeit anélkül, hogy javították volna a toxicitás esetének felismerését.27
Mások ugyanakkor felvetették, hogy egyes betegek eltérőek lehetnek a különböző vizsgálatokra való látszólagos érzékenységükben, és ezért a többféle módszerrel végzett gondos szűrés valószínűleg növeli a diagnosztikai hozamot a toxicitás felismerésében az irreverzibilis strukturális/funkcionális károsodás kialakulása előtt.7 Dr. Michael Marmor és Dr. Ronald Melles a közelmúltban 11 betegből álló, az ismert HCQ-toxicitású betegek 10 százalékát képviselő alcsoportban mutatták be ennek a sokoldalú megközelítésnek a szükségességét. Ez a kohorsz patognomikus 10-2-es mezőveszteséget mutatott ki markáns parafoveális gyűrűs szkotómákkal, amelyek erősen retinopátiára utaltak; ugyanakkor az SD-OCT-képalkotáson nem mutattak strukturális károsodásra utaló jeleket.28 A szerzők hangsúlyozták, hogy a HCQ-szűréssel kapcsolatban széleskörű megközelítést kell alkalmazni, nem szabad kizárólag egyetlen eljárásra támaszkodni, és minden kétértelmű eredményt további megerősítő vizsgálatokkal kell nyomon követni.
Jövőbeli irányok
Az adaptív optikai képalkotás megjelenése lehetővé tette a kúpok fotoreceptor-mozaikjának in vivo, ≤ 2 µm-es felbontású vizualizálását a szemoptikai aberrációk kompenzálásával.29-31 E technológia alkalmazásával különböző retinabetegségeknél olyan fotoreceptor-rendellenességeket fedeztek fel, amelyek egyébként SD-OCT-képalkotással nem voltak észlelhetők.32,33
Az adaptív optika alkalmazása a HCQ retinopátiában viszonylag új. Dr. Kimberly E. Stepien és munkatársai két, hosszú távú HCQ-terápiában részesülő betegnél kimutatták a kúpok fotoreceptor-mozaikjának zavarát a HVF 10-2 hibáknak és az SD-OCT ellipszoid zóna rendellenességeinek megfelelő területeken.33 Hasonlóképpen, koreai kutatók egy bikaszem-makulopátiában szenvedő betegnél is megfigyelték a kúpok mozaikjának zavarát, ahol az egyes kúpok szabálytalan alakúak és méretűek voltak.34 Emellett a foveális centrumtól különböző távolságokban lévő összes előre meghatározott vizsgálati ponton csökkent a mért kúpsűrűség. Összességében mindkét csoport javasolta, hogy az AO nem invazív, kvantitatív, nagy felbontású modalitást biztosít a HCQ retinopátiás betegek képalkotására, és lehetővé teheti az objektív látótérvesztést megelőző szubklinikai rendellenességek kimutatását. Nagyobb léptékű vizsgálatokra van szükség ezen eredmények validálásához.
A közelmúltban két csoport is leírta a mikroperimetriás rendszerek használatát a korai HCQ-toxicitás értékelésére.35,36 A perimetria egyidejű szemfenéki vizualizáció mellett történő vizsgálatával pontos anatómiai korrelátumot kaphatunk a funkcionális aberrációhoz.35 Lucia Martinez-Costa és munkatársai jelentős különbségeket figyeltek meg a mikroperimetriás retinaérzékenységi mérésekben 209 HCQ-t vagy klorokint szedő beteg és 204 kontrollszemély között.36 Dr. Renu Jivrajka és munkatársai 16, több mint öt éve HCQ-terápiában részesülő betegből álló kohorszban részletezték megállapításaikat, akiknél a hagyományos 10-2 HVF, SD-OCT, FAF vagy mfERG vizsgálat során nem mutatkoztak toxicitás jelei; mikroperimetriával azonban az átlagos retinaérzékenység jelentős általános csökkenését észlelték a betegek és az életkorban hasonló kontrollcsoportok között.35 Az alkalmazott mikroperimetriás rendszer további előnye volt, hogy képes volt egyidejű SD-OCT-felvételek készítésére és a retina érzékenységi és vastagsági értékeinek egymásra helyezésére, ami tovább erősítette a funkcionális válasz anatómiai struktúrával való korrelációjának gondolatát. A jövőben prospektív longitudinális vizsgálatokra van szükség, sorozatos mikroperimetriás vizsgálatokkal, annak pontosabb meghatározása érdekében, hogy a csökkent retinaérzékenységek valóban korai szubklinikai HCQ-toxicitást jelentenek-e.
A hidroxiklorokin értékes gyógyszer, amelynek összességében alacsony a mellékhatásprofilja. Bár az okuláris toxikus hatások ritkák, jelentős és irreverzibilis betegmorbiditással járhatnak. A toxicitás korai felismerése a szubklinikai stádiumban a gyógyszer abbahagyásával segíthet megelőzni a további strukturális és funkcionális romlást. Ezért a klinikusoknak alacsony küszöbértéket kell fenntartaniuk a HCQ-toxicitás gyanújára. Az egyik modalitással észlelt finom eltérések további utóvizsgálatokat indokolnak a leletek megerősítése vagy megcáfolása érdekében, a végső cél a korai diagnózis felállítása a visszafordíthatatlan látásvesztés előtt. Áttekintés
A 4. ábra a következő forrásból származik: Lyons JS, Severns ML. A korai hidroxiklorokin retinatoxicitás kimutatása a multifokális elektroretinográfia gyűrűarány-elemzésével javítva. Am J Ophthalmol 2007. May;143(5):801-809.
Dr. Rahimy másodéves ösztöndíjas a Wills Eye Hospitalban és a Thomas Jefferson University School of Medicine szemészeti klinikai oktatója. Dr. Vander a Wills Szemkórház retinaszolgálatának kezelőorvosa és a Thomas Jefferson University School of Medicine szemészprofesszora. Dr. Rahimy a [email protected] címen érhető el. Dr. Vander a jvander@midatlantic retina.com.
1 címen érhető el. Tehrani R, Ostrowski RA, Hariman R, Jay WM. A hidroxiklorokvin szemtoxicitása. Semin Ophthalmol 2008;23(3):201-209.
2. Semmer AE, Lee MS, Harrison AR, Olsen TW. A hidroxiklorokvin retinopátia szűrése. Br J Ophthalmol 2008;92(12): 1653-1655.
3. Wolfe F, Marmor MF. A hidroxiklorokvin retinatoxicitás aránya és előrejelzői rheumatoid arthritisben és szisztémás lupus erythematosusban szenvedő betegeknél. Arthritis Care Res (Hoboken) 2010;62(6):775-784.
4. Marmor MF, Kellner U, Lai TY, Lyons JS, Mieler WF. A klorokvin és hidroxiklorokvin retinopátia szűrésére vonatkozó felülvizsgált ajánlások. Ophthalmology 2011;118:415-422.
5. Michaelides M, Stover NB, Francis PJ, Weleber RG. A hidroxiklorokin és a klorokin okozta retinatoxicitás: Kockázati tényezők, szűrés és progresszió a terápia abbahagyása ellenére. Arch Ophthalmol 2011;129:30-39.
6. Mititelu M, Wong BJ, Brenner M, Bryar PJ, Jampol LM, Fawzi AA. A hidroxiklorokvin toxikus hatásainak progressziója a gyógyszeres terápia abbahagyása után: Új bizonyítékok a multimodális képalkotásból. JAMA Ophthalmol 2013;131:1187-1197.
7. Marmor MF. A hidroxiklorokvin-toxicitás szűrési eljárásainak összehasonlítása. Arch Ophthalmol 2012;130:461-469.
8. Elder M, Rahman AM, McLay J. Early paracentral visual field loss in patients taking hydroxychloroquine. Arch Ophthalmol 2006;124:1729-1733.
9. Marmor MF, Carr RE, Easterbrook M, Farjo AA, Mieler WF. A klorokvin és hidroxiklorokvin retinopátia szűrésére vonatkozó ajánlások: Az Amerikai Szemészeti Akadémia jelentése. Ophthalmology 2002;109:1377-1382.
10. Kellner S, Weinitz S, Kellner U. Spectral domain optical coherence tomography detects early stages of chloroquine retinopathy similar to multifocal electroretinography, fundus autofluorescence and near-infrared autofluorescence. Br J Ophthalmol 2009;93(11):1444-1447.
11. Chen E, Brown DM, Benz MS, et al. Spectral domain optical coherence tomography as an effective screening test for hydroxychloroquine retinopathy (the “flying saucer” sign). Clin Ophthalmol 2010;4:1151-1158.
12. Pasadhika S, Fishman GA, Choi D, Shahidi M. A perifoveális belső retina szelektív elvékonyodása mint a hidroxiklorokvin retinatoxicitás korai jele. Eye (Lond) 2010;24(5):756-762; quiz 763.
13. Pasadhika S, Fishman GA. A hidroxiklorokin vagy klorokin krónikus expozíciójának hatása a retina belső struktúráira. Eye (Lond) 2010;24(2):340-346.
14. Ulviye Y, Betul T, Nur TH, Selda C. Spectral domain optical coherence tomography for early detection of retinal alterations in patients using hydroxychloroquine. Indian J Ophthalmol 2013;61(4):168-171.
15. Kennedy CJ, Rakoczy PE, Constable IJ. A retina pigment epitheliumának lipofuscinja: A review. Eye (Lond) 1995;9 ( Pt 6)):763-771.
16. Okubo A, Rosa RH, Jr., Bunce CV, et al. A retinális pigment epithelium és a Bruch-membrán életkori változásainak összefüggései. Invest Ophthalmol Vis Sci 1999;40(2):443-449.
17. Holz FG, Bellman C, Staudt S, Schutt F, Volcker HE. Fundus autofluoreszcencia és a földrajzi atrófia kialakulása időskori makuladegenerációban. Invest Ophthalmol Vis Sci 2001;42(5):1051-1056.
18. Kellner U, Renner AB, Tillack H. Fundus autofluoreszcencia és mfERG a retina elváltozásainak korai kimutatására klorokint/hidroxiklorokint használó betegeknél. Invest Ophthalmol Vis Sci 2006;47(8):3531-3538.
19. Marmor MF. A fundus autofluoreszcencia nem a legjobb korai szűrővizsgálat a hidroxiklorokvin-toxicitásra. JAMA Ophthalmol 2013;131:1487-1488.
20. Lyons JS, Severns ML. A korai hidroxiklorokvin retinatoxicitás kimutatása a multifokális elektroretinográfia gyűrűarány-elemzésével javítva. Am J Ophthalmol 2007;143:801-809.
21. Maturi RK, Folk JC, Nichols B, Oetting TT, Kardon RH. Hydroxychloroquine retinopathia. Arch Ophthalmol 1999;117:1262-1263.
22. Lai TY, Chan WM, Li H, Lai RY, Lam DS. Multifokális elektroretinográfiás elváltozások hidroxiklorokvin-terápiában részesülő betegeknél. Am J Ophthalmol 2005;140:794-807.
23. Lai TY, Ngai JW, Chan WM, Lam DS. Látótér- és multifokális elektroretinográfia és ezek összefüggései hidroxiklorokvin-terápiában részesülő betegeknél. Doc Ophthalmol 2006;112(3):177-187.
24. Maturi RK, Yu M, Weleber RG. Hosszú távú hydroxychloroquin-használók multifokális elektroretinográfiás értékelése. Arch Ophthalmol 2004;122:973-981.
25. Lyons JS, Severns ML. A multifokális ERG gyűrűarányok használata a Plaquenil retinatoxicitás kimutatására és követésére: áttekintés : Review of mfERG ring ratios in Plaquenil toxicity. Doc Ophthalmol 2009;118(1):29-36.
26. Tzekov RT, Gerth C, Werner JS. Az emberi multifokális elektroretinogram komponenseinek szeneszcenciája: Egy lokalizált megközelítés. Graefes Arch Clin Exp Ophthalmol 2004;242(7):549-560.
27. Browning DJ. Az American Academy of Ophthalmology felülvizsgált, a hydroxychloroquine szűrésre vonatkozó irányelveinek hatása a tényleges gyakorlatra. Am J Ophthalmol 2013;155:418-428.e411.
28. Marmor MF, Melles RB. A látómezők és az optikai koherencia tomográfia közötti eltérés a hidroxiklorokvin retinopátiában. Ophthalmology 2014;121:1257-62.
29. Roorda A, Romero-Borja F, Donnelly Iii W, Queener H, Hebert T, Campbell M. Adaptív optikai pásztázó lézeres szemészeti vizsgálat. Opt Express 2002;10(9):405-412.
30. Park SP, Chung JK, Greenstein V, Tsang SH, Chang S. Az emberi kúp-fotoreceptorok sűrűségét befolyásoló tényezők vizsgálata adaptív optikai pásztázó lézerophthalmoszkóppal mérve. Exp Eye Res 2013;108:1-9.
31. Kim JE, Chung M. Adaptív optika a retina képalkotásához: Current status. Retina 2013;33:1483-1486.
32. Carroll J, Neitz M, Hofer H, Neitz J, Williams DR. Adaptív optikával feltárt funkcionális fotoreceptorveszteség: A színvakság alternatív oka. Proc Natl Acad Sci U S A 2004;101(22):8461-8466.
33. Stepien KE, Martinez WM, Dubis AM, Cooper RF, Dubra A, Carroll J. Subklinikai fotoreceptor-zavar súlyos fejsérülés hatására. Arch Ophthalmol 2012;130:400-402.
34. Bae EJ, Kim KR, Tsang SH, Park SP, Chang S. A retina károsodása klorokin makulopátiában, nagy felbontású képalkotással feltárva: Egy esettanulmány adaptív optikai pásztázó lézerophthalmoscopia alkalmazásával. Korean J Ophthalmol 2014;28(1):100-107.
35. Jivrajka RV, Genead MA, McAnany JJ, Chow CC, Mieler WF. Mikroperimetriás érzékenység hidroxiklorokvin (Plaquenil) terápiában részesülő betegeknél. Eye (Lond) 2013;27(9):1044-1052.
36. Martinez-Costa L, Victoria Ibanez M, Murcia-Bello C, et al. Mikroperimetria alkalmazása a hidroxiklorokvin és klorokvin retinatoxicitás értékelésére. Can J Ophthalmol 2013;48(5):400-405.