Generikus név: halobetasol propionát
Adagolási forma: krém
A Drugs.com által orvosilag felülvizsgált. Utolsó frissítés: 2020. április 21.
- Áttekintés
- Mellékhatások
- Adagolás
- Szakmai
- Ellenyomások
- Még
- Ultravate krém Leírás
- Ultravate krém – Klinikai farmakológia
- Farmakokinetika
- Az Ultravate krém indikációja és alkalmazása
- Ellenjavallatok
- Figyelmeztetések
- Általános
- Tájékoztatás a betegeknek
- Laborvizsgálatok
- Karcinogenezis, mutagenezis és a termékenység károsodása
- Vemhesség
- Szoptató anyák
- GYermekeknél történő alkalmazás
- Időskori alkalmazás
- Mellékhatások
- Túladagolás
- Ultravate krém adagolás és alkalmazás
- How is Ultravate Cream Supplied
- TÁROLÁS
- PAKOLÁSI JEGYZÉK.FŐTÁBLA TÁBLA
- Gyakran ismételt kérdések
- Többet az Ultravate (halobetazol topikális)
- Fogyasztói források
- Szakmai források
- Kapcsolódó kezelési útmutatók
Ultravate krém Leírás
Ultravate® (halobetasol propionát krém) krém, 0.05% halobetazol-propionátot, szintetikus kortikoszteroidot tartalmaz helyi bőrgyógyászati alkalmazásra. A kortikoszteroidok az elsősorban szintetikus szteroidok egy osztályát alkotják, amelyeket helyileg alkalmaznak gyulladáscsökkentő és viszketéscsillapító szerként.
Kémiailag a halobetazol-propionát 21-klór-6α, 9-difluor-11β, 17-dihidroxi-16β-metilpregna-1, 4-dien-3-20-dion, 17-propionát, C25H31ClF2O5. A következő szerkezeti képlettel rendelkezik:
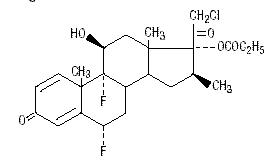
A halobetazol-propionát molekulatömege 485. Fehér, vízben nem oldódó kristályos por.
Az Ultravate krém minden grammja 0,5 mg/g halobetazol-propionátot tartalmaz cetil-alkohol, glicerin, izopropil-izosztearát, izopropil-palmitát, sztearet-21, diazolidinil-karbamid, metilklorizotiazolinon, (és) metilizotiazolinon és víz krémalapban.
Ultravate krém – Klinikai farmakológia
A többi helyi kortikoszteroidhoz hasonlóan a halobetazol-propionát gyulladáscsökkentő, viszketéscsillapító és érösszehúzó hatású. A helyi kortikoszteroidok gyulladáscsökkentő hatásának mechanizmusa általában nem világos. Úgy gondolják azonban, hogy a kortikoszteroidok a foszfolipáz A2 gátló fehérjék, az úgynevezett lipokortinok indukciója révén fejtik ki hatásukat. Feltételezések szerint ezek a fehérjék a gyulladás erős mediátorainak, például a prosztaglandinoknak és a leukotriéneknek a bioszintézisét szabályozzák azáltal, hogy gátolják közös prekurzoruk, az arachidonsav felszabadulását. Az arachidonsavat a foszfolipáz A2 szabadítja fel a membrán foszfolipidjeiből.
Farmakokinetika
A helyi kortikoszteroidok perkután felszívódásának mértékét számos tényező határozza meg, beleértve a hordozót és az epidermális gát integritását. A hidrokortizonnal legfeljebb 24 órán át alkalmazott okkluzív kötésekről nem bizonyították, hogy növelik a penetrációt; azonban a hidrokortizon 96 órán át történő okklúziója jelentősen fokozza a penetrációt. A helyi kortikoszteroidok felszívódhatnak a normál, ép bőrből. A bőr gyulladása és/vagy más betegségfolyamatok fokozhatják a perkután felszívódást.
Az emberen és állatokon végzett vizsgálatok azt mutatják, hogy a halobetazol-propionát alkalmazott dózisának kevesebb mint 6%-a kerül a keringésbe a krém helyileg történő alkalmazását követő 96 órán belül.
Az Ultravate krémmel végzett vizsgálatok azt mutatják, hogy a krém más helyi kortikoszteroidokkal összehasonlítva a szupernagy hatékonyságú tartományba tartozik.
Az Ultravate krém indikációja és alkalmazása
A 0,05%-os Ultravate krém szupernagy hatékonyságú kortikoszteroid, amely a kortikoszteroidokra reagáló bőrbetegségek gyulladásos és viszkető megnyilvánulásainak enyhítésére javallott. A két egymást követő héten túli kezelés nem ajánlott, és a teljes adag nem haladhatja meg az 50 g/hét értéket, mivel a gyógyszer elnyomhatja a hipotalamusz-hipofízis-mellékvese (HPA) tengelyt. Alkalmazása 12 év alatti gyermekeknél nem ajánlott.
A többi nagy aktivitású kortikoszteroidhoz hasonlóan a terápiát abba kell hagyni, ha a kontrollt sikerült elérni. Ha 2 héten belül nem tapasztalható javulás, a diagnózis újraértékelésére lehet szükség.
Ellenjavallatok
Az Ultravate krém ellenjavallt azoknál a betegeknél, akiknél a készítmény bármely összetevőjével szemben túlérzékenység áll fenn.
Figyelmeztetések
Általános
A helyi kortikoszteroidok szisztémás felszívódása reverzibilis hipotalamusz-hypophysis-mellékvese (HPA) tengely szuppressziót okozhat, ami a kezelés megvonása után glükokortikoszteroid-elégtelenség kialakulásának lehetőségével járhat. A Cushing-szindróma megnyilvánulásai, hiperglikémia és glükozuria is előidézhetők egyes betegeknél a lokális kortikoszteroidok szisztémás felszívódásával a kezelés alatt.
A lokális szteroidot nagy felületen vagy elzáródó területeken alkalmazó betegeket rendszeresen értékelni kell a HPA-tengely szuppressziójának jelei miatt. Ezt az ACTH-stimulációs, a.m. plazma kortizol és a vizelet szabad kortizol tesztek segítségével lehet elvégezni. A szupererős kortikoszteroidokat kapó betegeket nem szabad egyszerre 2 hétnél hosszabb ideig kezelni, és a HPA-szuppresszió fokozott kockázata miatt egyszerre csak kis területeket szabad kezelni.
A HPA-tengely szuppresszióját okozta az Ultravate Cream, amikor osztott adagokban, napi 7 grammos adagban, egy héten keresztül alkalmazták pikkelysömörben szenvedő betegeknél. Ezek a hatások a kezelés abbahagyásával visszafordíthatóak voltak.
Ha HPA tengely szuppressziót észlelnek, meg kell kísérelni a gyógyszer visszavonását, az alkalmazás gyakoriságának csökkentését vagy egy kevésbé hatásos kortikoszteroid helyettesítését. A HPA-tengely működésének helyreállása általában azonnal bekövetkezik a helyi kortikoszteroidok abbahagyását követően. Ritkán a glükokortikoszteroid-elégtelenség jelei és tünetei jelentkezhetnek, ami kiegészítő szisztémás kortikoszteroidok alkalmazását teszi szükségessé. A szisztémás kiegészítéssel kapcsolatos információkért lásd az adott készítmények alkalmazási előírását.
A gyermekbetegek a nagyobb bőrfelület/testtömeg arányuk miatt érzékenyebbek lehetnek az egyenértékű dózisok szisztémás toxicitására (lásd: ÓVALMASZKODÁSOK: Gyermekgyógyászati alkalmazás).
Irritáció kialakulása esetén az Ultravate krémet abba kell hagyni és megfelelő terápiát kell kezdeni. Az allergiás kontakt dermatitist kortikoszteroidokkal általában a gyógyulás elmaradásának megfigyelésével diagnosztizálják, nem pedig a klinikai exacerbáció észlelésével, mint a legtöbb, kortikoszteroidokat nem tartalmazó helyi készítmény esetében. Az ilyen megfigyelést megfelelő diagnosztikai tapaszvizsgálattal kell alátámasztani.
Ha egyidejűleg bőrfertőzések vannak jelen vagy alakulnak ki, megfelelő gombaölő vagy antibakteriális szert kell alkalmazni. Ha nem jelentkezik azonnal kedvező válasz, az Ultravate krém alkalmazását fel kell függeszteni, amíg a fertőzést megfelelően nem kontrollálják.
Az Ultravate krém nem alkalmazható rosacea vagy perioralis dermatitis kezelésére, és nem alkalmazható az arcon, az ágyékon vagy a hónaljban.
Tájékoztatás a betegeknek
A helyi kortikoszteroidokat alkalmazó betegeknek a következő információkat és utasításokat kell kapniuk:
- A gyógyszert az orvos utasításai szerint kell alkalmazni. Kizárólag külsőleg alkalmazható. Kerülje a szemmel való érintkezést.
- A gyógyszert nem szabad más betegségre használni, mint amire felírták.
- A kezelt bőrfelületet nem szabad bekötözni, más módon lefedni vagy becsomagolni, hogy az okkluzív legyen, kivéve, ha az orvos utasítása szerint.
- A betegeknek jelenteniük kell orvosuknak a helyi mellékhatások minden jelét.
Laborvizsgálatok
A következő vizsgálatok hasznosak lehetnek a betegek HPA tengely szuppressziójának értékelésében: ACTH-stimulációs teszt; A.M. plazma kortizol teszt; vizelet szabad kortizol teszt.
Karcinogenezis, mutagenezis és a termékenység károsodása
Hosszú távú állatkísérleteket nem végeztek a halobetazol-propionát karcinogén potenciáljának értékelésére. Két genotoxicitási vizsgálatban pozitív mutagén hatást figyeltek meg. A halobetazol-propionát pozitív volt a kínai hörcsög mikronukleusz tesztben és az egér limfóma génmutációs tesztben in vitro.
A patkányokon végzett vizsgálatok 50 µg/kg/nap dózisig terjedő orális adagolást követően nem jelezték a termékenység vagy az általános reprodukciós teljesítmény károsodását.
Egyéb genotoxicitási vizsgálatokban a halobetazol-propionát nem bizonyult genotoxikusnak az Ames/Salmonella tesztben, a kínai hörcsög szomatikus sejtjein végzett testvér kromatidcsere tesztben, rágcsálók csíra- és szomatikus sejtjein végzett kromoszóma-aberrációs vizsgálatokban, valamint a pontmutációk meghatározására szolgáló emlős spot tesztben.
Vemhesség
Teratogén hatások: C terhességi kategória
A kortikoszteroidok laboratóriumi állatokban teratogénnek bizonyultak, ha szisztémásan, viszonylag alacsony dózisban adták őket. Néhány kortikoszteroid teratogénnek bizonyult laboratóriumi állatokon bőrön történő alkalmazást követően.
A halobetazol-propionát teratogénnek bizonyult SPF patkányokban és csincsilla típusú nyulakban, ha szisztémásan adták vemhesség alatt 0,04-0,1 mg/kg dózisban patkányokban és 0,01 mg/kg dózisban nyulakban. Ezek a dózisok körülbelül 13, 33, illetve 3-szorosa az Ultravate krém humán helyi adagjának. A halobetazol-propionát nyulakban embriotoxikus volt, de patkányokban nem.
Patkányokban és nyulakban egyaránt szájpadhasadékot figyeltek meg. Omphalocele jelentkezett patkányoknál, de nyulaknál nem.
Nincsenek megfelelő és jól kontrollált vizsgálatok a halobetazol-propionát teratogén potenciáljáról terhes nőknél. Az Ultravate krém terhesség alatt csak akkor alkalmazható, ha a potenciális előny igazolja a magzatra jelentkező potenciális kockázatot.
Szoptató anyák
A szisztémásan alkalmazott kortikoszteroidok megjelennek az emberi tejben, és elnyomhatják a növekedést, befolyásolhatják az endogén kortikoszteroid termelést, vagy egyéb nemkívánatos hatásokat okozhatnak. Nem ismert, hogy a kortikoszteroidok helyi alkalmazása elegendő szisztémás felszívódást eredményezhet-e ahhoz, hogy kimutatható mennyiségek jelenjenek meg az emberi tejben. Mivel számos gyógyszer kiválasztódik az emberi tejbe, óvatosságra int, ha az Ultravate krémet szoptató nőnek adják.
GYermekeknél történő alkalmazás
Az Ultravate krém biztonságosságát és hatékonyságát gyermekbetegeknél nem állapították meg, és alkalmazása 12 év alatti gyermekbetegeknél nem javasolt. A bőrfelület és a testtömeg nagyobb aránya miatt a gyermekbetegeknél a felnőtteknél nagyobb a HPA-tengely szuppresszió és a Cushing-szindróma kockázata, ha helyi kortikoszteroidokkal kezelik őket. Ezért a kezelés megvonása során vagy azt követően is nagyobb a mellékvesekéreg-elégtelenség kockázata náluk. Csecsemőknél és gyermekeknél a helyi kortikoszteroidok nem megfelelő alkalmazása során mellékhatásokról, többek között striae-ról számoltak be.
HPA tengely szuppresszióról, Cushing-szindrómáról, lineáris növekedési elmaradásról, késleltetett súlygyarapodásról és intrakraniális hipertóniáról számoltak be helyi kortikoszteroidokat kapó gyermekeknél. A mellékvese-szuppresszió megnyilvánulásai gyermekeknél az alacsony plazma kortizolszintek és az ACTH-stimulációra adott válasz hiánya. Az intrakraniális hipertónia megnyilvánulásai közé tartoznak a kidudorodó fontanellák, a fejfájás és a kétoldali papillödéma.
Időskori alkalmazás
A klinikai vizsgálatokban Ultravate krémmel kezelt körülbelül 400 beteg 25%-a 61 éves vagy idősebb, 6%-a pedig 71 éves vagy idősebb volt. Nem észleltek általános különbséget a biztonságosság vagy a hatékonyság tekintetében ezen betegek és a fiatalabb betegek között; és más bejelentett klinikai tapasztalatok nem azonosítottak különbséget az idős és a fiatalabb betegek közötti válaszreakciókban, de nem zárható ki egyes idősebb egyének nagyobb érzékenysége.
Mellékhatások
A kontrollált klinikai vizsgálatokban az Ultravate krém esetében a leggyakrabban jelentett mellékhatások között a csípés, égés vagy viszketés szerepelt a betegek 4,4%-ánál. Ritkábban jelentett mellékhatások voltak a száraz bőr, az erythema, a bőr atrófiája, a leukoderma, a hólyagok és a kiütés.
A következő további helyi mellékhatásokat jelentették ritkán a helyi kortikoszteroidokkal kapcsolatban, és gyakrabban fordulhatnak elő nagy hatású kortikoszteroidok, például az Ultravate krém esetében. Ezeket a reakciókat az előfordulásuk megközelítőleg csökkenő sorrendjében soroljuk fel: folliculitis, hypertrichosis, akneiform kiütések, hypopigmentáció, perioralis dermatitis, allergiás kontakt dermatitis, másodlagos fertőzés, striae és miliaria.
Túladagolás
A helyileg alkalmazott Ultravate krém elegendő mennyiségben felszívódhat ahhoz, hogy szisztémás hatást fejtsen ki (lásdMEGHATÁSOK).
Ultravate krém adagolás és alkalmazás
A kezelőorvos utasítása szerint naponta egyszer vagy kétszer vékony rétegben kenje fel az Ultravate krémet az érintett bőrfelületre, és finoman, teljesen dörzsölje be.
Az Ultravate (halobetazol-propionát krém) krém egy szuper-nagyhatású helyi kortikoszteroid, ezért a kezelést két hétre kell korlátozni, és 50 g/hétnél nagyobb mennyiség nem alkalmazható. A többi kortikoszteroidhoz hasonlóan a kezelést abba kell hagyni, ha a kontrollt sikerült elérni. Ha 2 héten belül nem tapasztalható javulás, szükség lehet a diagnózis újraértékelésére.
Az Ultravate krém nem alkalmazható okkluzív kötésekkel.
How is Ultravate Cream Supplied
Ultravate® (halobetasol propionát krém) krém, 0.05% a következő tubusméretekben kerül forgalomba:
15 g (NDC 10631-103-15)
50 g (NDC 10631-103-50)
TÁROLÁS
15°C és 30°C (59°F és 86°F) között kell tárolni.
RANBAXY
Jacksonville, FL 32257 USA
09-0085 (lapos), 09-0086 (hajtogatott)
Újrafogalmazva 2010. május
PAKOLÁSI JEGYZÉK.FŐTÁBLA TÁBLA

15 grammos dobozcímke

15 grammos kartoncímke

50 grammos dobozcímke

50 grammos kartoncímke
| ULTRAVATE halobetasol propionát krém |
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
Címke – Ranbaxy Laboratories Inc. (169932519)
Regisztráló – Ranbaxy Laboratories Inc. (169932519)
| Egység | |||
| Név | Adress | ID/FEI | Operations |
| Contract Pharmaceuticals Limited | 248761249 | gyártás | |
Gyakran ismételt kérdések
- Halobetazol vs. clobetazol – hogyan hasonlíthatók össze?
- Ez használható mérges szömörce ellen?
- A fejbőrön is alkalmazható?
Többet az Ultravate (halobetazol topikális)
- Mellékhatások
- Terhesség vagy szoptatás alatt
- Adagolás Információk
- Gyógyszerkölcsönhatások
- Árképzés & Kuponok
- En Español
- 6 Vélemények
- Generikus elérhetőség
- Gyógyszercsoport:
Fogyasztói források
- Betegtájékoztatás
- Ultravate (Korszerű olvasás)
Szakmai források
- Receptköteles információk
Egyéb márkák Lexette, Bryhali, Halonate
Kapcsolódó kezelési útmutatók
- Psoriasis
- Atopic Dermatitis
- Dermatitis
- Eczema
Egészségügyi nyilatkozat