一般名:プロピオン酸ハロベタゾール
剤形:クリーム
医薬品のレビュー: Drugs.jp.com. 最終更新日:2020年4月21日
- 概要
- 副作用
- 用法用量
- 専門家
- 相互作用
- その他
- Ultravate Cream Description
- Ultravate Cream – Clinical Pharmacology
- 薬物動態
- ウルトラベイトクリームの効能・効果
- 禁忌
- 使用上の注意
- 一般的な注意
- 患者への情報
- 臨床検査
- 発がん性、変異原性、生殖能力障害
- Pregnancy
- 授乳婦
- 小児用
- 高齢者の使用
- 有害反応
- ウルトラベイトクリームの用法・用量
- ウルトラベイトクリームの用法・用量は、医師の指示のもとで使用する。 他のコルチコステロイドと同様に、コントロールが得られたら治療を中止すること。
- ウルトラベイトクリームの供給方法
- 保管
- PACKAGE LABEL.BOX
- よくある質問
- よくある質問 よくある質問5337
- ウルトラベイト(ハロベタゾール外用剤)の詳細
- Consumer resources
- プロフェッショナルリソース
- 関連治療ガイド
Ultravate Cream Description
ウルトラベート®(ハロベタソルプロピオン酸クリーム)クリーム、0.05%は、皮膚外用合成副腎皮質ホルモン剤であるハロベタゾールプロピオン酸塩を含有しています。 副腎皮質ステロイドは、抗炎症剤および鎮痒剤として局所的に使用される主に合成ステロイドのクラスを構成します。
化学的にハロベタゾールプロピオネートは、21-クロロ-6α、9-ジフルオロ-11-β、17-ジヒドロキシ-16-メチルプレグナ-1、4-ジエン-3-20-ジオン、17-プロピオン酸、C25H31ClF2O5です。 それは次の構造式を有する:
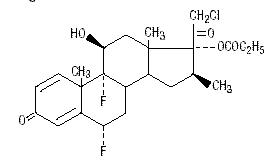
Halobetasol propionateは、485の分子量を有する。 604>
Ultravate Cream 1gあたり、セチルアルコール、グリセリン、イソステアリン酸イソプロピル、パルミチン酸イソプロピル、ステアレス-21、ジアゾリジニル尿素、メチルクロルイソチアゾリノン、(および)メチルイソチアゾリノンおよび水のクリーム基剤に0.5mg/gのハロベタソルプロピオンを含む。
Ultravate Cream – Clinical Pharmacology
他の局所副腎皮質ホルモンと同様に、プロピオン酸ハロベタゾールは抗炎症、鎮痒、血管収縮の作用があります。 一般に、副腎皮質ステロイド外用薬の抗炎症作用のメカニズムは不明である。 しかし、副腎皮質ステロイドは、リポコルチンと総称されるホスホリパーゼA2阻害蛋白の誘導により作用すると考えられている。 これらのタンパク質は、プロスタグランジンやロイコトリエンなどの炎症の強力な仲介物質の生合成を、それらの共通の前駆体であるアラキドン酸の放出を阻害することによって制御していると推測されている。 アラキドン酸はホスホリパーゼA2によって膜リン脂質から放出される。
薬物動態
局所コルチコステロイドの経皮吸収の程度は、薬剤や表皮障壁の完全性など多くの要因によって決定される。 ハイドロコルチゾンを用いた24時間までの閉塞ドレッシングは、浸透性を高めることが実証されていない;しかしながら、ハイドロコルチゾンを96時間閉塞すると、浸透性が著しく向上する。 局所用コルチコステロイドは、正常な無傷の皮膚から吸収されうる。 皮膚における炎症および/または他の疾患過程は、経皮吸収を増加させる可能性がある。
ヒトおよび動物試験は、クリームの局所投与後96時間以内に循環に入るハロベタゾールプロピオネートの適用量の6%未満であることを示している。
ウルトラベイトクリームは、他の副腎皮質ホルモン外用薬と比較して、超高活性領域であることが示されています。
ウルトラベイトクリームの効能・効果
ウルトラベイトクリーム0.05%は超高活性の副腎皮質ホルモンで、副腎皮質ホルモン反応性皮膚疾患の炎症やかゆみの緩和に適応されます。 本剤は視床下部-下垂体-副腎(HPA)軸を抑制する可能性があるため、連続2週間を超える投与は推奨されず、総投与量は50g/週を超えてはならない。 12歳未満の小児への使用は推奨されない。
他の高活性コルチコステロイドと同様に、コントロールが達成された時点で治療を中止すること。
禁忌
ウルトラベイトクリームは、本剤の成分に対して過敏症の既往歴のある患者には禁忌とされています。
使用上の注意
一般的な注意
外用コルチコステロイドの全身吸収は、治療中止後に副腎皮質ステロイド不全の可能性を伴う可逆性の視床下部-下垂体-副腎(HPA)軸抑制を生じる可能性がある。
広い表面積または閉塞部位にステロイド外用剤を塗布している患者は、HPA軸抑制の証拠を定期的に評価すべきである。 これは、ACTH刺激、午前中の血漿コルチゾール、および尿中遊離コルチゾールテストを使用することによって行うことができる。
ウルトラベートクリームは、乾癬患者において1日7gを1週間分割して使用したところ、HPA軸抑制を引き起こした。
HPA軸の抑制が認められた場合、薬剤の中止、塗布頻度の減少、より作用の弱いコルチコステロイドの代替を試みるべきである。 HPA軸機能の回復は、一般に局所的なコルチコステロイドの中止により速やかに起こる。 まれに、副腎皮質ホルモン機能不全の徴候および症状が現れ、全身性副腎皮質ホルモンの補充が必要となることがあります。
小児患者は、体格に対する皮膚表面の比率が大きいため、同等の用量でより全身毒性を受けやすい場合があります(注意:小児用を参照)
刺激が生じた場合、ウルトラベイトクリームを中止して適切な治療を行う必要があります。 副腎皮質ホルモンによるアレルギー性接触皮膚炎は通常、副腎皮質ホルモンを含まないほとんどの外用剤のように臨床的な悪化を指摘するよりも、むしろ治癒しないことを観察することによって診断される。 このような観察は、適切な診断的パッチテストで裏付けされるべきである。
皮膚感染症を併発した場合は、適切な抗真菌剤または抗菌剤が使用されるべきである。
ウルトラベイトクリームは酒さ、口周囲皮膚炎の治療には使用せず、顔面、鼠径部、腋窩には使用しないでください。
患者への情報
外用副腎皮質ホルモン剤を使用する患者には、以下の情報および指示を与えてください:
- 薬は、医師の指示に従って使用することです。 外用にのみ使用します。
- この薬は処方された疾患以外には使用しないでください。
- 治療した皮膚部位は、医師の指示がない限り、閉塞するように包帯、その他のカバーまたはラップをしてはいけません。
- 患者は局所副作用の兆候を医師に報告すること。
臨床検査
以下の検査がHPA軸抑制の患者評価に有用であろう。 ACTH刺激試験、午前中血漿コルチゾール試験、尿中遊離コルチゾール試験
発がん性、変異原性、生殖能力障害
ハロベタゾールプロピオネートの発がん性を評価するための長期動物試験は行われていない。 2つの遺伝毒性試験で正の変異原性作用が観察されました。
ラットを用いた50μg/kg/日までの経口投与試験では、受胎能力および一般的な生殖能力への障害は認められませんでした。
その他の遺伝毒性試験において、プロピオン酸ハロベタゾールは、Ames/Salmonella試験、チャイニーズハムスターの体細胞における姉妹染色体交換試験、ネズミの生殖細胞および体細胞の染色体異常試験、および点突然変異を判定する哺乳類スポット試験では遺伝毒性が認められません
Pregnancy
催奇形性を有すること。 妊娠のカテゴリーC
副腎皮質ホルモンは、比較的低い投与量で全身投与した場合、実験動物で催奇形性があることが示されています。
プロピオン酸ハロベタゾールは、SPFラットおよびチンチラ系ウサギにおいて、ラットでは0.04~0.1mg/kg、ウサギでは0.01mg/kgの用量で妊娠中に全身投与すると催奇形性を示すことが報告されています。 これらの用量は、ウルトラベイトクリームのヒト外用量のそれぞれ約13、33、3倍である。 プロピオン酸ハロベタゾールはウサギで胚毒性を示したが、ラットでは示さなかった。
ラット及びウサギの両方で口蓋裂が観察された。
妊娠中の女性におけるプロピオン酸ハロベタゾールの催奇形性の適切かつ良好な対照試験は存在しない。
授乳婦
全身投与されたコルチコステロイドはヒト乳汁中に現れ、成長を抑制し、内因性コルチコステロイドの生産を妨害し、または他の不都合な効果を引き起こす可能性があります。 副腎皮質ステロイドの局所投与が、ヒトの乳汁中に検出可能な量を生み出すのに十分な全身吸収をもたらすかどうかは不明である。
小児用
小児患者におけるウルトラベイトクリームの安全性および有効性は確立しておらず、12歳未満の小児患者への使用は推奨されません。 小児患者は、体重に対する皮膚表面積の割合が高いため、副腎皮質ステロイド外用剤で治療した場合、成人よりもHPA軸抑制やクッシング症候群のリスクが高くなります。 したがって、治療中または治療中止後に副腎機能不全になるリスクも高くなります。 604>
HPA 軸抑制、クッシング症候群、線状成長遅延、体重増加遅延、頭蓋内圧亢進は、副腎皮質ステロイド外用剤を投与されている小児で報告されています。 小児における副腎抑制の症状には、血漿コルチゾール値の低下とACTH刺激に対する反応の欠如が含まれる。
高齢者の使用
臨床試験でウルトラベイトクリームを使用した約400名の患者のうち、25%が61歳以上、6%が71歳以上であった。 また、他の報告されている臨床経験では、高齢者と若年者の反応の違いは確認されていませんが、一部の高齢者の感受性が高いことは否定できません。
有害反応
対照臨床試験において、ウルトラヴェイトクリームで最も頻繁に報告された有害事象は、刺痛、熱感、かゆみで4.
以下の追加的な局所副作用は、局所コルチコステロイドでまれに報告されており、ウルトラベイトクリームのような高活性コルチコステロイドでより頻繁に発生する可能性があります。 毛包炎、多毛症、にきび様発疹症、色素沈着、口腔周囲皮膚炎、アレルギー性接触皮膚炎、二次感染、線条および粟粒です。
ウルトラベイトクリームの用法・用量
医師の指示に従い、1日1~2回、患部の皮膚にウルトラベイトクリームを薄く塗り、軽く完全にすり込む
ウルトラベイト(ハロベタゾールプロピオン酸塩クリーム)クリームは超高活性の局所コルチコステロイドなので、治療は2週間までにし、50g/週以上の量は使用しないこと
ウルトラベイトクリームの用法・用量は、医師の指示のもとで使用する。 他のコルチコステロイドと同様に、コントロールが得られたら治療を中止すること。
ウルトラベイトクリームは閉塞性包帯と併用してはならない。
ウルトラベイトクリームの供給方法
ウルトラベイト®(ハロベタゾールプロピオン酸塩クリーム)クリーム、0.05%は、以下のチューブサイズで提供されています:
15g (NDC 10631-103-15)
50g (NDC 10631-103-50)
保管
15℃~30℃(59°F~86°F)で保管してください。
RANBAXY
Jacksonville, FL 32257 USA
09-0085 (Flat), 09-0086 (Folded)
Revised May 2010
PACKAGE LABEL.BOX
PACKAGE LABEL.PRINCIPAL DISPLAY PANEL

15g コンテナラベル

15g カートンラベル

50g コンテナラベル

50g カートンラベル
| ULTRAVATE halobetasol propionate cream |
||||||||||||||
|
||||||||||||||
|
||||||||||||||
|
||||||||||||||
|
||||||||||||||
|
||||||||||||||
ラベラー-。 ランバクシー・ラボラトリーズ・インク (169932519)
登録者-ランバクシー・ラボラトリーズ・インク(Ranbaxy Laboratories Inc. (169932519)
| Establishment | |||
| 名前 | 住所 | ID/FEI | 運営 |
| Contract Pharmaceuticals Limited | 248761249 | 製造 | |
よくある質問
- ハロベタゾールとクロベタゾールの比較
- ウルシに使えますか
- 頭皮に使えますか
- ウルシに使えますか
- 頭皮に使えますか
よくある質問
よくある質問5337
ウルトラベイト(ハロベタゾール外用剤)の詳細
- 副作用
- 妊娠中・授乳中
- 用法・用量について 情報
- 薬物相互作用
- 価格 & クーポン
- En Español
- 6 レビュー
- ジェネリック医薬品
- 薬効分類: ステロイド外用剤
Consumer resources
- 患者情報
- Ultravate (Advanced Reading)
プロフェッショナルリソース
- 処方情報
他のブランドLexette, ブライハリ、ハロン酸
関連治療ガイド
- 乾癬
- アトピー性皮膚炎
- 皮膚炎
- 湿疹
医療上の注意点