Generischer Name: Halobetasolpropionat
Dosierung Form: Creme
Medically reviewed by Drugs.com. Zuletzt aktualisiert am 21. April 2020.
- Übersicht
- Nebenwirkungen
- Dosierung
- Beratung
- Interaktionen
- Mehr
- Ultravate Creme Beschreibung
- Ultravate Creme – Klinische Pharmakologie
- Pharmakokinetik
- Indikationen und Anwendung von Ultravate Creme
- Kontraindikationen
- Vorsichtsmaßnahmen
- Allgemein
- Informationen für Patienten
- Laboruntersuchungen
- Karzinogenese, Mutagenese und Beeinträchtigung der Fruchtbarkeit
- Schwangerschaft
- Stillende Mütter
- Anwendung bei Kindern
- Geriatrische Anwendung
- Nebenwirkungen
- Überdosierung
- Ultravate Creme Dosierung und Anwendung
- Wie wird Ultravate Creme geliefert
- Lagerung
- PACKUNGSEtikett.HAUPTANZEIGEPLATTE
- Häufig gestellte Fragen
- Mehr über Ultravate (Halobetasol topisch)
- Ressourcen für Verbraucher
- Ressourcen für Fachleute
- Verwandte Behandlungsleitfäden
Ultravate Creme Beschreibung
Ultravate® (Halobetasolpropionat Creme) Creme, 0.05% enthält Halobetasolpropionat, ein synthetisches Kortikosteroid zur topischen Anwendung in der Dermatologie. Die Kortikosteroide bilden eine Klasse von hauptsächlich synthetischen Steroiden, die topisch als entzündungshemmendes und juckreizstillendes Mittel verwendet werden.
Chemisch gesehen ist Halobetasolpropionat 21-Chlor-6α, 9-difluor-11β, 17-dihydroxy-16β-methylpregna-1, 4-dien-3-20-dion, 17-propionat, C25H31ClF2O5. Es hat die folgende Strukturformel:
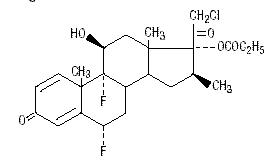
Halobetasolpropionat hat das Molekulargewicht von 485. Es ist ein weißes kristallines Pulver, das in Wasser unlöslich ist.
Jedes Gramm Ultravate Creme enthält 0,5 mg/g Halobetasolpropionat in einer Cremegrundlage aus Cetylalkohol, Glycerin, Isopropylisostearat, Isopropylpalmitat, Steareth-21, Diazolidinylharnstoff, Methylchlorisothiazolinon (und) Methylisothiazolinon und Wasser.
Ultravate Creme – Klinische Pharmakologie
Wie andere topische Kortikosteroide hat Halobetasolpropionat entzündungshemmende, juckreizstillende und gefäßverengende Eigenschaften. Der Mechanismus der entzündungshemmenden Wirkung der topischen Kortikosteroide ist im Allgemeinen unklar. Es wird jedoch angenommen, dass Kortikosteroide durch die Induktion von Phospholipase-A2 hemmenden Proteinen, die als Lipocortine bezeichnet werden, wirken. Es wird angenommen, dass diese Proteine die Biosynthese potenter Entzündungsmediatoren wie Prostaglandine und Leukotriene kontrollieren, indem sie die Freisetzung ihrer gemeinsamen Vorstufe Arachidonsäure hemmen. Arachidonsäure wird durch Phospholipase A2 aus Membranphospholipiden freigesetzt.
Pharmakokinetik
Das Ausmaß der perkutanen Absorption topischer Kortikosteroide wird durch viele Faktoren bestimmt, darunter das Vehikel und die Integrität der epidermalen Barriere. Okklusivverbände mit Hydrocortison für bis zu 24 Stunden erhöhen die Penetration nachweislich nicht; eine Okklusion von Hydrocortison für 96 Stunden erhöht die Penetration jedoch deutlich. Topische Kortikosteroide können von normaler, intakter Haut absorbiert werden. Entzündungen und/oder andere Krankheitsprozesse in der Haut können die perkutane Absorption erhöhen.
Human- und Tierstudien deuten darauf hin, dass weniger als 6 % der aufgetragenen Dosis von Halobetasolpropionat innerhalb von 96 Stunden nach topischer Anwendung der Creme in den Blutkreislauf gelangen.
Studien, die mit Ultravate Creme durchgeführt wurden, deuten darauf hin, dass es sich im Vergleich zu anderen topischen Kortikosteroiden im Bereich der Superhochpotenz befindet.
Indikationen und Anwendung von Ultravate Creme
Ultravate Creme 0,05% ist ein Superhochpotenz-Kortikosteroid, das zur Linderung der entzündlichen und juckenden Manifestationen von auf Kortikosteroid reagierenden Dermatosen angezeigt ist. Eine Behandlung über zwei aufeinanderfolgende Wochen hinaus wird nicht empfohlen, und die Gesamtdosis sollte 50 g/Woche nicht überschreiten, da das Arzneimittel die Hypothalamus-Hypophysen-Nebennieren-Achse (HPA) unterdrücken kann. Die Anwendung bei Kindern unter 12 Jahren wird nicht empfohlen.
Wie bei anderen hochwirksamen Kortikosteroiden sollte die Therapie abgesetzt werden, wenn eine Kontrolle erreicht wurde. Wenn innerhalb von 2 Wochen keine Besserung eintritt, kann eine Neubewertung der Diagnose erforderlich sein.
Kontraindikationen
Ultravate Creme ist bei Patienten mit einer Überempfindlichkeit gegen einen der Bestandteile des Präparates kontraindiziert.
Vorsichtsmaßnahmen
Allgemein
Die systemische Absorption von topischen Kortikosteroiden kann zu einer reversiblen Suppression der Hypothalamus-Hypophysen-Nebennieren-Achse (HPA) führen, die nach Absetzen der Behandlung zu einer Glukokortikosteroid-Insuffizienz führen kann. Manifestationen des Cushing-Syndroms, Hyperglykämie und Glukosurie können bei einigen Patienten auch durch die systemische Absorption von topischen Kortikosteroiden während der Behandlung hervorgerufen werden.
Patienten, die ein topisches Steroid großflächig oder auf verschlossene Bereiche auftragen, sollten regelmäßig auf Anzeichen einer Unterdrückung der HPA-Achse untersucht werden. Dies kann mit Hilfe des ACTH-Stimulationstests, des A.M.-Plasmacortisols und des freien Cortisols im Urin erfolgen. Patienten, die hochwirksame Kortikosteroide erhalten, sollten nicht länger als 2 Wochen am Stück behandelt werden, und wegen des erhöhten Risikos einer HPA-Suppression sollten jeweils nur kleine Bereiche behandelt werden.
Ultravat-Creme erzeugte eine HPA-Achsen-Suppression, wenn sie in geteilten Dosen von 7 Gramm pro Tag eine Woche lang bei Patienten mit Psoriasis angewendet wurde. Diese Effekte waren nach Absetzen der Behandlung reversibel.
Wenn eine Unterdrückung der HPA-Achse festgestellt wird, sollte versucht werden, das Medikament abzusetzen, die Häufigkeit der Anwendung zu verringern oder ein weniger starkes Kortikosteroid zu ersetzen. Die Funktion der HPA-Achse erholt sich im Allgemeinen sofort nach Absetzen der topischen Kortikosteroide. In seltenen Fällen können Anzeichen und Symptome einer Glukokortikosteroid-Insuffizienz auftreten, die eine zusätzliche systemische Kortikosteroidbehandlung erforderlich machen. Informationen zur systemischen Ergänzung finden Sie in der Gebrauchsinformation dieser Produkte.
Pädiatrische Patienten können aufgrund ihres größeren Verhältnisses von Hautoberfläche zu Körpermasse anfälliger für systemische Toxizität bei äquivalenten Dosen sein (siehe VORSICHTSMASSNAHMEN: Anwendung bei Kindern).
Wenn eine Reizung auftritt, sollte Ultravate Creme abgesetzt und eine geeignete Therapie eingeleitet werden. Eine allergische Kontaktdermatitis mit Kortikosteroiden wird in der Regel durch die Beobachtung einer fehlenden Abheilung diagnostiziert und nicht durch die Feststellung einer klinischen Verschlimmerung wie bei den meisten topischen Produkten, die keine Kortikosteroide enthalten. Eine solche Beobachtung sollte durch geeignete diagnostische Pflastertests bestätigt werden.
Wenn gleichzeitig Hautinfektionen vorhanden sind oder sich entwickeln, sollte ein geeignetes antimykotisches oder antibakterielles Mittel verwendet werden. Wenn eine günstige Reaktion nicht sofort eintritt, sollte die Anwendung von Ultravate Creme unterbrochen werden, bis die Infektion ausreichend kontrolliert wurde.
Ultravate Creme sollte nicht zur Behandlung von Rosacea oder perioraler Dermatitis verwendet werden, und sie sollte nicht im Gesicht, in der Leiste oder in den Achselhöhlen angewendet werden.
Informationen für Patienten
Patienten, die topische Kortikosteroide anwenden, sollten die folgenden Informationen und Anweisungen erhalten:
- Das Arzneimittel ist nach Anweisung des Arztes anzuwenden. Es ist nur zur äußerlichen Anwendung bestimmt. Vermeiden Sie den Kontakt mit den Augen.
- Das Medikament sollte nicht für andere Erkrankungen als die, für die es verschrieben wurde, verwendet werden.
- Das behandelte Hautareal sollte nicht bandagiert oder anderweitig abgedeckt oder eingewickelt werden, um es zu verschließen, es sei denn, der Arzt hat dies angeordnet.
- Patienten sollten ihrem Arzt alle Anzeichen von lokalen Nebenwirkungen melden.
Laboruntersuchungen
Die folgenden Tests können bei der Beurteilung von Patienten auf eine HPA-Achsen-Suppression hilfreich sein: ACTH-Stimulationstest; A.M. Plasma-Cortisol-Test; Test des freien Cortisols im Urin.
Karzinogenese, Mutagenese und Beeinträchtigung der Fruchtbarkeit
Langzeitstudien an Tieren wurden nicht durchgeführt, um das karzinogene Potential von Halobetasolpropionat zu bewerten. Positive Mutagenitätseffekte wurden in zwei Genotoxizitätstests beobachtet. Halobetasolpropionat war positiv in einem Mikronukleustest am chinesischen Hamster und in einem Maus-Lymphom-Genmutationstest in vitro.
Studien an der Ratte nach oraler Verabreichung in Dosen bis zu 50 µg/kg/Tag zeigten keine Beeinträchtigung der Fruchtbarkeit oder der allgemeinen Reproduktionsleistung.
In anderen Genotoxizitätstests erwies sich Halobetasolpropionat als nicht genotoxisch im Ames/Salmonella-Assay, im Schwesterchromatid-Austausch-Test in somatischen Zellen des chinesischen Hamsters, in Chromosomenaberrationsstudien an Keim- und somatischen Zellen von Nagetieren und in einem Säugetier-Spot-Test zur Bestimmung von Punktmutationen.
Schwangerschaft
Teratogene Wirkungen: Schwangerschaftskategorie C
Kortikosteroide haben sich bei Labortieren als teratogen erwiesen, wenn sie in relativ niedriger Dosierung systemisch verabreicht wurden. Einige Kortikosteroide haben sich nach dermaler Anwendung bei Labortieren als teratogen erwiesen.
Halobetasolpropionat hat sich bei SPF-Ratten und Kaninchen vom Chinchilla-Typ als teratogen erwiesen, wenn es während der Trächtigkeit systemisch in Dosen von 0,04 bis 0,1 mg/kg bei Ratten und 0,01 mg/kg bei Kaninchen verabreicht wurde. Diese Dosen entsprechen etwa dem 13-, 33- bzw. 3-fachen der topischen Dosis von Ultravate Creme beim Menschen. Halobetasolpropionat war bei Kaninchen embryotoxisch, aber nicht bei Ratten.
Gaumenspalte wurde sowohl bei Ratten als auch bei Kaninchen beobachtet. Omphalozele wurde bei Ratten, aber nicht bei Kaninchen beobachtet.
Es gibt keine adäquaten und gut kontrollierten Studien zum teratogenen Potential von Halobetasolpropionat bei schwangeren Frauen. Ultravate Creme sollte während der Schwangerschaft nur angewendet werden, wenn der potentielle Nutzen das potentielle Risiko für den Fötus rechtfertigt.
Stillende Mütter
Systemisch verabreichte Kortikosteroide gehen in die Muttermilch über und könnten das Wachstum unterdrücken, die endogene Kortikosteroidproduktion beeinträchtigen oder andere unerwünschte Wirkungen verursachen. Es ist nicht bekannt, ob die örtliche Verabreichung von Kortikosteroiden zu einer ausreichenden systemischen Absorption führen könnte, um nachweisbare Mengen in der Muttermilch zu erzeugen. Da viele Arzneimittel in die Muttermilch ausgeschieden werden, ist bei der Verabreichung von Ultravate Creme an eine stillende Frau Vorsicht geboten.
Anwendung bei Kindern
Die Sicherheit und Wirksamkeit von Ultravate Creme bei pädiatrischen Patienten wurde nicht nachgewiesen und die Anwendung bei pädiatrischen Patienten unter 12 Jahren wird nicht empfohlen. Aufgrund eines größeren Verhältnisses von Hautoberfläche zu Körpermasse besteht bei pädiatrischen Patienten ein höheres Risiko als bei Erwachsenen, dass die HPA-Achse unterdrückt wird und ein Cushing-Syndrom auftritt, wenn sie mit topischen Kortikosteroiden behandelt werden. Daher besteht bei ihnen auch ein größeres Risiko einer Nebenniereninsuffizienz während oder nach Absetzen der Behandlung. Bei unsachgemäßer Anwendung topischer Kortikosteroide bei Säuglingen und Kindern wurde über unerwünschte Wirkungen, einschließlich Striae, berichtet.
Bei Kindern, die topische Kortikosteroide erhalten, wurden eine Unterdrückung der HPA-Achse, das Cushing-Syndrom, eine lineare Wachstumsretardierung, eine verzögerte Gewichtszunahme und eine intrakranielle Hypertonie festgestellt. Zu den Manifestationen einer Nebennierensuppression bei Kindern gehören niedrige Plasmakortisolspiegel und ein Ausbleiben der Reaktion auf eine ACTH-Stimulation. Zu den Manifestationen der intrakraniellen Hypertension gehören vorgewölbte Fontanellen, Kopfschmerzen und beidseitiges Papillenödem.
Geriatrische Anwendung
Von etwa 400 Patienten, die in klinischen Studien mit Ultravate Creme behandelt wurden, waren 25 % 61 Jahre und älter und 6 % 71 Jahre und älter. Es wurden keine allgemeinen Unterschiede in der Sicherheit oder Wirksamkeit zwischen diesen Patienten und jüngeren Patienten beobachtet; und auch bei anderen berichteten klinischen Erfahrungen wurden keine Unterschiede im Ansprechen zwischen älteren und jüngeren Patienten festgestellt, aber eine höhere Empfindlichkeit einiger älterer Personen kann nicht ausgeschlossen werden.
Nebenwirkungen
In kontrollierten klinischen Studien gehörten Stechen, Brennen oder Juckreiz bei 4,4 % der Patienten zu den am häufigsten berichteten unerwünschten Wirkungen von Ultravate Creme. Weniger häufig wurden trockene Haut, Erythem, Hautatrophie, Leukoderma, Bläschen und Ausschlag berichtet.
Die folgenden zusätzlichen lokalen Nebenwirkungen werden bei topischen Kortikosteroiden selten berichtet und können bei hochwirksamen Kortikosteroiden wie Ultravate Creme häufiger auftreten. Diese Reaktionen sind in abnehmender Reihenfolge ihres Auftretens aufgeführt: Follikulitis, Hypertrichose, akneiforme Eruptionen, Hypopigmentierung, periorale Dermatitis, allergische Kontaktdermatitis, Sekundärinfektion, Striae und Miliaria.
Überdosierung
Topisch angewendete Ultravate Creme kann in ausreichenden Mengen absorbiert werden, um systemische Wirkungen zu erzeugen (siehe VORSICHTSMASSNAHMEN).
Ultravate Creme Dosierung und Anwendung
Tragen Sie eine dünne Schicht Ultravate Creme ein- oder zweimal täglich auf die betroffene Haut auf, wie von Ihrem Arzt verordnet, und reiben Sie sie sanft und vollständig ein.
Ultravate (Halobetasolpropionat Creme) Creme ist ein hochwirksames topisches Kortikosteroid; daher sollte die Behandlung auf zwei Wochen begrenzt werden, und es sollten keine größeren Mengen als 50 g/Woche verwendet werden. Wie bei anderen Kortikosteroiden sollte die Therapie abgesetzt werden, wenn eine Kontrolle erreicht ist. Wenn innerhalb von 2 Wochen keine Besserung eintritt, kann eine Neubewertung der Diagnose erforderlich sein.
Ultravate Creme sollte nicht mit Okklusivverbänden angewendet werden.
Wie wird Ultravate Creme geliefert
Ultravate® (Halobetasolpropionat Creme) Creme, 0.05% wird in den folgenden Tubengrößen geliefert:
15 g (NDC 10631-103-15)
50 g (NDC 10631-103-50)
Lagerung
Lagerung zwischen 15°C und 30°C (59°F und 86°F).
RANBAXY
Jacksonville, FL 32257 USA
09-0085 (flach), 09-0086 (gefaltet)
Revised May 2010
PACKUNGSEtikett.HAUPTANZEIGEPLATTE

15-Gramm-Behälter-Etikett

15-Gramm-Karton-Etikett

50-Gramm-Behälter-Etikett

50-Gramm-Karton-Etikett
| ULTRAVATE Halobetasolpropionat Creme |
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
Etikettierer – Ranbaxy Laboratories Inc. (169932519)
Registrant – Ranbaxy Laboratories Inc. (169932519)
| Einrichtung | |||
| Name | Adresse | ID/FEI | Betrieb |
| Contract Pharmaceuticals Limited | 248761249 | Herstellung | |
Häufig gestellte Fragen
- Halobetasol vs. Clobetasol – wie sind sie zu vergleichen?
- Kann es bei Giftefeu verwendet werden?
- Kann es auf der Kopfhaut verwendet werden?
Mehr über Ultravate (Halobetasol topisch)
- Nebenwirkungen
- Während der Schwangerschaft oder Stillzeit
- Dosierung Informationen
- Wechselwirkungen
- Preisangaben&Gutscheine
- En Español
- 6 Bewertungen
- Verfügbarkeit der Generika
- Medikamentenklasse: Topische Steroide
Ressourcen für Verbraucher
- Patienteninformationen
- Ultravate (Advanced Reading)
Ressourcen für Fachleute
- Rezeptinformationen
Andere Marken Lexette, Bryhali, Halonat
Verwandte Behandlungsleitfäden
- Psoriasis
- Atopische Dermatitis
- Dermatitis
- Ekzeme
Medizinischer Haftungsausschluss