Bevezetés
A pajzsmirigyfunkciós változások előfordulási gyakorisága a nőknél igen magas (5/1000 pajzsmirigy-alulműködés és 3/1000 pajzsmirigy túlműködés esetén1), és mivel ezen állapotok közül sok a szülőképes korban jelentkezik, nincs abban semmi különös, hogy a terhesség összefüggésben áll ezekkel a betegségekkel. Ráadásul a terhes nők pajzsmirigyhormon (TH) szintjének mérésére vonatkozó klinikai gyakorlat kiterjesztésével egyre több olyan pajzsmirigyműködési rendellenességet fedeznek fel terhes nőknél, amelyeket más körülmények között figyelmen kívül hagytak volna.
Másrészt az anyai pajzsmirigyműködés jelentős változásokon megy keresztül a terhesség alatt, ami a különböző laboratóriumi paraméterek változását eredményezi. Emiatt a különböző pajzsmirigyfunkciós paraméterek értelmezésekor más megközelítést kell alkalmazni a terhes nőknél, mint a nem terheseknél, hogy elkerüljük az esetlegesen súlyos következményekkel járó téves diagnózisokat és értékeléseket.
A fentiek következtében az utóbbi években megnőtt az érdeklődés a pajzsmirigy fiziológiája és a terhesség alatti lehetséges változások iránt.2 Ezek közül áttekintettük a terhességi pajzsmirigy túlműködéssel kapcsolatos szempontokat, annak kihívásait és lehetséges következményeit, mind a terhesség alatt (az anyában és/vagy a magzatban), mind a szülés után (az anyában és/vagy az újszülöttben).
Pajzsmirigyfunkció értékelése a terhesség alatt
A terhesség alatt jelentős élettani változások következnek be, amelyek jelentős hatást gyakorolnak az anyai pajzsmirigyfunkció különböző paramétereire3,4, többek között a következők:
- –
TSH. A TSH-szintek csökkenése hagyományosan minden terhességi időszakban megfigyelhető a nem terhes nőknél talált szintekhez képest,5 minimális szintekkel az első trimeszterben, amelyek aztán a második és harmadik trimeszterben emelkednek. A TSH-szintek e változásai tükrözik a humán koriongonadotropin (HCG) szintek változásait, amelyek az első trimeszterben tetőznek, majd ezt követően fokozatosan csökkennek. Ezért a különböző tudományos társaságok normális referenciaértékeket6-8 állapítottak meg (1. táblázat).
1. táblázat.Referencia TSH-értékek a különböző társaságok szerint.
Társadalom TSH-szintek (μU/ml) terhességben első trimeszter második trimeszter. trimeszter Harmadik trimeszter Endo 2007/SEEN 2009 ATA 2011 0.1-2,5 0,2-3 0,3-3 ATA: American Thyroid Association; Endo: Endokrinológiai Társaság; SEEN: Spanyol Endokrinológiai és Táplálkozástudományi Társaság.
Források: Stagnaro-Green és mtsi.6 Abalovich és mtsi.7 és Galofré és mtsi.8
Megjegyzendő, hogy a TSH-szintek csökkenése még nagyobb a többes terhességben, és hogy a dohányzó terhes nők TSH-szintje alacsonyabb az első és harmadik trimeszterben.9
- –
TBGT-T4. A terhességgel járó megnövekedett ösztrogénszintek növelik a TBG-szinteket és következésképpen a TT4-értékeket. A TT4-szintek változása azonban nagyon következetes (150%-kal nő), és mind a trimesztertől, mind az alkalmazott módszertől függetlenül történik. Így, ha a TT4-szintek rendelkezésre állnak, a terhes nők T4-termelését úgy lehet megbecsülni, hogy a nem terhes nőkre vonatkozó referenciahatárokat 1,5-el megszorozzuk.
- –
FT4. A klinikai gyakorlatban a legtöbb szabad T4 (FT4) mérést nem az arany standardnak számító egyensúlyi dialízis vagy ultraszűrési módszerrel végzik. A rutinszerűen alkalmazott eljárás egy immunoassay-rendszer, ahol az FT4 nem közvetlenül kvantitatív érték, hanem egy fehérjeérzékeny (a TBG és az albumin által befolyásolt) módszerrel becsülik, és amelyet ezért a terhesség erősen módosít, és a trimesztertől függően is változik. Ezenkívül minden vizsgálati módszernek vannak sajátos variációi. Ez azt jelenti, hogy a terhesség alatti FT4 megfelelő értelmezéséhez a terhességi kortól és az alkalmazott módszertől függő referenciaértékeknek kell rendelkezésre állniuk, amint azt az American Thyroid Association (ATA) is megállapítja.6
A hyperthyreosis hatása az anyára és a magzatra
Amint azt a 2. táblázat mutatja, a terhesség alatti hyperthyreosis súlyos következményekkel járhat mind az anya és a magzat, mind pedig a születés után az újszülött számára.10-12 Meg kell jegyezni azt is, hogy endogén hyperthyreosisban nemrégiben a trombózis fokozott kockázatáról számoltak be, amely a hyperthyreosis kontrollálásával nyilvánvalóan reverzibilis.13 A terhesség alatti mélyvénás trombózis és a pulmonális tromboembólia fokozott kockázata miatt14 magas szintű gyanakvást kell fenntartani, hogy e szövődményt időben fel lehessen fedezni, és esetleg profilaktikus intézkedéseket kell mérlegelni.
Táblázat 2.A hyperthyreosis anya-magzati hatása.
Anyai
Vetélés
Preeclampsia (többszörös kockázat×5)7
Koraszülés (többszörös kockázat×10)12
. Abruptio placentae
Szívelégtelenség (szorozza a kockázatot×20)12
Pajzsmirigy vihar (szorozza a kockázatot×10)12
Vénás trombózis13
Magzati
Low születési súly
Intrauterin növekedési retardáció
Koraszülöttség
Kicsi a terhességi korhoz képest
Magzati halál
Pajzsmirigy diszfunkció (hyperthyreosis) vagy hypothyreosis)
Magzati golyva
Újszülöttkori
Átmeneti hyperthyreosis
Átmeneti vagy tartós hypothyreosis
Források:A terhesség alatti hyperthyreosis osztályozása
A 3. táblázat a terhesség alatti hyperthyreosis különböző diagnosztikai lehetőségeit ismerteti. Egyrészt számos, közvetlenül magából a terhességből eredő állapot létezik, amelyek a tranziens gesztációs thyreotoxicosis (TGT) címszó alá sorolhatók. Másrészt minden olyan állapot, amely a terhességen kívül pajzsmirigy-túlműködéshez vezet, a terhesség alatt is előfordulhat. Végül a TH-szint emelkedése exogén TH-ellátás miatt is előfordulhat.
3. táblázatA terhességi hyperthyreosis etiológiai osztályozása.
Tranziens terhességi thyreotoxicosis
Hyperemesis gravidarum
Többszörös terhesség
Trophoblastos hyperthyreosis (mol, choriocarcinoma)
Hyperreactio luteinalis
Familiáris terhességi thyreotoxicosis
Hyperplacentosis
Pajzsmirigybetegség
Graves-kór
Graves-kór
Pajzsmirigygyulladás
Multinoduláris golyva
Toxikus pajzsmirigy adenoma
Iatrogén
Túlkezelés
Pajzsmirigyhormonok véletlen bevitele (élelmiszer-szennyezés, stb.)
Ténybeli
Tranziens terhességi thyreotoxicosis
Ez a terhesség alatti hyperthyreosis leggyakoribb oka, és a terhességek 1-3%-ában fordulhat elő.15,16 Úgy definiálták, mint átmeneti hyperthyreosis, amely a terhesség első felére korlátozódik, és amelyet emelkedett FT4- vagy TT4-szint (igazított), szupprimált vagy nem kimutatható TSH-szint jellemez, pajzsmirigy autoantitestek16 vagy Graves-kórra (GD) utaló fizikai jellemzők hiányában.17 Ez általában a megnövekedett HCG-szint vagy a TSH-receptorok iránti nagyobb affinitás következménye.
A legjellemzőbb állapot ebben a csoportban (3. táblázat) a hyperemesis gravidarum (HG), de vannak más állapotok is, amelyek szintén fokozott HCG-szintekkel járnak, mint például a többszörös terhesség vagy a trophoblastos betegség (hydatid mole vagy choriocarcinoma), amelyek TGT-prevalenciája akár 50% is lehet.17 Vannak más, kevésbé gyakori okok is, mint a hyperreactio luteinalis,18 amelyet a terhesség során kialakuló theca-lutein-ciszták jellemeznek, vagy a hyperplacentosis,19 ahol a placenta súlyának és HCG-termelésének növekedése figyelhető meg. Létezik egy familiáris állapot is (familiáris gesztációs tirotoxicosis20), ahol a TSH-receptor fiziológiás HCG-szintekkel szembeni túlérzékenysége domináns autoszomális mutáció miatt alakul ki; klinikailag jellemző, hogy a TGT minden terhességben és a család minden nőjénél normális HCG-szintek mellett alakul ki.
Hyperemesis gravidarum
A TGT leggyakoribb oka a HG. A HG az összes terhesség 0,5-10/1000 terhességében fordul elő,21 és az esetek 30-60%-ában emelkedett szabad TH-szintekkel és TSH-szuppresszióval jár együtt.22 Meg kell jegyezni, hogy a HG fogalmát a terhesség első trimeszterében hányással, dehidratációval, a testsúly legalább 5%-ának elvesztésével és ketonuriával járó állapotokra kell korlátozni.23
Ezekben az esetekben a hyperthyreosisra a TSH-szintek szuppressziója és minimális FT4-emelkedés jellemző, általában normális FT3-szintek mellett. A pajzsmirigy túlműködés, valamint a társuló hányás általában spontán megszűnik a 20. hét előtt, és a tüneti kezelés intravénás hidratálással és B-vitamin-komplexszel elegendő a Wernicke-encephalopathia kivételes kockázatának megelőzésére24. Nincs bizonyíték arra, hogy a pajzsmirigy-ellenes gyógyszerekkel (ATD) történő kezelés bármilyen előnnyel járna,25 ezért alkalmazásuk nem tanácsos.6
Kivételesen az erősen feltűnő pajzsmirigy-túlműködési komponenssel rendelkező HG vagy a gasztrointesztinális intoleranciával (hányinger és hányás) társuló GD utalhat a kettő közötti differenciáldiagnózis szükségességére. A 4. táblázat a főbb különbségeket mutatja be. Mindenesetre, ha a hyperthyreosis a terhesség első trimeszterén túl is fennáll, a TGT-től eltérő okra kell gyanakodni.
4. táblázatA Graves-kór és a hyperemesis közötti különbségek.
Jele Graves-kór Hyperémia A pajzsmirigy túlműködés tünetei a terhesség előtt ++ – A pajzsmirigy túlműködés tünetei a terhesség alatt. +/++ -/+ Émelygés/hányás -/+ +++ Golyva/ophthalmopathia. + – Pajzsmirigy antitestek ++ – T-US Hypervaszkuláris Normális Családban előfordult HG – + Hasonló tünetek korábbi terhességben – + .
T4 T3 .
TT3/TT4 arány >20 T-US: HG: hyperemesis gravidarum.
Graves-kór
A pajzsmirigybetegségek közül a GD a terhességi hyperthyreosis leggyakoribb oka, az összes terhesség 0,1-1%-ában fordul elő (klinikai és szubklinikai hyperthyreosis 0,4%-ban, illetve 0,6%-ban).10
A GD természetes lefolyása a terhesség alatt a tünetek súlyosbodása az első trimeszterben a TSH-receptor HCG általi stimulációjának additív hatása miatt, majd a terhesség második felében a terhesség immunmoduláló hatása miatt javulás, és a szülés után kiújulás.
Graves-kór a terhességben
A terhesség alatti aktív GD tünetei nem különböznek az állapotra jellemző tünetektől. Egyes tünetek néha összetéveszthetők magával a terhesség tüneteivel. A szemtünetek és a golyva esetleges jelenléte segít az állapot tisztázásában, a hormonmérések pedig lehetővé teszik a diagnózist.
A Graves-kór kezelése terhességben
Mint ismeretes, nem terhes nőknél három lehetséges terápiás megközelítés létezik a GD kezelésére: 131I, műtét vagy gyógyszeres kezelés ATD-kkel. E három lehetőség közül a 131I beadása terhességben ellenjavallt a fejlődési rendellenesség kockázata miatt,7 ezért a lehetőségek a thyreoidektómiára vagy az ATD-k alkalmazására korlátozódnak. Ami a műtétet illeti, azt csak kivételes körülmények között szabad elvégezni, amint azt alább tárgyaljuk.
Orvosi kezelés. Pajzsmirigyellenes gyógyszerek
A terhesség alatti GD gyógyszeres kezelésére néhány évvel ezelőttig hagyományosan a propiltiuracilt (PTU) tartották a metimazollal/karbimazollal (MM/CM) szemben a legmegfelelőbb kezelésnek.26 Ez az elképzelés néhány olyan vizsgálaton alapult, amelyek szerint a PTU placentáris átvitele minimális az MM/CM-hez képest27 , valamint az MM/CM teratogén hatásain. Jelenleg ismert, hogy mindkét ATD átjut a placentán, és ezért ugyanolyan eséllyel hatnak a magzatra és okoznak magzati hipotireózist26 .
Az MM/CM szerepe továbbá a magzati aplasia cutis és a choanal- és oesophagealis atresia, valamint néhány más, globálisan “metimazol embriopátiának” nevezett rendellenesség28 magzati megjelenésében igen ellentmondásos,29-31 és ezeket a rendellenességeket egyes esetekben magának a hyperthyreosis káros hatásainak tulajdonították. A legújabb tanulmányok32,33 azonban azt mutatják, hogy az MM/CM teratogén hatású, ellentétben a PTU-val.
Másrészt az utóbbi években megjelentek jelentések PTU-val kezelt betegek fulmináns toxikus hepatitisének eseteiről,34,35 0,1% és 0,5% közötti előfordulási arányokkal és magas halálozási aránnyal (25-50%).10,36 Még neonatális hepatitis eseteiről is beszámoltak olyan újszülötteknél, akik PTU-val kezelt anyától születtek.37,38
Ezért dilemmával állunk szemben: egyrészt egyértelműen felismertnek tűnik, hogy az MM/CM fejlődési rendellenesség kockázatával jár, másrészt, hogy a PTU végzetes szövődményeket okozhat.
Az alternatívával szembesülve egyes szerzők a terhesség előtti ablációs kezelést javasolták a GD-s nőknél.39 Ez a megoldás azonban aligha oldja meg a problémát, mert a GD-s nők a legtöbb esetben nem terveznek terhességet. Másrészt ez az intézkedés nem akadályozza meg az esetleges magzati hyperthyreosis (Fhyper) kialakulását a pajzsmirigy-stimuláló antitestek (TSI) magas szintjének fennmaradása miatt, ami orvosi kezelést igényel, így újra felveti a problémát.
Ezért az ATA kritériumokat határozott meg a PTU általános populációban és terhes nőknél történő alkalmazására vonatkozóan.40 Terhesség esetén az ATA a terhesség első trimeszterében (az organogenezis időszakában) nem javasolja az MM/CM alkalmazását, és a PTU alkalmazását ajánlja. A terhesség 12. hete után a PTU-t a májbetegség kockázata miatt abba kell hagyni, és a GD-ellenőrzést MM/CM-mel kell folytatni. Terhességen kívül a PTU alkalmazása csak két esetben javasolt: először is, ha pajzsmirigyvihar lép fel, másodszor pedig az MM/CM által kiváltott mellékhatások esetén.
A PTU-kezelés megkezdésének késedelmének elkerülése érdekében célszerű, hogy a potenciálisan teherbe esni képes, fogamzásgátló módszert nem alkalmazó GD-s nőknek otthon PTU álljon rendelkezésre, és utasítást kapjanak a gyógyszeres kezelés (MM/CM-ről PTU-ra történő) váltásra, amint igazolták a terhességet.
Az orvosi kezelés. Klinikai kezelés
A fentiek szerint a terhesség alatti GD kezelésének az első trimeszterben PTU-ból, ezt követően pedig MM/CM-ből kell állnia. A kezdő adag 50-300 mg/nap PTU három osztott adagban, 5-15 mg/nap metimazol, vagy 10-15 mg/nap karbimazol egyszeri adagban.6 Mindig meg kell próbálni a lehető legkisebb adagot alkalmazni.
Béta-blokkolókat csak átmenetileg szabad alkalmazni, mert hosszú távú alkalmazásukat méhen belüli növekedési elmaradással, bradycardiával és újszülöttkori hipoglikémiával hozták összefüggésbe.41 Ezenkívül egyes szerzők fokozott vetélésről számoltak be propranolol és ATD kombinált kezelés esetén.42
Az ATD adagjának beállításakor törekedni kell arra, hogy az anya pajzsmirigyműködését a szubklinikai túlműködés határértéke közelében tartsuk, mert a magzati pajzsmirigy sokkal érzékenyebb az ATD-k blokkoló hatására. Valójában a kimutatható TSH jelenléte azt jelzi, hogy az ATD dózisát csökkenteni kell.10,43
A terhesség alatti GD igen dinamikus lefolyást mutat, így a betegek akár 20-30%-a is elérheti a kontroll olyan fokát, amely lehetővé teszi az ATD abbahagyását a terhesség utolsó trimeszterében44. A kombinált séma (ATD-k és TH-k) alkalmazása a GD kezelésére abszolút ellenjavallt terhességben, mivel magzati hypothyreosis-t (Fhypo) okoz.6,43
Műtét
A várandós nőknél a GD ellenőrzésére alkalmazott műtétet illetően a különböző konszenzusok és klinikai irányelvek6,7,43 egyetértenek abban, hogy azt csak az alábbi esetekben javasolják:
- 1
Az ATD-kkel szembeni mellékhatások, amelyek megakadályozzák azok alkalmazását.
- 2
Nagy ATD-dózisok szükségessége.
- 3
A beteg nem tartja be az orvosi kezelést.
Az olasz irányelvek43 emellett a légúti kompresszióval járó kiterjedt anyai golyva esetén is javasolják a műtétet.
Ha elvégzik, a műtét legjobb időpontja a második trimesztertől kezdődően van. Ez indokolja a béta-blokkolók és nátrium-jodid (50-100 mg/nap)45 alkalmazását rövid ideig (10-14 napig) a GD-ben szenvedő terhes nőknél a műtétre való felkészülésként. A fentiekben tárgyaltak szerint a béta-blokkolókkal való hosszú távú kezelés kerülendő. Óvatosnak kell lenni a kálium-jodid adásakor is, hogy megelőzzük a golyva és/vagy a Fhypo kialakulását.
A műtét mélyreható változást okoz. Egyrészt a hyperthyreosis a terhes nőknél megszűnik, de az anyában hypothyreosis alakul ki, ami gyors pótlást és rendszeres TSH-monitorozást igényel. A TSI-szinteket is ellenőrizni kell, és szükség esetén monitorozni kell a magzati hyperthyreózist.
A pajzsmirigy autoimmunitás változásai a terhesség alatt
Egyes szerzők kimutatták, legalábbis néhány esetben, hogy a TSH-receptor elleni antitestek funkcionális aktivitása stimulálóról gátló vagy blokkoló aktivitásra változik.46,47 Ez azt jelenti, hogy a terhesség nemcsak az autoantitest-szinteket, hanem azok funkcionális profilját is modulálja. Ez az elképzelés azt jelenti, hogy a GD a terhesség alatt nemcsak normális funkcióvá, hanem akár hipofunkcióvá is alakulhat a stimuláló-blokkoló aktivitás e változása miatt, ahogyan arról néhány esetben már beszámoltak.48 Vagyis a GD a terhességben egy változékony folyamat, amely állandó rendszeres ellenőrzést igényel, és amelyet nem szabad elhanyagolni még akkor sem, ha az ATD-ket nem igénylő, látszólagos remissziós állapotot értek el.
Pajzsmirigy-stimuláló antitestek mérése terhességben
Az esetleges TSI autoantitestek magzati pajzsmirigyre gyakorolt hatásának megelőzése érdekében az ETA 1998-ban közzétette49 a terhesség alatti TSI-mérés indikációit meghatározó kritériumokat az anya GD jellemzőitől függően (5. táblázat).
5. táblázatA TSI mérésének indikációi az Európai Pajzsmirigy Társaság szerint.
(I) Terhesség előtt gyógyszeres kezeléssel gyógyult Euthyreoid GD-s nő
– Nincs mérés
(II)131I vagy műtét után gyógyult Euthyreoid GD-s nő
– TSI korai mérése: Ha pozitív, monitorozza a magzati hyperthyreosis
– TSI mérése a harmadik trimeszterben (ha pozitív az első trimeszterben): ha pozitív, monitorozza az újszülöttkori hyperthyreózist
(III) Terhesség alatt GD miatt kezelt nő
– TSI mérése a harmadik trimeszterben, ha pozitív, monitorozza az újszülöttkori hyperthyreózist
GD: Basedow-kór.
Forrás:
Forrás:
Sz: Laurberg és mtsi.49
Amennyiben a GD a terhesség előtt gyógyszeres kezeléssel gyógyult, az immunállapot megoldottnak tekinthető, és a TSI mérése nem szükséges.
Ha a GD-t ablációs kezeléssel (műtét vagy sugárkezelés) oldják meg, az immunállapot fennmaradhat. A TSI-szintek általában 12-18 hónappal a műtét után negatívvá válnak. A 131I ablációs terápia után a szintek az első néhány hónapban kezdetben emelkednek, majd csökkennek, bár akár öt évig is magasak maradhatnak.50 Ez azt jelenti, hogy a 131I utáni esetleges Fhyper megelőzése érdekében hosszú távú fogamzásgátlást kell fenntartani. Így azoknál a nőknél, akik teherbe akarnak esni, és magas TSI-titerrel rendelkeznek, a műtétet előnyben kell részesíteni a 131I-vel szemben. Mindezekben az esetekben a TSI-szinteket korán meg kell határozni a HF potenciális kockázatának felmérése érdekében, és a harmadik trimeszterben újra meg kell mérni, hogy lássák, továbbra is pozitívak-e, és fennáll-e ezért az újszülöttkori hyperthyreosis kockázata.
A terhesség alatti aktív GD esetén a Fhyper potenciális kockázatát az anya ATD-kkel történő kezelésével lehet kontrollálni. Célszerűnek tartják azonban a TSI vizsgálatát a terhesség végén, hogy felmérjék az újszülöttkori hyperthyreosis kockázatát.
Az ATA6 körülbelül a 20-24. héten javasolja a vizsgálatot, és sokkal általánosabb ajánlásokat fogalmaz meg:
- –
Az anya aktív hyperthyreosisban szenved.
- –
A 131I-vel történő kezelés története.
- –
Kori thyreoidektómia.
- –
Kori újszülött hyperthyreosisban.
Graves-kór a magzatban
Nem szabad elfelejteni, hogy a magzati pajzsmirigy a 20. héttől érik el az érettséget, és ezért ugyanolyan hatásokra (ATD-k és TSI) képes reagálni, mint a felnőtt pajzsmirigy. Emiatt mind Fhypo, mind Fhyper előfordulhat terhességi GD esetén.
Magzati hypothyreosis
Fhypo általában relatív ATD-túladagolás miatt fordul elő, ami az anyában fenntarthatja a normális működést, de a magzatban egyértelmű hypofunkciót okoz.
Szuggesztív klinikai tünetek
Az állapot klinikailag gyanítható a szülészeti ultrahangvizsgálat során észlelt magzati golyva és az ATD-vel kezelt terhes nőnél kialakuló polyhydramnios alapján.
A magzati golyva jelenléte, függetlenül a funkcionális szempontoktól, tömeghatása miatt riasztó jel51 (1. ábra). Figyelembe kell venni, hogy a pajzsmirigy megnagyobbodása a magzat hátsó nyakának hiperextenzióját okozza, ami viszont rontja a magzat méhen belüli mozgékonyságát, és ennek következtében rendellenes szüléskori megjelenéshez vezet (válldystocia, farfekvés stb.). Még ha ez a hiperextenzió nem is akadályozza meg a magzat megfelelő feji helyzetét, megakadályozza a magzat nyakának megfelelő hajlítását a szüléshez, ami arccal történő fekvést okoz. Mindezek a helyzetek császármetszést igényelnek. Azonban nem ez a fő szövődmény, mivel a góc által a magzat éretlen légcsőporcaira gyakorolt kompresszió légcső- és nyelőcső-összenyomódást okozhat. Ez légúti elzáródást eredményez, ami a fulladás veszélyével jár. Ezenkívül a nyelőcső összenyomódása akadályozza a magzatvíz lenyelését, ami folyadékfelhalmozódáshoz és polihidramnion kialakulásához vezet. Ez kedvez a koraszülésnek, az újszülöttkori morbiditás és mortalitás fő okának.
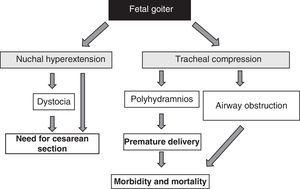 1. ábra.
1. ábra.A magzati góc kialakulásának következményei.
(0.1MB).Diagnózis
A fhypo gyanújának megerősítésére szolgáló egyetlen teljesen megbízható eljárás a magzati TH-szint mérése chordocentézissel. Ez az eljárás nem mentes a szövődményektől (a magzati halálozás 2%-os kockázatával jár52), és bonyolultabb, mint az egyszerű amniocentézis. A magzati TH-szintek magzatvízben történő mérése azonban nem megbízható, és nem korrelál a magzati vérben történő mérésükkel.53 Nem szabad elfelejteni, hogy a magzatvízben anyai eredetű TH-k is megtalálhatók.54 A különböző irányelvek szerint6,43 a chordocentézist csak akkor szabad elvégezni, ha golyva észlelhető olyan magzatnál, akinek az anyja ATD-ket szed, és a Fhyper vagy Fhypo biztos diagnózisa nem állítható fel, és mindig tapasztalt központban.
Ez a megközelítés helyett a magzati TH-k metabolizmusából származó W vegyület mérését javasolták a közelmúltban. A magzatban, ellentétben a felnőttekkel, a TH-k metabolizmusa a szulfokonjugációs útvonalat követi, dijódtironin-szulfátot képezve; ez a vegyület viszont metilálódik a placentában és a méhfalban, mielőtt az anyai keringésbe kerül és W vegyületet képez. Ez a vegyület minden terhes nőben megtalálható a magzati pajzsmirigyműködés kialakulásától kezdve, és a terhesség során fokozatosan növekszik, majd a szülés után eltűnik. Ezért javasolták a magzati pajzsmirigyműködés markerének.55 Ebben a környezetben az ATD-kkel kezelt terhes nőnél a W vegyület szintjének nem megfelelő progressziója a fhypo kialakulására utalhat.56 Ez azonban egyelőre nem több, mint egy kvázi-kísérleti módszer.
Kezelés
Az első intézkedés az ATD-k abbahagyása. Az ATD-hatások látenciája miatt azonban, miután abbahagyták, TH-pótlásra is szükség van, amíg a magzati pajzsmirigy teljesen helyre nem áll. A TH-k placentáris átjutása korlátozott, ezért azokat intra-amnionotikus úton kell beadni. Ez az út, bár invazív, sokkal biztonságosabb, mint a chordocentézis, és a terhesség első felét követően minimális a vetélés kockázata.57
A magzat T4-gyel történő intraamnionális kezelését illetően nincs bevett kezelési séma, és az irodalmi adatok meglehetősen ellentmondásosak.53,58,59 Az eddig közölt esetek közelmúltbeli áttekintése51 megállapította, hogy az átlagos adag körülbelül 279μg levotiroxin heti egyszer (egytől hat hétig). Úgy tűnik, hogy ez 0,5-2,5 héttel az első adag után visszafordítja a magzati strúmát. Néhány esetben ismételt TH-méréseket végeztek, míg más esetekben a golyva eltűnését csak ultrahanggal követték nyomon.
Magzati hyperthyreosis
A golyva ritka szövődmény, és a jelenlegi vagy korábbi GD-ben szenvedő anyától született csecsemők akár 1-2%-ánál is előfordulhat, bár valószínűleg aluldiagnosztizált állapotról van szó.60,61
A Fhyper kialakulása – a TSH-receptor mutációk nagyon ritka eseteitől eltekintve62 – lehet a várandós nő rosszul kontrollált GD-jének következménye, vagy, ami még gyakoribb, kialakulhat olyan terhes nőnél, akinek a terhessége előtt ablációs terápiával gyógyult a GD, és továbbra is magas a TSI-szintje. A TSI mérésének indikációit a Fhyper kockázatának megállapítása céljából már tárgyaltuk. A normálisnál 3- vagy 5-szer magasabb TSI-szintek6,63 a Fhyper kockázatával járnak.
Szuggesztív klinikai tünetek
A magzati golyva megjelenése az egyik legkorábbi jellemző. Magzati bradycardia, előrehaladott csontkor, általános növekedési elmaradás és craniosynostosis is előfordulhat.64 Súlyosabb formákban magzati hydrops-szal járó szívelégtelenség vagy a központi idegrendszer károsodott érése mentális retardációval járhat. Végül koraszülés is előfordulhat.65
Diagnózis
A fent említett jelek nem véglegesek; a tachycardia nem mindig fordul elő, és az ultrahangos golyva jelenléte gyakori lelet Fhypo esetén. Ha kétség merül fel azzal kapcsolatban, hogy az állapot az ATD-k hatása miatt Fhypo vagy a rossz anyai kontroll miatt Fhyper, egyes szerzők ultrahangadatokon alapuló pontozási rendszert javasoltak66 (6. táblázat). Ha a kétség továbbra is fennáll, a magzati TH-t chordocentézissel kell mérni, a Fhypo szakaszban leírtak szerint. A W vegyület (korábban tárgyalt) esetleg hasznos lehet erre a célra a jövőben.
6. táblázat.Ultrahangos pontozás a hyperthyreosis és hypothyreosis megkülönböztetésére magzati golyva esetén.
Ultrahangos jellemző Pontok Magzati szívfrekvencia Tachycardia 1 Normális 0 Gömbölyded érrendszer Központi 1 Perifériás vagy hiányzik 0 Magzati mozgások Normál 1 Fokozott 0 Csonttartás. érés Gyorsított -1 Normál 0 Késleltetett 1 Score értelmezése ≥2 sugallja. pajzsmirigy túlműködést Adapted from Huel et al.66Kezelés
A kezelésnek az ATD-ken kell alapulnia. Ebben az esetben, a Fhypo-tól eltérően, a kezelést nem intra-amnionotikus úton kell beadni, mivel az ATD-k szabadon áthaladnak a placentán. Rosszul kontrollált GD-vel rendelkező terhes nőnél fellépő Fhyper esetén csak az anya kezelésének módosítására van szükség. Ezzel szemben, ha az anya funkciója a korábbi ablációs terápiának köszönhetően normális, és csak a magzat mutat túlműködést, az MM/CM-et 10-20 mg/nap dózisokkal kezdődően kell az anyának adni. A kezelést 4-5 naponta ellenőrizni kell a magzati HR és a golyva lefolyása alapján, hogy a magzatot ne adagoljuk túl és ne okozzunk Fhypo-t.10
Ha az ATD-k adásakor az anyánál hypothyreosis lép fel, levothyroxint kell adni neki, amely alig jut át a placentán, és ezért kompenzálja a hypothyreosist anélkül, hogy a magzatra hatással lenne. Ez az egyetlen olyan körülmény, amikor a kombinált séma alkalmazható.
Graves-betegség az újszülöttben
Újszülötteknél a terhesség alatti GD mind hyperthyreózist, mind hypothyreózist okozhat.
Újszülöttkori hyperthyreózis
Ez az aktív GD10 és magas TSI-titerrel rendelkező terhes nők által az utolsó trimeszterben született csecsemők 1-5%-ánál fordulhat elő. A magzat a terhesség alatt az anya által kapott ATD-k hatására fenntartja normális működését. Az ATD-k felezési ideje 24-72 óra, és ezen időszak után megszűnik a magzati pajzsmirigyre gyakorolt hatásuk. Ez az anyai TSI-nek lesz kitéve, amely a szülés után akár 12 hétig is fennmaradhat.
Az eredetileg tünetmentes újszülöttben a szülés után néhány nappal fellépő pajzsmirigy túlműködés, sőt szívelégtelenség is megjelenhet.
Ez az állapot olyan anyák újszülöttjeinél is előfordulhat, akik a terhesség előtt ablációs terápiában részesültek, és továbbra is emelkedett TSI-szinteket mutatnak, akiknél nem diagnosztizált Fhyper lépett fel. Ezekben az esetekben az újszülöttkori hyperthyreosis a Fhyper folytatása; az újszülöttek születéskor súlyos érintettséget, alacsony súlyt és felgyorsult csontérést mutatnak.
A kezelésnek MM/CM 0,5-1mg/testsúlykg/nap dózisban és propranolol 2mg/testsúlykg/nap36 adásából kell állnia, a klinikai lefolyástól függően és szem előtt tartva, hogy ez egy átmeneti állapot. Meg kell jegyezni, hogy a TSI-k idővel megváltoztathatják funkcionális profiljukat, és receptorblokkolókká válhatnak, és hipotireózis alakulhat ki.
Szekunder neonatális hipotireózis
A rosszul kontrollált GD-ben szenvedő anyától született csecsemőknél előfordulhat, hogy a TH-k emelkedett szintjei, amelyeknek a terhesség alatt ki voltak téve, a TSH-szekréció szuppresszióját okozták, ami születéskor másodlagos hipotireózishoz vezetett.67 Ez a helyzet lehet átmeneti vagy végleges a TSH-szekréció tartós hipofízis-károsodásának eredményeként.
Az újszülötteknek levothyroxint kell adni, majd rendszeres értékelést kell végezni a TSH-szekréció esetleges helyreállásáig.
Az RSH-receptort blokkoló anyai autoantitestek perzisztenciája miatt kialakuló átmeneti újszülöttkori hypothyreosis is előfordulhat.68
Graves-betegség szülés utáni nőknél
A terhesség előtt vagy után korábban kontrollált GD a szülés után kiújulhat. A szülés utáni kiújulási arány akár 84% is lehet, szemben a terhesség nélküli nők 56%-ával.69 Ezért ajánlott az anyai TH-k mérése hat héttel a szülés után és akár egy évig is.10
Ha a GD kiújul, orvosi kezelésre lesz szükség MM/CM-mel. Bár az ATD-k kiválasztódnak az anyatejbe, adásuk nem jár kockázattal a szoptatás alatt, és akár 20-30 mg MM/CM is bevehető anélkül, hogy az újszülöttek pajzsmirigyére hatással lenne.70 Az ATD-ket osztott adagokban és mindig a tejbevitel befejezése után kell bevenni.
Felmerült, hogy az anyatejben lévő TSI a csecsemő éretlen gasztrointesztinális epithelén keresztül az újszülöttek általános keringésébe kerülhet, és újszülöttkori hyperthyreózist okozhat vagy meghosszabbíthatja. Erre azonban még nincs meggyőző bizonyíték.71
Addendum
A kézirat benyújtása után az Észak-Amerikai Endokrinológiai Társaság új klinikai gyakorlati útmutatót adott ki a pajzsmirigyzavarok kezeléséről a terhesség és a szülés utáni időszakban (J Clin Endocrinol Metab 2012; 97: 2543-2565). A terhességi pajzsmirigy túlműködésről szóló fejezetben megadott ajánlások nem térnek el lényegesen a jelen áttekintésben tárgyaltaktól.
Érdekütközések
A szerző kijelenti, hogy nincsenek összeférhetetlenségei.
Megállapítja, hogy nem áll összeférhetetlenségben.
- –