Introducere
Prevalența modificărilor funcției tiroidiene la femei este foarte mare (5/1000 pentru hipotiroidism și 3/1000 pentru hipertiroidism1) și, deoarece multe dintre aceste afecțiuni apar la vârsta fertilă, nu este nimic ciudat în ideea ca sarcina să fie asociată cu aceste boli. În plus, pe măsură ce practica clinică de măsurare a nivelurilor de hormoni tiroidieni (TH) la gravide se extinde, un număr tot mai mare de anomalii ale funcției tiroidiene, care ar fi fost trecute cu vederea în alte circumstanțe, sunt acum detectate la gravide.
Pe de altă parte, funcția tiroidiană maternă suferă modificări semnificative în timpul sarcinii, ceea ce duce la modificări ale diferiților parametri de laborator. Din această cauză, ar trebui utilizată o abordare diferită la femeile gravide față de cele care nu sunt gravide atunci când se interpretează diferiții parametri ai funcției tiroidiene, pentru a evita diagnosticele și evaluările greșite cu consecințe potențial severe.
Ca urmare a celor de mai sus, în ultimii ani a apărut un interes pentru fiziologia și modificările potențiale ale glandei tiroide în timpul sarcinii.2 Dintre acestea, am trecut în revistă aspecte legate de hipertiroidismul în sarcină, provocările și consecințele potențiale ale acestuia, atât în timpul sarcinii (la mamă și/sau făt), cât și după naștere (la mamă și/sau nou-născut).
Evaluarea funcțională a tiroidei în timpul sarcinii
În timpul sarcinii apar modificări fiziologice semnificative care au un impact considerabil asupra diferiților parametri ai funcției tiroidei materne3,4, printre care se numără următoarele:
- –
TSH. În mod tradițional, în orice perioadă a sarcinii au fost observate niveluri scăzute de TSH în comparație cu nivelurile găsite la femeile care nu sunt însărcinate5, cu niveluri minime în primul trimestru, care cresc ulterior în al doilea și al treilea trimestru. Aceste modificări ale nivelurilor de TSH reflectă modificările nivelurilor de gonadotropină corionică umană (HCG), care ating un maxim în primul trimestru și scad treptat după aceea. Acesta este motivul pentru care diferitele societăți științifice au stabilit valori normale de referință6-8 (tabelul 1).
Tabel 1.Valorile de referință ale TSH în funcție de diferite societăți.
Societatea Nivelurile TSH (μU/ml) în sarcină Primul trimestru Secundul trimestru trimestru Trimestrul al treilea Endo 2007/SEEN 2009 ATA 2011 0.1-2,5 0,2-3 0,3-3 ATA: American Thyroid Association; Endo: Endocrine Society; SEEN: Societatea Spaniolă de Endocrinologie și Nutriție.
Surse: Stagnaro-Green et al.6 , Abalovich et al.7 și Galofré et al.8
Trebuie remarcat faptul că scăderile nivelurilor de TSH sunt și mai mari în cazul sarcinilor multiple și că femeile însărcinate care fumează au niveluri mai scăzute de TSH în primul și al treilea trimestru.9
- –
TBGT-T4. Nivelurile crescute de estrogen asociate cu sarcina cresc nivelurile de TBG și, în consecință, valorile TT4. Cu toate acestea, modificările nivelurilor de TT4 sunt foarte consistente (cresc cu 150%) și fac acest lucru independent atât de trimestru, cât și de metoda utilizată. Astfel, dacă nivelurile de TT4 sunt disponibile, producția de T4 de către femeile gravide poate fi estimată prin înmulțirea cu 1,5 a limitelor de referință la femeile care nu sunt gravide.
- –
FT4. În practica clinică, majoritatea măsurătorilor de T4 liber (FT4) nu sunt efectuate utilizând metodele de dializă de echilibru sau de ultrafiltrare, care reprezintă standardul de aur. Procedura utilizată în mod curent este un sistem de imunodozare în care FT4 nu este o valoare direct cuantificată, ci mai degrabă estimată printr-o metodă sensibilă la proteine (influențată de TBG și albumină) și care, prin urmare, este puternic modificată de sarcină și variază, de asemenea, în funcție de trimestru. În plus, fiecare metodă de testare are variații specifice. Aceasta înseamnă că, pentru o interpretare adecvată a FT4 în timpul sarcinii, trebuie să se dispună de valori de referință în funcție de vârsta gestațională și de metoda utilizată, așa cum afirmă American Thyroid Association (ATA).6
Impactul hipertiroidismului asupra mamei și fătului
După cum se arată în tabelul 2, hipertiroidismul în timpul sarcinii poate avea consecințe grave atât pentru mamă și făt, cât și, după naștere, pentru nou-născut.10-12 De asemenea, trebuie remarcat faptul că în hipertiroidismul endogen a fost recent raportat un risc crescut de tromboză, aparent reversibil odată cu controlul hipertiroidismului.13 Din cauza riscului crescut de tromboză venoasă profundă și de tromboembolism pulmonar în timpul sarcinii,14 trebuie menținut un nivel ridicat de suspiciune pentru a permite depistarea precoce a acestei complicații și poate fi necesară luarea în considerare a unor măsuri profilactice.
Impactul materno-fetal al hipertiroidismului.
Maternal
Avort spontan
Preeclampsie (multiplică riscul×5)7
Naștere prematură (multiplică riscul×10)12
. Abruptio placentae
Insuficiență cardiacă (înmulțește riscul×20)12
Furtună tiroidiană (înmulțește riscul×10)12
Tromboză venoasă13
Fetală
Scăzută greutate mică la naștere
Întârziere de creștere intrauterină
Prematuritate
Mici pentru vârsta gestațională
Moarte fetală
Disfuncție tiroidiană (hipertiroidism) sau hipotiroidism)
Gușă fetală
Neonatală
Hipertiroidism tranzitoriu
Hipotiroidism tranzitoriu sau permanent
Clasificarea hipertiroidismului în timpul sarcinii
Tabelul 3 descrie diferitele posibilități de diagnostic atunci când hipertiroidismul apare în timpul sarcinii. Pe de o parte, există o serie de afecțiuni care rezultă direct din sarcina însăși, care pot fi înglobate sub denumirea de tirotoxicoză gestațională tranzitorie (TGT). Pe de altă parte, orice afecțiune care duce la hiperfuncție tiroidiană în afara sarcinii poate apărea și în timpul sarcinii. În cele din urmă, nivelurile crescute de TH pot apărea și din cauza aportului exogen de TH.
Clasificarea etiologică a hipertiroidismului în sarcină.
Tirotoxicoza gestațională tranzitorie
Hiperemesis gravidarum
Sarcina multiplă
Hipertiroidismul trofoblastic (mol, coriocarcinom)
Hiperreactio luteinalis
Tirotoxicoza gestațională familială
Hiperplacentare
Boală tiroidiană
Boala Graves
. Tiroidită
Gușă multinodulară
Adenom tiroidian toxic
Iatrogenă
Supratratament
Tratament excesiv
Ingestie involuntară de hormoni tiroidieni (contaminare alimentară, etc.)
Factice
Tirotoxicoza gestațională tranzitorie
Este cea mai frecventă cauză de hipertiroidism în timpul sarcinii și poate apărea la 1-3% din toate sarcinile.15,16 A fost definită ca un hipertiroidism tranzitoriu care se limitează la prima jumătate a sarcinii și se caracterizează prin niveluri crescute de FT4 sau TT4 (ajustate) cu TSH suprimat sau nedetectabil în absența autoanticorpilor tiroidieni16 sau a unor caracteristici fizice care sugerează boala Graves (GD).17 Aceasta este de obicei rezultatul unor niveluri crescute de HCG sau de la o afinitate mai mare pentru receptorii TSH.
Cea mai caracteristică afecțiune din acest grup (tabelul 3) este hyperemesis gravidarum (HG), dar există și alte afecțiuni asociate cu niveluri crescute de HCG, cum ar fi sarcina multiplă sau boala trofoblastică (mola hidatică sau coriocarcinom) cu o prevalență a TGT de până la 50%.17 Există, de asemenea, și alte cauze mai puțin frecvente, cum ar fi hiperreactio luteinalis,18 caracterizată prin formarea de chisturi de theca-luteină în cadrul sarcinii, sau hiperplacentoza,19 unde se observă o creștere a greutății placentei și a producției de HCG. Există, de asemenea, o afecțiune familială (tirotoxicoza gestațională familială20) în care apare o hipersensibilitate a receptorului TSH la nivelurile fiziologice de HCG din cauza unei mutații autosomale dominante; aceasta se caracterizează clinic prin apariția TGT la toate sarcinile și la toate femeile din familie cu niveluri normale de HCG.
Hiperemesis gravidarum
Cea mai frecventă cauză de TGT este HG. HG apare la 0,5-10/1000 din toate sarcinile,21 și este asociată cu niveluri crescute de TH liber și supresia TSH în 30-60% din cazuri.22 Trebuie remarcat faptul că conceptul de HG ar trebui să fie restrâns la condițiile asociate în primul trimestru de sarcină cu vărsături, deshidratare, pierdere de cel puțin 5% din greutatea corporală și cetonurie.23
În aceste cazuri, hipertiroidismul se caracterizează prin supresia nivelurilor de TSH și creșteri minime de FT4, cu niveluri de FT3 frecvent normale. Hiperfuncția tiroidiană, precum și vărsăturile asociate, se rezolvă de obicei spontan înainte de săptămâna 20, iar tratamentul simptomatic cu hidratare intravenoasă și complex de vitamina B este suficient pentru a preveni riscul excepțional de encefalopatie Wernicke.24 Nu există dovezi că tratamentul cu medicamente antitiroidiene (ATD) aduce vreun beneficiu25 și, prin urmare, utilizarea lor este nerecomandată.6
Excepțional, HG cu o componentă de hiperfuncție tiroidiană foarte vizibilă sau GD cu intoleranță gastrointestinală asociată (greață și vărsături) pot sugera necesitatea unui diagnostic diferențial între ele. Tabelul 4 prezintă principalele diferențe. În orice caz, dacă hipertiroidismul durează dincolo de primul trimestru de sarcină, trebuie suspectată o altă cauză decât TGT.
Diferențe între boala Graves și hiperemeză.
| Semnul | Boala lui Graves | Hiperemeză | |
| Simptome de hipertiroidism înainte de sarcină | ++ | – | |
| Simptome de hipertiroidism în timpul sarcinii | +/++ | -/+ | |
| Nausee/vomită | -/+ | +++ | |
| Goiter/oftalmopatie | + | – | |
| Anticorpi tiroidieni | ++ | – | |
| T-US | Hipervascular | Normal | |
| Antecedente familiale de HG | – | + | |
| Simptome similare în sarcina anterioară | – | + | |
| T4 | |||
| T3 | |||
| >TT3/TT4 raport | >20 |
T-.US: ecografie tiroidiană; HG: hyperemesis gravidarum.
Boala Graves
Dintre bolile tiroidiene, GD este cea mai frecventă cauză de hipertiroidism în sarcină, apărând la 0,1-1% din toate sarcinile (hipertiroidism clinic și subclinic la 0,4% și respectiv 0,6%).10
Historia naturală a GD în timpul sarcinii este o exacerbare a simptomelor în primul trimestru datorită efectului aditiv al stimulării de către HCG a receptorului TSH, urmată de o ameliorare în a doua jumătate a sarcinii datorită efectului imunomodulator al sarcinii și de reapariția acesteia după naștere.
Boala Graves în sarcină
Simptomele GD active în sarcină nu diferă de cele tipice afecțiunii. Unele simptome pot fi uneori confundate cu cele ale sarcinii propriu-zise. Posibila prezență a semnelor oculare și a gușei ajută la clarificarea afecțiunii, iar măsurătorile hormonale permit stabilirea diagnosticului.
Tratamentul bolii Graves în sarcină
După cum se știe, există trei abordări terapeutice potențiale pentru GD la femeile care nu sunt gravide: 131I, intervenția chirurgicală sau tratamentul medical cu ATD. Dintre aceste trei opțiuni, administrarea de 131I este contraindicată în sarcină din cauza riscului de malformație7 și, prin urmare, opțiunile sunt limitate la tiroidectomie sau la utilizarea de ATD. În ceea ce privește intervenția chirurgicală, aceasta trebuie efectuată numai în circumstanțe excepționale, așa cum se discută mai jos.
Tratament medical. Medicamente antitiroidiene
Pentru tratamentul medical al GD în sarcină, propiltiouracilul (PTU) a fost considerat în mod tradițional ca fiind tratamentul de elecție în comparație cu metimazol/carbimazol (MM/CM) până acum câțiva ani.26 Acest concept se baza pe unele studii care sugerau transferul placentar minim al PTU în comparație cu MM/CM27 și pe efectele teratogene ale MM/CM. În prezent se știe că ambele ATD traversează placenta și, prin urmare, au aceleași șanse de a afecta fătul și de a provoca hipotiroidism fetal.26
În plus, rolul MM/CM în apariția la făt a aplasiei cutanate și a atreziei choanale și esofagiene, împreună cu alte câteva malformații denumite global „metimazol embriopatie”,28 a fost foarte controversat,29-31 iar aceste malformații au fost atribuite în unele cazuri efectelor nocive ale hipertiroidismului propriu-zis. Studii recente,32,33 arată însă că MM/CM are efecte teratogene, spre deosebire de PTU.
Pe de altă parte, în ultimii ani au apărut raportări de cazuri de hepatită toxică fulminantă la pacienți tratați cu PTU,34,35 cu rate de prevalență cuprinse între 0,1% și 0,5% și o rată de mortalitate ridicată (25-50%).10,36 Au fost raportate chiar și cazuri de hepatită neonatală la nou-născuții născuți din mame care au fost tratate cu PTU.37,38
Ne aflăm așadar în fața unei dileme: pe de o parte, pare să fie clar recunoscut faptul că MM/CM implică un risc de malformații, iar pe de altă parte, că PTU poate provoca complicații fatale.
În fața acestei alternative, unii autori au recomandat terapia de ablație înainte de sarcină la femeile cu GD.39 Totuși, această soluție abia rezolvă problema, deoarece femeile cu GD nu planifică sarcina în majoritatea cazurilor. Pe de altă parte, această măsură nu previne un eventual hipertiroidism fetal (Fhyper) datorat persistenței unor niveluri ridicate de anticorpi tiroid-stimulatori (TSI), care necesită tratament medical, ridicând astfel din nou problema.
Din acest motiv, ATA a stabilit criteriile de utilizare a PTU în populația generală și la femeile gravide.40 Pentru sarcină, ATA sfătuiește împotriva utilizării MM/CM în primul trimestru de sarcină (perioada de organogeneză) și recomandă utilizarea PTU. După săptămâna 12 de sarcină, PTU trebuie întrerupt din cauza riscului de afecțiuni hepatice, iar controlul GD trebuie continuat cu MM/CM. În afara sarcinii, utilizarea PTU este recomandată doar în două circumstanțe: în primul rând, dacă apare furtuna tiroidiană și, în al doilea rând, în prezența efectelor adverse induse de MM/CM.
Pentru a evita întârzierea începerii tratamentului cu PTU, este recomandabil ca femeile cu GD care pot rămâne potențial gravide și care nu utilizează nicio metodă contraceptivă să aibă la dispoziție PTU la domiciliu și să fie instruite să schimbe medicația (de la MM/CM la PTU) imediat ce se verifică sarcina.
Tratament medical. Management clinic
După cum s-a discutat mai sus, tratamentul GD în timpul sarcinii trebuie să constea în PTU în primul trimestru și MM/CM ulterior. Doza inițială poate varia de la 50 până la 300mg/zi de PTU în trei doze divizate, 5 până la 15mg/zi de metimazol sau 10 până la 15mg/zi de carbimazol în doză unică.6 Trebuie să se încerce întotdeauna să se utilizeze cea mai mică doză posibilă.
Beta-blocantele trebuie utilizate doar tranzitoriu, deoarece utilizarea lor pe termen lung a fost asociată cu retard de creștere intrauterină, bradicardie și hipoglicemie neonatală.41 Mai mult, unii autori au raportat o creștere a numărului de avorturi spontane în cazul tratamentului combinat cu propranololol și ATD.42
Când se ajustează doza de ATD, trebuie să se încerce să se mențină funcția tiroidiană a mamei aproape de limita hiperfuncției subclinice, deoarece glanda tiroidă a fătului este mult mai sensibilă la efectul de blocare al ATD. De fapt, prezența unei TSH detectabile este o indicație că doza de ATD trebuie diminuată.10,43
GD în timpul sarcinii prezintă o evoluție foarte dinamică, astfel încât până la 20%-30% dintre paciente ating un grad de control care permite întreruperea ATD în ultimul trimestru de sarcină.44 Utilizarea unei scheme combinate (ATD și TH) pentru tratamentul GD este absolut contraindicată în sarcină, deoarece determină hipotiroidism fetal (Fhypo).6,43
Chirurgie
În ceea ce privește utilizarea chirurgiei pentru controlul GD la gravide, diferitele consensuri și ghiduri clinice6,7,43 sunt de acord în a o recomanda numai dacă apar următoarele:
- 1
Reacții adverse la ATD care împiedică utilizarea lor.
- 2
Necesitatea unor doze mari de ATD.
- 3
Nerespectarea de către pacient a tratamentului medical.
În plus, ghidurile italiene43 recomandă, de asemenea, intervenția chirurgicală pentru cazurile de gușă maternă extinsă cu compresie a căilor respiratorii.
Dacă se efectuează, cel mai bun moment pentru intervenție chirurgicală este începând cu al doilea trimestru. Acest lucru justifică utilizarea beta-blocantelor și a iodurii de sodiu (50-100mg/zi)45 pentru o perioadă scurtă de timp (10-14 zile) la gravidele cu GD ca pregătire pentru operație. După cum s-a discutat mai sus, trebuie evitat tratamentul pe termen lung cu beta-blocante. De asemenea, trebuie să se manifeste prudență atunci când se administrează iodură de potasiu pentru a preveni apariția gușei și/sau a Fhypo.
Operația chirurgicală determină o schimbare profundă a situației. Pe de o parte, hipertiroidismul este rezolvat la gravide, dar hipotiroidismul este indus la mamă, necesitând o înlocuire rapidă și o monitorizare regulată a TSH. De asemenea, trebuie controlate nivelurile de TSI, iar hipertiroidismul fetal trebuie monitorizat, dacă este necesar.
Schimbări ale autoimunității tiroidiene în timpul sarcinii
Câțiva autori au demonstrat, cel puțin în unele cazuri, că activitatea funcțională a anticorpilor împotriva receptorului TSH se schimbă de la o activitate stimulatoare la una inhibitoare sau blocantă.46,47 Aceasta înseamnă că sarcina modulează nu numai nivelurile de autoanticorpi, ci și profilul lor funcțional. Acest concept implică faptul că GD în timpul sarcinii poate evolua nu numai spre o funcție normală, ci chiar spre hipofuncție din cauza acestei modificări a activității stimulatoare-blocante, așa cum a fost raportat în unele cazuri.48 Altfel spus, GD în sarcină este un proces schimbător care necesită o monitorizare constantă și regulată și care nu trebuie neglijat chiar și atunci când s-a ajuns la o situație de remisiune aparentă care nu necesită ATD.
Măsurarea anticorpilor antistimulatori tiroidieni în sarcină
Pentru a preveni impactul potențialilor autoanticorpi ai IAT asupra glandei tiroide fetale, în 1998 ETA a publicat49 criterii care stabilesc indicațiile pentru măsurarea IAT în sarcină în funcție de caracteristicile GD la mamă (tabelul 5).
Indicații pentru măsurarea IOT conform Asociației Europene de Tiroidă.
(I) Femeia eutiroidă cu GD vindecată cu tratament medical înainte de sarcină
– Nu se măsoară
(II) Femeia eutiroidă cu GD vindecată după131I sau intervenție chirurgicală
– Se măsoară TSI precoce: dacă este pozitivă, se monitorizează hipertiroidismul fetal
– Măsurați TSI în trimestrul al treilea (dacă este pozitivă în primul trimestru): dacă este pozitivă, monitorizați hipertiroidismul neonatal
(III) Femeia tratată pentru GD în timpul sarcinii
– Măsurați TSI în al treilea trimestru dacă este pozitivă, monitorizați hipertiroidismul neonatal
GD: Boala Graves.
Sursa: Laurberg et al.49
În cazurile în care GD a fost vindecată înainte de sarcină cu tratament medical, se consideră că afecțiunea imună este rezolvată și nu este necesară măsurarea TSI.
Când GD este rezolvată cu ajutorul terapiei de ablație (chirurgie sau radioterapie), afecțiunea imună poate persista. Nivelurile TSI devin de obicei negative la 12-18 luni după operație. După terapia de ablație cu 131I, nivelurile cresc inițial în primele câteva luni și ulterior scad, deși pot rămâne ridicate timp de până la cinci ani.50 Acest lucru înseamnă că, pentru a preveni un potențial Fhyper după 131I, trebuie menținută contracepția pe termen lung. Astfel, la femeile care doresc să conceapă și care au titruri ridicate de ITI, este de preferat intervenția chirurgicală în locul 131I. În toate aceste cazuri, nivelurile TSI trebuie să fie cuantificate precoce pentru a evalua riscul potențial de HF și trebuie măsurate din nou în trimestrul al treilea pentru a vedea dacă acestea continuă să fie pozitive și dacă există, prin urmare, un risc de hipertiroidism neonatal.
În cazul unei GD active în timpul sarcinii, riscul potențial de Fhyper este controlat prin tratamentul mamei cu ATD. Cu toate acestea, se consideră recomandabilă testarea TSI la sfârșitul sarcinii pentru a evalua riscul de hipertiroidism neonatal.
ATA6 recomandă testarea la aproximativ 20-24 de săptămâni și stabilește recomandări mult mai generale:
- –
Mamă cu hipertiroidism activ.
- –
Istoric de tratament cu 131I.
- –
Tiroidectomie anterioară.
- –
Nou-născut anterior cu hipertiroidism.
Boala Graves la făt
Trebuie avut în vedere faptul că glanda tiroidă fetală ajunge la maturitate începând cu săptămâna 20 și, prin urmare, este capabilă să răspundă la aceleași influențe (ATD și TSI) ca și glanda tiroidă adultă. Din acest motiv, atât Fhypo cât și Fhyper pot fi întâlnite în cadrul GD în sarcină.
Hipotiroidismul fetal
Fhypo apare de obicei din cauza supradozajului relativ de ATD, care poate menține o funcție normală la mamă, dar determină o hipofuncție clară la făt.
Semne clinice sugestive
Afecțiunea poate fi suspectată clinic pe baza gușei fetale în ecografia obstetricală și în apariția polihidramniosului la o gravidă tratată cu ATD.
Prezența gușei fetale, indiferent de aspectele funcționale, este un semnal de alarmă datorită efectului său de masă51 (Fig. 1). Trebuie ținut cont de faptul că mărirea de volum a tiroidei determină hiperextensia cefei fătului, ceea ce, la rândul său, afectează mobilitatea intrauterină a fătului și, în consecință, duce la o prezentare anormală la naștere (distocie de umăr, prezentare în decubit dorsal etc.). Chiar dacă această hiperextensie nu împiedică o poziție cefalică adecvată a fătului, ea împiedică flexia adecvată a gâtului fetal pentru naștere, cauzând prezentarea cu fața. Toate aceste situații impun efectuarea unei operații cezariene. Cu toate acestea, aceasta nu este principala complicație, deoarece compresia exercitată de gușă asupra cartilajelor traheale imature ale fătului poate provoca compresie traheală și esofagiană. Aceasta are ca rezultat obstrucția căilor respiratorii, cu riscul aferent de asfixie. Mai mult, compresia esofagiană afectează înghițirea lichidului amniotic, ceea ce duce la acumularea de lichid și la apariția polihidramniosului. Aceasta favorizează nașterea prematură, principala cauză de morbiditate și mortalitate neonatală.
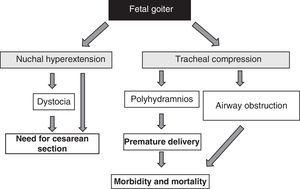
Consecințele dezvoltării gușei la făt.
Diagnostic
Singura procedură pe deplin fiabilă pentru confirmarea unei suspiciuni de Fhypo este măsurarea nivelurilor de TH fetal cu ajutorul cordocentezei. Aceasta este o procedură care nu este lipsită de complicații (este asociată cu un risc de 2% de moarte fetală52) și este mai complexă decât simpla amniocenteză. Cu toate acestea, măsurarea nivelurilor de TH fetal în lichidul amniotic nu este fiabilă și nu se corelează cu măsurarea acestora în sângele fetal.53 Trebuie avut în vedere faptul că în lichidul amniotic se pot găsi TH de origine maternă.54 Conform diferitelor ghiduri,6,43, cordocenteza trebuie efectuată numai atunci când se detectează gușă la un făt a cărui mamă ia ATD și nu se poate pune un diagnostic cert de Fhyper sau Fhypo, și întotdeauna într-un centru cu experiență.
În locul acestei abordări, s-a sugerat recent măsurarea compusului W, rezultat din metabolismul THs fetale. La făt, spre deosebire de adulți, metabolismul THs urmează calea de sulfo-conjugare pentru a forma sulfat de diiodotironină; acest compus este la rândul său metilat în placentă și în peretele uterin înainte de a trece în circulația maternă și de a forma compusul W. Acest compus se găsește la toate femeile gravide de la dezvoltarea funcției tiroidiene fetale și crește treptat în timpul sarcinii, dispărând după naștere. Prin urmare, a fost propus ca marker al funcției tiroidiene fetale.55 În acest context, o evoluție neadecvată a nivelului compusului W la o gravidă tratată cu ATD poate sugera apariția Fhypo.56 Cu toate acestea, pentru moment, aceasta nu este decât o metodă cvasi-experimentală.
Tratament
Prima măsură care trebuie luată este întreruperea ATD. Cu toate acestea, din cauza latenței efectelor ATD odată întrerupte, este necesară și înlocuirea TH până la recuperarea completă a glandei tiroide fetale. Trecerea placentară a TH-urilor este limitată și, prin urmare, acestea trebuie administrate pe cale intraamniotică. Această cale, deși invazivă, este mult mai sigură decât cordocenteza, cu un risc minim de avort spontan după prima jumătate a sarcinii.57
În ceea ce privește tratamentul intraamniotic al fătului cu T4, nu există o schemă de tratament stabilită, iar datele din literatură sunt destul de contradictorii.53,58,59 O analiză recentă51 a cazurilor raportate până în prezent a concluzionat că doza medie este de aproximativ 279μg de levotiroxină o dată pe săptămână (timp de una până la șase săptămâni). Aceasta pare să inverseze gușa fetală la 0,5-2,5 săptămâni după prima doză. În unele cazuri au fost efectuate măsurători repetate ale TH, în timp ce în altele dispariția gușei a fost monitorizată doar prin ecografie.
Hipertiroidism fetal
Hiperul este o complicație rară și poate apărea la până la 1-2% dintre copiii născuți de mame cu GD actuală sau anterioară, deși este posibil să fie o afecțiune subdiagnosticată.60,61
Dezvoltarea Fhyper, cu excepția cazurilor foarte rare de mutații ale receptorului TSH,62 poate fi rezultatul unei GD slab controlate la o femeie gravidă sau, mai frecvent, poate apărea la o femeie gravidă cu GD vindecată înainte de sarcină cu terapie de ablație care continuă să aibă niveluri ridicate de TSI. Indicațiile pentru măsurarea TSI pentru a stabili riscul de Fhyper au fost deja discutate. Nivelurile TSI de 3 sau 5 ori mai mari decât cele normale6,63 implică un risc de Fhyper.
Semne clinice sugestive
Apariția gușii fetale este una dintre cele mai timpurii caracteristici. Pot fi observate, de asemenea, bradicardie fetală, vârstă osoasă avansată, retard de creștere generală și craniosinostoză.64 În formele mai severe, pot apărea insuficiență cardiacă cu hidrops fetal sau alterarea maturizării sistemului nervos central cu retard mental. În cele din urmă poate apărea nașterea prematură.65
Diagnostic
Semnele menționate mai sus nu sunt definitive; tahicardia nu apare întotdeauna, iar prezența gușei la ecografie este o constatare frecventă în cazul Fhypo. În cazul în care apar îndoieli cu privire la faptul dacă afecțiunea este Fhypo din cauza efectului ATD-urilor sau Fhyper din cauza controlului matern deficitar, unii autori au propus un sistem de punctaj bazat pe datele ecografice66 (tabelul 6). În cazul în care persistă îndoiala, THs fetale ar trebui să fie măsurate prin cordocenteză, așa cum se menționează în secțiunea Fhypo. Compusul W (discutat anterior) poate fi, eventual, util în acest scop în viitor.
Scoring ecografic pentru diferențierea hipertiroidismului de hipotiroidism în gușa fetală.
| Caracteristica ecografică | Puncte | |
| Frecvența cardiacă fetală | ||
| Tahicardie | 1 | |
| Normal | 0 | |
| Vascularizarea gușă | ||
| Centrală | 1 | |
| Periferică sau absentă | 0 | |
| Mișcările fetale | ||
| Normale | 1 | |
| Crescute | 0 | |
| Osulatură maturare | ||
| Accelerată | -1 | |
| Normală | 0 | |
| Întârziat | 1 | |
| Interpretare scor | ||
| ≥2 sugerează hipertiroidism | ||
Tratament
Tratamentul trebuie să se bazeze pe ATD. În acest caz, spre deosebire de Fhypo, tratamentul nu trebuie administrat pe cale intraamniotică, deoarece ATD-urile traversează liber placenta. În cazul apariției Fhyper la o femeie gravidă cu GD slab controlată, este necesară doar ajustarea tratamentului la mamă. În schimb, dacă mama are o funcție normală datorită unui tratament de ablație anterior și doar fătul prezintă hiperfuncție, MM/CM trebuie administrat mamei începând cu doze de 10-20mg/zi. Tratamentul trebuie monitorizat la fiecare 4-5 zile pe baza HR fetale și a evoluției gușei pentru a nu supradoza fătul și a nu provoca Fhypo.10
Dacă mama prezintă hipotiroidism atunci când se administrează ATD, trebuie să i se administreze levotiroxină, care abia traversează placenta și, prin urmare, compensează hipotiroidismul fără a afecta fătul. Aceasta este singura circumstanță în care se poate folosi schema combinată.
Boala Graves la nou-născut
La nou-născuți, GD în timpul sarcinii poate cauza atât hipertiroidism, cât și hipotiroidism.
Hipertiroidism neonatal
Acesta poate apărea la 1-5% dintre copiii născuți la gravidele cu GD10 activă și titruri mari de TSI în ultimul trimestru. Fătul își menține funcția normală în timpul sarcinii datorită efectului ATD-urilor primite de către mamă. ATD-urile au un timp de înjumătățire de 24-72h, iar după această perioadă încetează să mai acționeze asupra glandei tiroide fetale. Aceasta devine expusă la TSI maternă, care poate persista până la 12 săptămâni după naștere.
În consecință, apare o hiperfuncție tiroidiană și chiar insuficiență cardiacă, care apare la câteva zile după naștere la un nou-născut inițial asimptomatic.
Această afecțiune poate apărea și la nou-născuții mamelor care au primit tratament de ablație înainte de sarcină și continuă să aibă niveluri ridicate de TSI, la care a apărut Fhyper nediagnosticat. În aceste cazuri, hipertiroidismul neonatal este o continuare a Fhyper; nou-născuții prezintă o afectare severă, greutate mică și o maturare osoasă accelerată la naștere.
Tratamentul trebuie să constea în administrarea de MM/CM în doze de 0,5-1mg/kg de greutate corporală/zi și propranolol 2mg/kg de greutate corporală/zi36 în funcție de evoluția clinică și ținând cont de faptul că este o situație tranzitorie. Trebuie reținut faptul că STI-urile își pot schimba în cele din urmă profilul funcțional pentru a deveni blocanți ai receptorilor și a dezvolta hipotiroidism.
Ipotiroidism neonatal secundar
La copiii născuți din mame cu GD slab controlată, se poate constata că nivelurile ridicate de TH la care au fost expuse în timpul sarcinii au determinat suprimarea secreției de TSH, ceea ce duce la hipotiroidism secundar la naștere.67 Această situație poate fi tranzitorie sau definitivă, ca urmare a afectării hipofizare permanente a secreției de TSH.
Nou-născuților trebuie să li se administreze levotiroxină, urmată de evaluări regulate până la eventuala recuperare a secreției de TSH.
Se poate observa, de asemenea, hipotiroidism neonatal tranzitoriu datorat persistenței autoanticorpilor materni care blochează receptorul RSH.68
Boala Graves la femeile în postpartum
Boala Graves controlată anterior, fie înainte sau după sarcină, poate recidiva după naștere. Rata de recurență după naștere poate fi de până la 84%, comparativ cu 56% la femeile fără sarcină.69 Prin urmare, se recomandă ca TH matern să fie măsurați la șase săptămâni după naștere și până la un an.10
Dacă GD recidivează, va fi necesar un tratament medical cu MM/CM. Deși ATD-urile sunt secretate în laptele matern, administrarea lor nu implică niciun risc în timpul alăptării, iar până la 20-30 mg de MM/CM pot fi administrate fără impact asupra glandei tiroide a nou-născuților.70 ATD-urile trebuie administrate în doze divizate și întotdeauna după terminarea consumului de lapte.
S-a sugerat că TSI din laptele matern ar putea ajunge în circulația generală a nou-născuților prin epiteliul gastrointestinal imatur al sugarului și ar putea cauza sau prelungi hipertiroidismul neonatal. Cu toate acestea, deocamdată nu există dovezi concludente că acest lucru se întâmplă.71
Addendum
După trimiterea acestui manuscris, Societatea Nord-Americană de Endocrinologie a emis noi ghiduri de practică clinică privind Managementul disfuncției tiroidiene în timpul sarcinii și postpartum (J Clin Endocrinol Metab 2012; 97: 2543-2565). Recomandările oferite în secțiunea privind hipertiroidismul în sarcină nu diferă substanțial de cele discutate în această recenzie.
Conflicte de interese
Autorul declară că nu are conflicte de interese.
.