- Descrever a estrutura e funções das proteínas
- Objectivos de aprendizagem
- Aminoácidos
- Pergunta prática
- A significância evolutiva do citocromo c
- Estrutura da proteína
- Estrutura primária
- Estrutura Secundária
- Estrutura terciária
- Estrutura quaternária
- Denaturação e Dobra de Proteína
- Função das Proteínas
- Em resumo: Proteínas
- Check Your Understanding
Descrever a estrutura e funções das proteínas
Proteínas são polímeros de aminoácidos. Cada aminoácido contém um carbono central, um hidrogênio, um grupo carboxil, um grupo amino e um grupo R variável. O grupo R especifica a que classe de aminoácidos ele pertence: cadeias laterais hidrofílicas carregadas eletricamente, cadeias laterais polares mas não carregadas, cadeias laterais hidrofóbicas não polares e casos especiais.
Proteínas têm diferentes “camadas” de estrutura: primária, secundária, terciária, quaternária.
Proteínas têm uma variedade de funções nas células. As principais funções incluem atuar como enzimas, receptores, moléculas de transporte, proteínas reguladoras para expressão gênica, e assim por diante. Enzimas são catalisadores biológicos que aceleram uma reação química sem serem alterados permanentemente. Eles têm “locais ativos” onde o substrato/reagente se liga e podem ser ativados ou inibidos (inibidores competitivos e/ou não competitivos).
Objectivos de aprendizagem
- Demonstrem familiaridade com unidades monoméricas de proteínas: aminoácidos
- Definir as diferentes camadas da estrutura da proteína
- Identificar várias funções principais das proteínas
>
>
Aminoácidos
>
Proteínas são uma das moléculas orgânicas mais abundantes nos sistemas vivos e têm a mais diversa gama de funções de todas as macromoléculas. As proteínas podem ser estruturais, regulatórias, contráteis ou protetoras; podem servir no transporte, armazenamento ou membranas; ou podem ser toxinas ou enzimas. Cada célula de um sistema vivo pode conter milhares de proteínas, cada uma com uma função única. As suas estruturas, tal como as suas funções, variam muito. No entanto, são todos polímeros de aminoácidos, dispostos numa sequência linear.

Figure 1. Os aminoácidos têm um carbono assimétrico central ao qual estão ligados um grupo amino, um grupo carboxilo, um átomo de hidrogênio e uma cadeia lateral (grupo R).
Aminoácidos são os monômeros que compõem as proteínas. Cada aminoácido tem a mesma estrutura fundamental, que consiste em um átomo central de carbono, também conhecido como carbono alfa (α), ligado a um grupo amino (NH2), a um grupo carboxilo (COOH), e a um átomo de hidrogênio. Cada aminoácido também tem outro átomo ou grupo de átomos ligados ao átomo central conhecido como grupo R (Figura 1).
O nome “aminoácido” é derivado do fato de que eles contêm tanto o grupo de aminoácidos quanto o grupo carboxil-ácido em sua estrutura básica. Como mencionado, há 20 aminoácidos presentes nas proteínas. Dez destes são considerados aminoácidos essenciais em humanos porque o corpo humano não os pode produzir e são obtidos da dieta.
Para cada aminoácido, o grupo R (ou cadeia lateral) é diferente (Figura 2).
Pergunta prática

Figure 2. Existem 20 aminoácidos comuns comumente encontrados em proteínas, cada um com um grupo R diferente (grupo variante) que determina sua natureza química.
Que categorias de aminoácidos você esperaria encontrar na superfície de uma proteína solúvel, e que você esperaria encontrar no interior? Que distribuição de aminoácidos você esperaria encontrar em uma proteína embutida em um bico lipídico?
A natureza química da cadeia lateral determina a natureza do aminoácido (ou seja, se é ácido, básico, polar ou não-polar). Por exemplo, o aminoácido glicina tem um átomo de hidrogênio como o grupo R. Aminoácidos como valina, metionina e alanina são não-polares ou hidrofóbicos na natureza, enquanto aminoácidos como serina, treonina e cisteína são polares e têm cadeias laterais hidrofílicas. As cadeias laterais de lisina e arginina são carregadas positivamente, e portanto estes aminoácidos também são conhecidos como aminoácidos básicos. A prolina tem um grupo R que está ligado ao grupo de aminoácidos, formando uma estrutura semelhante a um anel. A prolina é uma exceção à estrutura padrão de um ácido animo, uma vez que seu grupo de aminoácidos não é separado da cadeia lateral (Figura 2).
Aminoácidos são representados por uma única letra maiúscula ou uma abreviação de três letras. Por exemplo, valina é conhecida pela letra V ou pelo símbolo de três letras val. Assim como alguns ácidos gordos são essenciais para uma dieta, alguns aminoácidos também são necessários. Eles são conhecidos como aminoácidos essenciais, e em humanos eles incluem isoleucina, leucina, e cisteína. Aminoácidos essenciais referem-se àqueles necessários para a construção de proteínas no organismo, embora não produzidos pelo organismo; quais aminoácidos são essenciais varia de organismo para organismo.

Figure 3. A formação de ligações peptídicas é uma reação de síntese de desidratação. O grupo carboxilo de um aminoácido está ligado ao grupo aminoácido do aminoácido que entra. No processo, uma molécula de água é liberada.
A sequência e o número de aminoácidos determinam a forma, tamanho e função da proteína. Cada aminoácido é ligado a outro aminoácido por uma ligação covalente, conhecida como ligação peptídea, que é formada por uma reação de desidratação. O grupo carboxil de um aminoácido e o grupo aminoácido do aminoácido que entra se combinam, liberando uma molécula de água. A ligação resultante é a ligação peptídeo (Figura 3).
Os produtos formados por tais ligações são chamados de peptídeos. Como mais aminoácidos se juntam a esta cadeia crescente, a cadeia resultante é conhecida como polipéptido. Cada polipeptídeo tem um grupo de aminoácidos livres em uma extremidade. Esta extremidade é chamada terminal N, ou o amino terminal, e a outra extremidade tem um grupo carboxil livre, também conhecido como terminal C ou carboxil. Enquanto os termos polipeptídeo e proteína são às vezes utilizados de forma intercambiável, um polipeptídeo é tecnicamente um polímero de aminoácidos, enquanto o termo proteína é utilizado para um polipeptídeo ou polipeptídeos que se combinaram entre si, muitas vezes têm grupos protéticos não-peptídicos ligados, têm uma forma distinta e têm uma função única. Após a síntese proteica (tradução), a maioria das proteínas é modificada. Estas são conhecidas como modificações pós-tradução. Elas podem sofrer clivagem, fosforilação, ou podem requerer a adição de outros grupos químicos. Somente após estas modificações a proteína é completamente funcional.
A significância evolutiva do citocromo c
Citocromo c é um componente importante da cadeia de transporte de elétrons, uma parte da respiração celular, e é normalmente encontrada na organela celular, a mitocôndria. Esta proteína tem um grupo protético heme, e o íon central do heme fica alternadamente reduzido e oxidado durante a transferência dos elétrons. Como o papel desta proteína essencial na produção de energia celular é crucial, ela tem mudado muito pouco ao longo de milhões de anos. A sequência proteica mostrou que existe uma quantidade considerável de homologia da sequência de aminoácidos do citocromo c entre diferentes espécies; em outras palavras, o parentesco evolutivo pode ser avaliado medindo as semelhanças ou diferenças entre as sequências de DNA ou proteínas de várias espécies.
Os cientistas determinaram que o citocromo c humano contém 104 aminoácidos. Para cada molécula de citocromo c de organismos diferentes que foram sequenciados até à data, 37 destes aminoácidos aparecem na mesma posição em todas as amostras de citocromo c. Isto indica que pode ter havido um antepassado comum. Ao comparar as sequências de proteínas humanas e de chimpanzés, não foi encontrada qualquer diferença na sequência. Quando as sequências humanas e de macacos rhesus foram comparadas, a única diferença encontrada foi em um aminoácido. Em outra comparação, a sequência humana com levedura mostra uma diferença na 44ª posição.
Estrutura da proteína
Como discutido anteriormente, a forma de uma proteína é crítica para a sua função. Por exemplo, uma enzima pode se ligar a um substrato específico em um local conhecido como o local ativo. Se este local ativo for alterado devido a mudanças locais ou mudanças na estrutura geral da proteína, a enzima pode ser incapaz de se ligar ao substrato. Para entender como a proteína obtém sua forma ou conformação final, precisamos entender os quatro níveis da estrutura da proteína: primária, secundária, terciária e quaternária.
Estrutura primária
A sequência única de aminoácidos em uma cadeia de polipeptídeos é sua estrutura primária. Por exemplo, o hormônio pancreático insulina tem duas cadeias de polipeptídeos, A e B, e eles estão ligados entre si por ligações de dissulfeto. O aminoácido terminal N da cadeia A é a glicina, enquanto o aminoácido terminal C é a asparagina (Figura 4). As sequências de aminoácidos nas cadeias A e B são exclusivas da insulina.
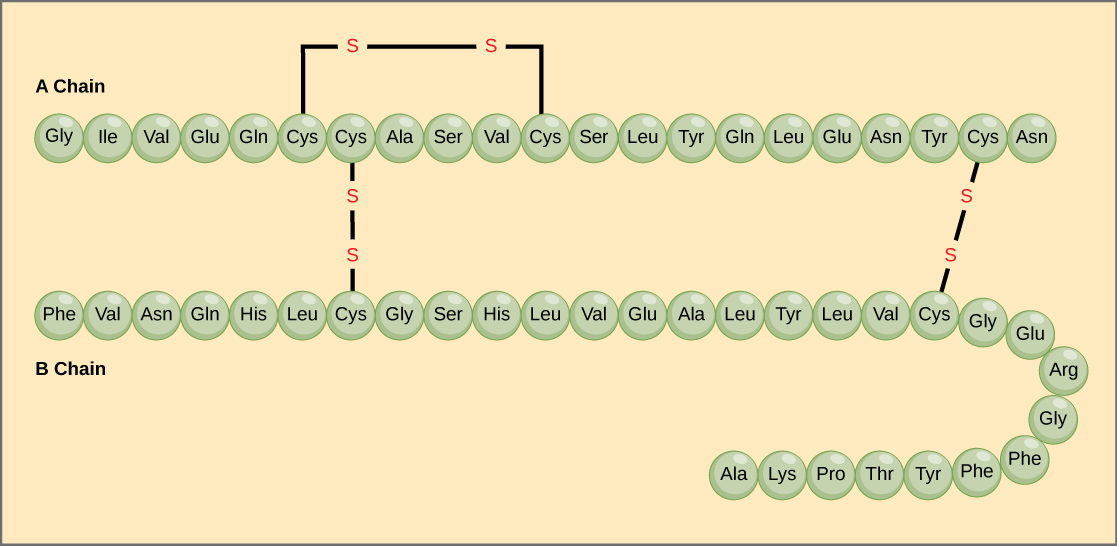
Figure 4. A insulina sérica bovina é uma hormona proteica feita de duas cadeias de peptídeos, A (21 aminoácidos de comprimento) e B (30 aminoácidos de comprimento). Em cada cadeia, a estrutura primária é indicada por abreviaturas de três letras que representam os nomes dos aminoácidos, na ordem em que estão presentes. O aminoácido cisteína (cys) tem um grupo sulfidrílico (SH) como uma cadeia lateral. Dois grupos sulfidrílicos podem reagir na presença de oxigênio para formar uma ligação dissulfeto (S-S). Duas ligações de dissulfureto ligam as cadeias A e B, e uma terceira ajuda a cadeia A a dobrar-se na forma correcta. Note que todas as ligações de dissulfureto têm o mesmo comprimento, mas são desenhadas em tamanhos diferentes para maior clareza.
A sequência única para cada proteína é determinada em última instância pelo gene que codifica a proteína. Uma mudança na sequência de nucleotídeos da região codificadora do gene pode levar à adição de um aminoácido diferente à cadeia de polipeptídeos em crescimento, causando uma mudança na estrutura e função da proteína. Na anemia falciforme, a cadeia da hemoglobina β (uma pequena porção da qual é mostrada na Figura 5) tem uma única substituição de aminoácidos, causando uma mudança na estrutura e função da proteína.
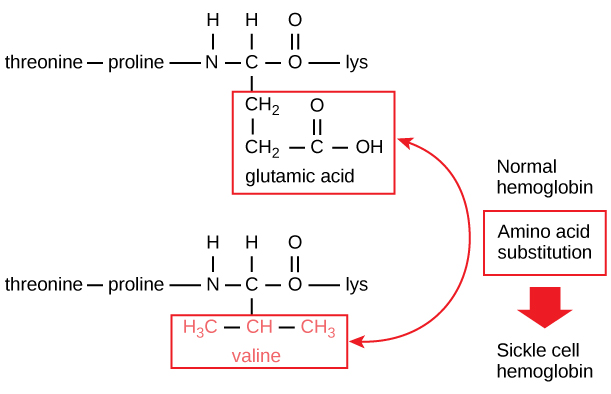
Figure 5. A cadeia beta da hemoglobina tem 147 resíduos em comprimento, mas uma única substituição de aminoácidos leva a anemia falciforme. Na hemoglobina normal, o aminoácido na posição sete é o glutamato. Na hemoglobina falciforme, esse glutamato é substituído por uma valina.
Especificamente, o aminoácido ácido glutâmico é substituído por valina na cadeia β. O mais notável a considerar é que uma molécula de hemoglobina é composta por duas cadeias alfa e duas cadeias beta que consistem cada uma em cerca de 150 aminoácidos. A molécula, portanto, tem cerca de 600 aminoácidos. A diferença estrutural entre uma molécula de hemoglobina normal e uma molécula de foice – que diminui drasticamente a expectativa de vida – é um único aminoácido dos 600. O que é ainda mais notável é que esses 600 aminoácidos são codificados por três nucleotídeos cada, e a mutação é causada por uma única mudança de base (mutação pontual), 1 em 1800 bases.
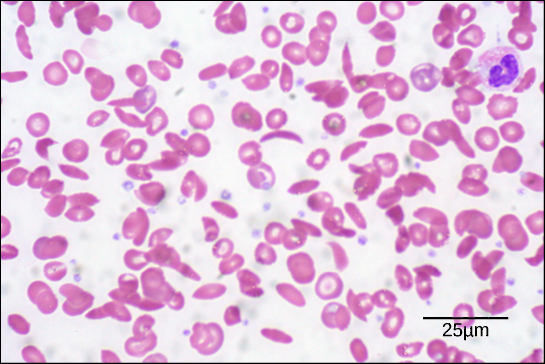
Figure 6. Neste esfregaço de sangue, visualizado com ampliação de 535x usando microscopia de campo brilhante, as células falciformes são em forma de lua crescente, enquanto as células normais são em forma de disco. (crédito: modificação do trabalho de Ed Uthman; dados da barra em escala de Matt Russell)
Por causa desta mudança de um aminoácido na cadeia, as moléculas de hemoglobina formam fibras longas que distorcem os glóbulos vermelhos biconcavos, ou em forma de disco, e assumem uma forma em crescente ou “foice”, que obstrui as artérias (Figura 6). Isto pode levar a uma miríade de problemas de saúde graves, tais como falta de ar, tonturas, dores de cabeça e dores abdominais para aqueles afetados por esta doença.
Estrutura Secundária
A dobra local do polipeptídeo em algumas regiões dá origem à estrutura secundária da proteína. As mais comuns são as estruturas de folhas pregueadas α-helix e β (Figura 7). Ambas as estruturas são a α-estrutura da hélice – a hélice mantida em forma por ligações de hidrogênio. As ligações de hidrogênio se formam entre o átomo de oxigênio no grupo carbonila em um aminoácido e outro aminoácido que é quatro aminoácidos mais distantes ao longo da cadeia.
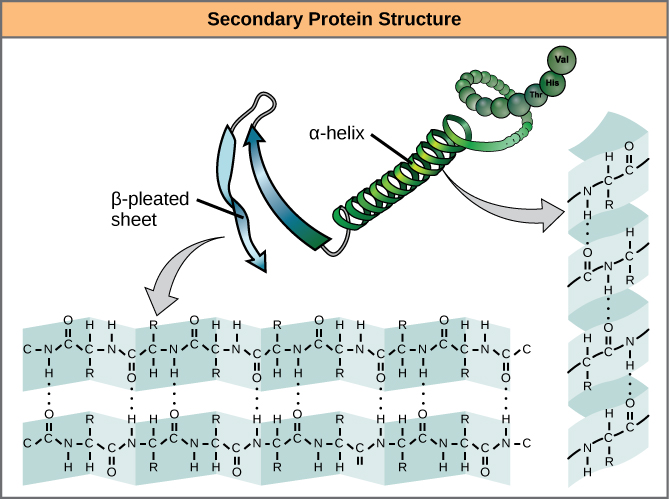
Figure 7. A folha de hélice α e a folha plissada β são estruturas secundárias de proteínas que se formam devido à ligação de hidrogênio entre grupos carbonilo e aminoácidos na espinha dorsal do peptídeo. Alguns aminoácidos têm uma propensão para formar uma hélice α, enquanto outros têm uma propensão para formar uma folha pregueada β.
Tudo o giro helicoidal em uma hélice alfa tem 3,6 resíduos de aminoácidos. Os grupos R (os grupos variantes) do polipeptídio sobressaem da cadeia da hélice α. Na folha plissada β, as “pregas” são formadas pela ligação de hidrogênio entre átomos na espinha dorsal da cadeia de polipeptídeos. Os grupos R são ligados aos carbonos e estendem-se acima e abaixo das dobras da dobra. Os segmentos pregueados alinham paralelos ou antiparalelos entre si, e as ligações de hidrogênio se formam entre o átomo parcialmente positivo de nitrogênio no grupo amino e o átomo parcialmente negativo de oxigênio no grupo carbonilo da espinha dorsal do peptídeo. As estruturas de folhas plissadas α-helix e β são encontradas na maioria das proteínas globulares e fibrosas e desempenham um papel estrutural importante.
Estrutura terciária
A estrutura tridimensional única de um polipeptídeo é a sua estrutura terciária (Figura 8). Esta estrutura é em parte devido a interações químicas no trabalho na cadeia de polipeptídeos. Em primeiro lugar, as interações entre os grupos R criam a complexa estrutura tridimensional terciária de uma proteína. A natureza dos grupos R encontrados nos aminoácidos envolvidos pode neutralizar a formação das ligações de hidrogênio descritas para estruturas secundárias padrão. Por exemplo, os grupos R com cargas semelhantes são repelidos uns pelos outros e aqueles com cargas diferentes são atraídos uns pelos outros (ligações iónicas). Quando a proteína é dobrada, os grupos R hidrofóbicos de aminoácidos não-polares encontram-se no interior da proteína, enquanto os grupos R hidrofílicos encontram-se no exterior. Os primeiros tipos de interacções são também conhecidos como interacções hidrofóbicas. A interação entre cadeias laterais de cisteína forma elos dissulfeto na presença de oxigênio, a única ligação covalente que se forma durante a dobra da proteína.
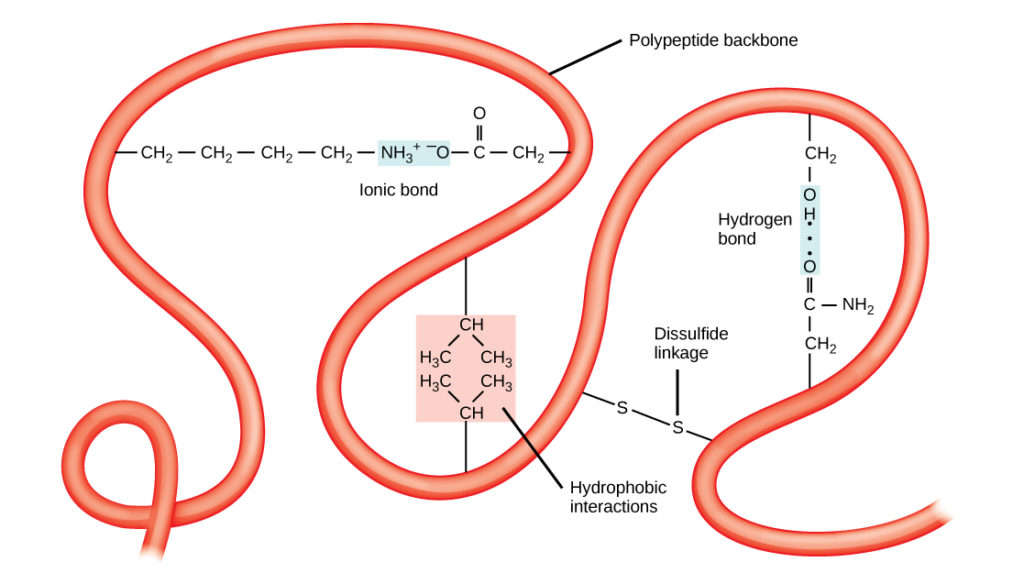
Figure 8. A estrutura terciária das proteínas é determinada por uma variedade de interações químicas. Estas incluem interacções hidrofóbicas, ligações iónicas, ligações de hidrogénio e dissulfureto.
Todas estas interacções, fracas e fortes, determinam a forma tridimensional final da proteína. Quando uma proteína perde sua forma tridimensional, ela pode não ser mais funcional.
Estrutura quaternária
Na natureza, algumas proteínas são formadas a partir de vários polipeptídeos, também conhecidos como subunidades, e a interação dessas subunidades forma a estrutura quaternária. As fracas interações entre as subunidades ajudam a estabilizar a estrutura geral. Por exemplo, a insulina (uma proteína globular) tem uma combinação de ligações de hidrogênio e ligações de dissulfeto que fazem com que ela se aglomere em uma forma de bola. A insulina começa como um único polipéptido e perde algumas sequências internas na presença de modificações pós-tradução após a formação das ligações de dissulfureto que mantêm as cadeias restantes unidas. A seda (uma proteína fibrosa), entretanto, tem uma estrutura de folha plissada β que é o resultado da ligação de hidrogênio entre diferentes cadeias.
Os quatro níveis da estrutura da proteína (primária, secundária, terciária e quaternária) são ilustrados na Figura 9.
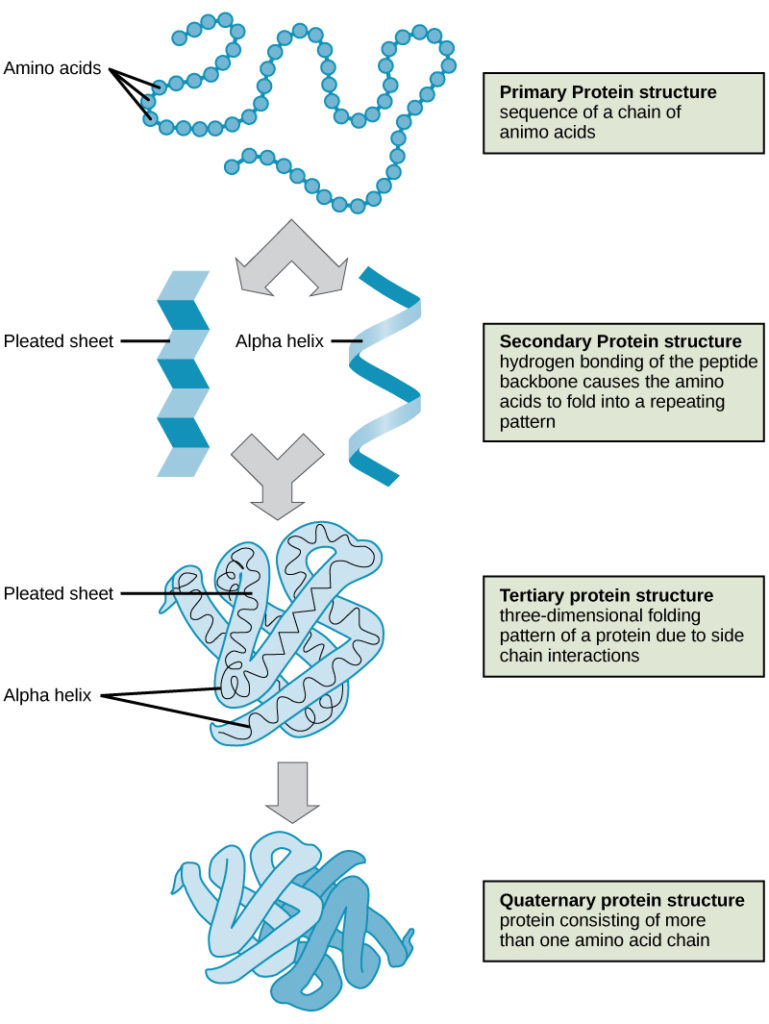
Figure 9. Os quatro níveis da estrutura da proteína podem ser observados nestas ilustrações. (crédito: modificação do trabalho do National Human Genome Research Institute)
Denaturação e Dobra de Proteína
Cada proteína tem sua própria seqüência e forma únicas que são mantidas juntas por interações químicas. Se a proteína estiver sujeita a mudanças na temperatura, pH ou exposição a produtos químicos, a estrutura da proteína pode mudar, perdendo sua forma sem perder sua seqüência primária no que é conhecido como desnaturação. A desnaturação é frequentemente reversível porque a estrutura primária do polipeptídeo é conservada no processo se o agente desnaturante for removido, permitindo que a proteína retome sua função. Algumas vezes a desnaturação é irreversível, levando à perda da função. Um exemplo de desnaturação irreversível da proteína é quando um ovo é frito. A proteína albumina na clara de ovo líquida é desnaturada quando colocada em uma frigideira quente. Nem todas as proteínas são desnaturadas a altas temperaturas; por exemplo, as bactérias que sobrevivem em fontes quentes têm proteínas que funcionam a temperaturas próximas da ebulição. O estômago também é muito ácido, tem um pH baixo, e desnaturam proteínas como parte do processo de digestão; no entanto, as enzimas digestivas do estômago retêm sua atividade sob estas condições.
O dobramento das proteínas é crítico para sua função. Originalmente pensava-se que as próprias proteínas eram responsáveis pelo processo de dobramento. Só recentemente foi descoberto que muitas vezes eles recebem assistência no processo de dobramento por ajudantes proteicos conhecidos como chaperones (ou chaperonins) que se associam com a proteína alvo durante o processo de dobramento. Eles agem evitando a agregação de polipéptidos que compõem a estrutura completa da proteína, e se dissociam da proteína uma vez que a proteína alvo é dobrada.
Função das Proteínas
Os principais tipos e funções das proteínas estão listados na Tabela 1.
| Tabela 1. Tipos de proteínas e funções | ||
|---|---|---|
| Tipo | Exemplos | Funções |
| Enzimas Digestivas | Amilase, lipase, pepsina, tripsina | Ajuda na digestão de alimentos por catabolização de nutrientes em unidades monoméricas |
| Transporte | Hemoglobina, albumina | Carregar substâncias no sangue ou linfa por todo o corpo |
| Estrutura | Actina, tubulina, queratina | Construir diferentes estruturas, como o citoesqueleto |
| Hormonas | Insulina, tiroxina | Coordenar a actividade de diferentes sistemas corporais |
| Defesa | Imunoglobulinas | Proteger o corpo de patogéneos estranhos |
| Contractil | Actina, myosin | Contracção muscular afectada |
| Armazenamento | Proteínas de armazenamento de legumes, clara de ovo (albumina) | Prover alimentação no desenvolvimento precoce do embrião e da plântula |
Duas proteínas especiais e comuns são enzimas e hormonas. Enzimas, que são produzidas por células vivas, são catalisadores em reacções bioquímicas (como a digestão) e são geralmente proteínas complexas ou conjugadas. Cada enzima é específica para o substrato (um reagente que se liga a uma enzima) sobre o qual actua. A enzima pode ajudar na decomposição, rearranjo, ou reacções de síntese. Enzimas que quebram seus substratos são chamadas de enzimas catabólicas, enzimas que constroem moléculas mais complexas a partir de seus substratos são chamadas de enzimas anabólicas, e enzimas que afetam a taxa de reação são chamadas de enzimas catalíticas. Deve-se notar que todas as enzimas aumentam a taxa de reação e, portanto, são consideradas como catalisadores orgânicos. Um exemplo de uma enzima é a amilase salivar, que hidrolisa seu substrato amilose, um componente do amido.
Hormonas são moléculas de sinalização química, geralmente pequenas proteínas ou esteróides, secretadas por células endócrinas que atuam para controlar ou regular processos fisiológicos específicos, incluindo crescimento, desenvolvimento, metabolismo e reprodução. Por exemplo, a insulina é uma hormona proteica que ajuda a regular o nível de glucose no sangue.
Proteínas têm diferentes formas e pesos moleculares; algumas proteínas são globulares em forma enquanto outras são fibrosas na natureza. Por exemplo, a hemoglobina é uma proteína globular, mas o colágeno, encontrado em nossa pele, é uma proteína fibrosa. A forma da proteína é crítica para sua função, e esta forma é mantida por muitos tipos diferentes de ligações químicas. Alterações na temperatura, pH e exposição a produtos químicos podem levar a alterações permanentes na forma da proteína, levando à perda da função, conhecida como desnaturação. Todas as proteínas são compostas de diferentes arranjos dos mesmos 20 tipos de aminoácidos.
Em resumo: Proteínas
Proteínas são uma classe de macromoléculas que desempenham uma gama diversificada de funções para a célula. Elas ajudam no metabolismo, fornecendo suporte estrutural e agindo como enzimas, portadores, ou hormônios. Os blocos de construção de proteínas (monômeros) são aminoácidos. Cada aminoácido tem um carbono central que está ligado a um grupo amino, um grupo carboxil, um átomo de hidrogênio e um grupo R ou cadeia lateral. Existem 20 aminoácidos que ocorrem comumente, cada um deles diferente no grupo R. Cada aminoácido está ligado aos seus vizinhos por uma ligação de peptídeo. Uma longa cadeia de aminoácidos é conhecida como polipéptido.
Proteínas são organizadas em quatro níveis: primário, secundário, terciário, e (opcional) quaternário. A estrutura primária é a sequência única de aminoácidos. A dobra local do polipeptídeo para formar estruturas como a hélice α e a folha plissada β constitui a estrutura secundária. A estrutura tridimensional global é a estrutura terciária. Quando dois ou mais polipeptídeos se combinam para formar a estrutura completa da proteína, a configuração é conhecida como a estrutura quaternária de uma proteína. A forma e função da proteína estão intrinsecamente ligadas; qualquer mudança de forma causada por mudanças de temperatura ou pH pode levar à desnaturação da proteína e a uma perda de função.
Check Your Understanding
Responda a(s) pergunta(s) abaixo para ver o quão bem você entende os tópicos abordados na seção anterior. Este pequeno questionário não conta para a sua nota na classe, e você pode repeti-lo um número ilimitado de vezes.
Utilize este questionário para verificar a sua compreensão e decidir se (1) estudar mais a seção anterior ou (2) passar para a próxima seção.