Einführung
Die Prävalenz von Schilddrüsenfunktionsveränderungen bei Frauen ist sehr hoch (5/1000 für Hypothyreose und 3/1000 für Hyperthyreose1), und da viele dieser Erkrankungen im gebärfähigen Alter auftreten, ist es nicht verwunderlich, dass eine Schwangerschaft mit diesen Krankheiten in Verbindung gebracht wird. Außerdem werden mit der Ausweitung der klinischen Praxis der Messung des Schilddrüsenhormonspiegels (TH) bei Schwangeren immer mehr Anomalien der Schilddrüsenfunktion festgestellt, die unter anderen Umständen übersehen worden wären.
Andererseits verändert sich die mütterliche Schilddrüsenfunktion während der Schwangerschaft erheblich, was zu Veränderungen der verschiedenen Laborparameter führt. Aus diesem Grund sollte bei schwangeren Frauen bei der Interpretation der verschiedenen Schilddrüsenfunktionsparameter anders vorgegangen werden als bei nichtschwangeren Frauen, um Fehldiagnosen und -beurteilungen mit möglicherweise schwerwiegenden Folgen zu vermeiden.
Aus diesem Grund ist in den letzten Jahren ein großes Interesse an der Physiologie und den möglichen Veränderungen der Schilddrüse während der Schwangerschaft entstanden.2 Wir haben uns mit den Aspekten der Hyperthyreose in der Schwangerschaft, ihren Herausforderungen und möglichen Folgen sowohl während der Schwangerschaft (bei der Mutter und/oder dem Fötus) als auch nach der Geburt (bei der Mutter und/oder dem Neugeborenen) befasst.
Funktionelle Beurteilung der Schilddrüse während der Schwangerschaft
Während der Schwangerschaft kommt es zu bedeutenden physiologischen Veränderungen, die einen erheblichen Einfluss auf die verschiedenen Parameter der mütterlichen Schilddrüsenfunktion3,4 haben, darunter die folgenden:
- –
TSH. Im Vergleich zu nicht schwangeren Frauen sind die TSH-Werte in der Schwangerschaft traditionell erniedrigt,5 wobei die Werte im ersten Trimester am niedrigsten sind und dann im zweiten und dritten Trimester ansteigen. Diese Veränderungen des TSH-Spiegels spiegeln die Veränderungen des HCG-Spiegels (humanes Choriongonadotropin) wider, der im ersten Trimester seinen Höhepunkt erreicht und danach allmählich abnimmt. Aus diesem Grund haben die verschiedenen wissenschaftlichen Gesellschaften normale Referenzwerte6-8 festgelegt (Tabelle 1).
Tabelle 1.Referenz-TSH-Werte nach verschiedenen Gesellschaften.
Gesellschaft TSH-Werte (μU/ml) in der Schwangerschaft Erstes Trimenon Zweites Trimenon Drittes Trimenon Endo 2007/SEEN 2009 ATA 2011 0.1-2,5 0,2-3 0,3-3 ATA: American Thyroid Association; Endo: Endocrine Society; SEEN: Spanische Gesellschaft für Endokrinologie und Ernährung.
Quellen: Stagnaro-Green et al.6, Abalovich et al.7 und Galofré et al.8
Es ist zu beachten, dass der TSH-Spiegel bei Mehrlingsschwangerschaften noch stärker abnimmt und dass schwangere Frauen, die rauchen, im ersten und dritten Trimester niedrigere TSH-Spiegel aufweisen.9
- –
TBGT-T4. Die mit der Schwangerschaft verbundenen erhöhten Östrogenspiegel erhöhen den TBG-Spiegel und folglich auch die TT4-Werte. Die Veränderungen der TT4-Werte sind jedoch sehr konsistent (sie steigen um 150 %) und zwar unabhängig vom Trimester und der verwendeten Methode. Wenn also TT4-Werte verfügbar sind, kann die T4-Produktion bei schwangeren Frauen geschätzt werden, indem die Referenzwerte bei nicht schwangeren Frauen mit 1,5 multipliziert werden.
- –
FT4. In der klinischen Praxis werden die meisten Messungen von freiem T4 (FT4) nicht mit den Goldstandard-Methoden der Gleichgewichtsdialyse oder Ultrafiltration durchgeführt. Bei dem routinemäßig verwendeten Verfahren handelt es sich um ein Immunoassay-System, bei dem FT4 nicht direkt quantitativ bestimmt, sondern durch eine proteinempfindliche Methode (beeinflusst durch TBG und Albumin) geschätzt wird, die daher durch die Schwangerschaft stark verändert wird und auch je nach Trimester variiert. Darüber hinaus weist jede Untersuchungsmethode spezifische Abweichungen auf. Das bedeutet, dass für eine adäquate Interpretation von FT4 während der Schwangerschaft Referenzwerte in Abhängigkeit vom Gestationsalter und der verwendeten Methode zur Verfügung stehen müssen, wie die American Thyroid Association (ATA) feststellt.6
Auswirkungen der Hyperthyreose auf die Mutter und den Fötus
Wie in Tabelle 2 dargestellt, kann eine Hyperthyreose während der Schwangerschaft schwerwiegende Folgen sowohl für die Mutter und den Fötus als auch nach der Geburt für das Neugeborene haben.10-12 Es sollte auch beachtet werden, dass vor kurzem über ein erhöhtes Thromboserisiko bei endogener Hyperthyreose berichtet wurde, das offenbar mit der Kontrolle der Hyperthyreose reversibel ist.13 Aufgrund des erhöhten Risikos für tiefe Venenthrombosen und pulmonale Thromboembolien während der Schwangerschaft14 sollte ein hohes Maß an Verdacht aufrechterhalten werden, um eine frühzeitige Erkennung dieser Komplikation zu ermöglichen, und es müssen möglicherweise prophylaktische Maßnahmen in Betracht gezogen werden.
Tabelle 2.Maternal-fetale Auswirkungen der Hyperthyreose.
Mütterliche
Fehlgeburt
Präeklampsie (multipliziert das Risiko×5)7
Frühgeburt (multipliziert das Risiko×10)12
Abruptio placentae
Herzinsuffizienz (vervielfacht das Risiko×20)12
Schilddrüsensturm (vervielfacht das Risiko×10)12
Venöse Thrombose13
Fötales
Niedriges Geburtsgewicht
Intrauterine Wachstumsretardierung
Frühgeburtlichkeit
Klein für das Gestationsalter
Fetaler Tod
Schilddrüsenfunktionsstörung (Hyperthyreose oder Hypothyreose)
Fetale Struma
Neonatal
Vorübergehende Hyperthyreose
Vorübergehende oder dauerhafte Hypothyreose
Quellen: Patil-Sisodia und Mestman10 und Laurberg et al.11.Klassifikation der Hyperthyreose in der Schwangerschaft
Tabelle 3 beschreibt die verschiedenen diagnostischen Möglichkeiten beim Auftreten einer Hyperthyreose in der Schwangerschaft. Einerseits gibt es eine Reihe von Erkrankungen, die direkt aus der Schwangerschaft selbst resultieren und unter dem Begriff transiente Gestations-Thyreotoxikose (TGT) zusammengefasst werden können. Andererseits kann jede Erkrankung, die außerhalb der Schwangerschaft zu einer Schilddrüsenüberfunktion führt, auch während der Schwangerschaft auftreten. Schließlich können erhöhte TH-Spiegel auch durch exogene TH-Zufuhr auftreten.
Tabelle 3.Etiologische Klassifikation der Hyperthyreose in der Schwangerschaft.
Transiente Schwangerschafts-Thyreotoxikose
Hyperemesis gravidarum
Mehrlingsschwangerschaft
Trophoblastische Hyperthyreose (mole, Choriokarzinom)
Hyperreactio luteinalis
Familiäre Gestations-Thyreotoxikose
Hyperplazentose
Schilddrüsenerkrankungen
Morbus Basedow
Schilddrüsenentzündung
Multinoduläre Struma
Toxisches Schilddrüsenadenom
Iatrogene
Überbehandlung
Unbeabsichtigte Aufnahme von Schilddrüsenhormonen (Lebensmittelkontamination, etc.)
Faktisch
Transiente Schwangerschafts-Thyreotoxikose
Dies ist die häufigste Ursache für eine Hyperthyreose während der Schwangerschaft und kann bei 1-3 % aller Schwangerschaften auftreten.15,16 Sie ist definiert als eine vorübergehende Hyperthyreose, die sich auf die erste Hälfte der Schwangerschaft beschränkt und durch erhöhte FT4- oder TT4-Werte (angepasst) mit unterdrücktem oder nicht nachweisbarem TSH bei Fehlen von Schilddrüsen-Autoantikörpern16 oder körperlichen Merkmalen, die auf Morbus Basedow (GD) hindeuten, gekennzeichnet ist.17 Dies ist in der Regel das Ergebnis erhöhter HCG-Werte oder einer größeren Affinität zu TSH-Rezeptoren.
Die charakteristischste Erkrankung innerhalb dieser Gruppe (Tabelle 3) ist Hyperemesis gravidarum (HG), aber es gibt auch andere Erkrankungen, die mit erhöhten HCG-Spiegeln einhergehen, wie z. B. Mehrlingsschwangerschaften oder trophoblastische Erkrankungen (Hydatidenmole oder Choriokarzinom) mit einer TGT-Prävalenz von bis zu 50 %.17 Es gibt auch andere, weniger häufige Ursachen wie die Hyperreactio luteinalis,18 die durch die Bildung von Theca-Lutein-Zysten im Rahmen einer Schwangerschaft gekennzeichnet ist, oder die Hyperplazentose,19 bei der ein erhöhtes Plazentagewicht und eine erhöhte HCG-Produktion zu beobachten sind. Es gibt auch eine familiäre Erkrankung (familiäre gestationale Thyreotoxikose20), bei der eine Hypersensitivität des TSH-Rezeptors gegenüber physiologischen HCG-Spiegeln aufgrund einer autosomal-dominanten Mutation auftritt; diese ist klinisch dadurch gekennzeichnet, dass sich bei allen Schwangerschaften und bei allen Frauen der Familie mit normalen HCG-Spiegeln eine TGT entwickelt.
Hyperemesis gravidarum
Die häufigste Ursache einer TGT ist HG. HG tritt bei 0,5-10/1000 aller Schwangerschaften auf21 und ist in 30-60 % der Fälle mit erhöhten freien TH-Spiegeln und TSH-Suppression verbunden.22 Es ist zu beachten, dass der Begriff HG auf Zustände beschränkt werden sollte, die im ersten Trimester der Schwangerschaft mit Erbrechen, Dehydratation, Verlust von mindestens 5 % des Körpergewichts und Ketonurie einhergehen.23
In diesen Fällen ist die Hyperthyreose durch die Suppression der TSH-Spiegel und minimale FT4-Anstiege gekennzeichnet, wobei die FT3-Spiegel in der Regel normal sind. Die Schilddrüsenüberfunktion und das damit verbundene Erbrechen verschwinden in der Regel spontan vor der 20. Woche, und eine symptomatische Behandlung mit intravenöser Flüssigkeitszufuhr und Vitamin-B-Komplex ist ausreichend, um das außergewöhnliche Risiko einer Wernicke-Enzephalopathie zu verhindern.24 Es gibt keine Belege dafür, dass eine Behandlung mit Antischilddrüsenmedikamenten (ATD) irgendeinen Nutzen bringt,25 und ihre Anwendung ist daher nicht ratsam.6
Ausnahmsweise können HG mit einer sehr auffälligen Schilddrüsenüberfunktionskomponente oder GD mit begleitenden gastrointestinalen Unverträglichkeiten (Übelkeit und Erbrechen) die Notwendigkeit einer Differenzialdiagnose zwischen ihnen nahelegen. Tabelle 4 zeigt die wichtigsten Unterschiede. Wenn die Hyperthyreose über das erste Schwangerschaftstrimester hinaus andauert, sollte in jedem Fall eine andere Ursache als TGT vermutet werden.
Tabelle 4.Unterschiede zwischen Morbus Basedow und Hyperemesis.
Zeichen Morbus Basedow Hyperemesis Symptome einer Hyperthyreose vor der Schwangerschaft ++ – Symptome einer Hyperthyreose während der Schwangerschaft +/++ -/+ Übelkeit/Erbrechen -/+ +++ Kropf/Ophthalmopathie + – Schilddrüsenantikörper ++ – T-US Hypervaskulär Normal Familiäre Vorgeschichte von HG – + Ähnliche Symptome in früherer Schwangerschaft – + T4 T3 TT3/TT4 Verhältnis >20 T-US: Schilddrüsen-Ultraschall; HG: Hyperemesis gravidarum.
Morbus Basedow
Unter den Schilddrüsenerkrankungen ist die GD die häufigste Ursache für eine Hyperthyreose in der Schwangerschaft und tritt bei 0,1-1 % aller Schwangerschaften auf (klinische und subklinische Hyperthyreose bei 0,4 % bzw. 0,6 %).10
Der natürliche Verlauf der GD während der Schwangerschaft ist eine Verschlimmerung der Symptome während des ersten Trimesters aufgrund der additiven Wirkung der Stimulation des TSH-Rezeptors durch HCG, gefolgt von einer Besserung in der zweiten Hälfte der Schwangerschaft aufgrund der immunmodulatorischen Wirkung der Schwangerschaft und dem Wiederauftreten nach der Geburt.
Morbus Basedow in der Schwangerschaft
Die Symptome der aktiven GD in der Schwangerschaft unterscheiden sich nicht von den typischen Symptomen der Erkrankung. Einige Symptome können manchmal mit denen der Schwangerschaft selbst verwechselt werden. Das mögliche Vorhandensein von Augenzeichen und Struma trägt zur Klärung der Erkrankung bei, und Hormonmessungen ermöglichen die Diagnose.
Behandlung der Basedow-Krankheit in der Schwangerschaft
Bekanntlich gibt es drei mögliche Therapieansätze für die Basedow-Krankheit bei nicht schwangeren Frauen: 131I, Operation oder medikamentöse Behandlung mit ATDs. Von diesen drei Möglichkeiten ist die Verabreichung von 131I in der Schwangerschaft wegen der Gefahr von Missbildungen kontraindiziert7 , so dass nur die Thyreoidektomie oder die Verwendung von ATDs in Frage kommen. Ein chirurgischer Eingriff sollte nur in Ausnahmefällen durchgeführt werden, wie weiter unten erläutert wird.
Medizinische Behandlung. Schilddrüsenmedikamente
Für die medikamentöse Behandlung der GD in der Schwangerschaft galt Propylthiouracil (PTU) bis vor einigen Jahren als die Behandlung der Wahl im Vergleich zu Methimazol/Carbimazol (MM/CM).26 Dieses Konzept beruhte auf einigen Studien, die auf eine minimale Plazentaübertragung von PTU im Vergleich zu MM/CM27 und auf die teratogenen Wirkungen von MM/CM hinwiesen. Heute weiß man, dass beide ATDs die Plazenta passieren und daher die gleiche Chance haben, den Fötus zu beeinträchtigen und eine fetale Hypothyreose zu verursachen.26
Außerdem war die Rolle von MM/CM beim Auftreten von Aplasia cutis und Choanal- und Ösophagusatresie beim Fötus zusammen mit einigen anderen Fehlbildungen, die allgemein als „Methimazolembryopathie“ bezeichnet werden,28 sehr umstritten,29-31 und diese Fehlbildungen wurden in einigen Fällen auf die schädlichen Auswirkungen der Hyperthyreose selbst zurückgeführt. Neuere Studien32,33 zeigen jedoch, dass MM/CM im Gegensatz zu PTU teratogene Wirkungen hat.
Andererseits wurde in den letzten Jahren über Fälle von fulminanter toxischer Hepatitis bei Patienten, die mit PTU behandelt wurden, berichtet,34,35 mit Prävalenzraten von 0,1 % bis 0,5 % und einer hohen Sterblichkeitsrate (25-50 %).10,36 Es wurden sogar Fälle von neonataler Hepatitis bei Neugeborenen von Müttern, die mit PTU behandelt wurden, berichtet.37,38
Wir stehen also vor einem Dilemma: Einerseits scheint klar anerkannt zu sein, dass MM/CM ein Missbildungsrisiko birgt, und andererseits, dass PTU tödliche Komplikationen verursachen kann.
Angesichts dieser Alternative haben einige Autoren bei Frauen mit GD eine Ablationstherapie vor der Schwangerschaft empfohlen.39 Diese Lösung löst das Problem jedoch kaum, da Frauen mit GD in den meisten Fällen keine Schwangerschaft planen. Andererseits verhindert diese Maßnahme nicht eine eventuelle fetale Hyperthyreose (Fhyper) aufgrund des Fortbestehens hoher Konzentrationen von schilddrüsenstimulierenden Antikörpern (TSI), die eine medizinische Behandlung erfordern, was das Problem erneut aufwirft.
Aus diesem Grund hat die ATA Kriterien für die Verwendung von PTU in der Allgemeinbevölkerung und bei Schwangeren festgelegt.40 Für die Schwangerschaft rät die ATA von der Verwendung von MM/CM im ersten Trimester der Schwangerschaft (der Organogeneseperiode) ab und empfiehlt die Verwendung von PTU. Nach der 12. Schwangerschaftswoche sollte PTU wegen des Risikos einer Lebererkrankung abgesetzt werden, und die GD-Kontrolle sollte mit MM/CM fortgesetzt werden. Außerhalb der Schwangerschaft wird die Verwendung von PTU nur unter zwei Umständen empfohlen: erstens, wenn ein Schilddrüsensturm auftritt, und zweitens, wenn durch MM/CM induzierte unerwünschte Wirkungen vorliegen.
Um eine Verzögerung des Beginns der Behandlung mit PTU zu vermeiden, ist es ratsam, dass Frauen mit GD, die möglicherweise schwanger werden können und keine Verhütungsmethode anwenden, PTU zu Hause zur Verfügung haben und angewiesen werden, die Medikation (von MM/CM auf PTU) umzustellen, sobald eine Schwangerschaft nachgewiesen ist.
Medizinische Behandlung. Klinisches Management
Wie oben beschrieben, sollte die Behandlung von GD während der Schwangerschaft im ersten Trimester aus PTU und danach aus MM/CM bestehen. Die Anfangsdosis kann zwischen 50 und 300 mg/Tag PTU in drei geteilten Dosen, 5 bis 15 mg/Tag Methimazol oder 10 bis 15 mg/Tag Carbimazol als Einzeldosis liegen.6 Es sollte immer versucht werden, die niedrigstmögliche Dosis zu verwenden.
Betablocker sollten nur vorübergehend eingesetzt werden, da ihr langfristiger Einsatz mit intrauteriner Wachstumsretardierung, Bradykardie und neonataler Hypoglykämie in Verbindung gebracht wurde.41 Darüber hinaus haben einige Autoren über vermehrte Fehlgeburten bei kombinierter Propranolol- und ATD-Behandlung berichtet.42
Bei der Anpassung der ATD-Dosis sollte versucht werden, die Schilddrüsenfunktion der Mutter nahe der Grenze zur subklinischen Überfunktion zu halten, da die fetale Schilddrüse viel empfindlicher auf die blockierende Wirkung von ATDs reagiert. Tatsächlich ist das Vorhandensein von nachweisbarem TSH ein Anzeichen dafür, dass die ATD-Dosis verringert werden sollte.10,43
Die Schilddrüsenerkrankung während der Schwangerschaft zeigt einen sehr dynamischen Verlauf, so dass bis zu 20-30 % der Patientinnen einen Grad der Kontrolle erreichen, der das Absetzen der ATD im letzten Trimester der Schwangerschaft ermöglicht.44 Die Verwendung eines kombinierten Schemas (ATDs und THs) zur Behandlung von GD ist in der Schwangerschaft absolut kontraindiziert, da es zu einer fetalen Hypothyreose (Fhypo) führt.6,43
Chirurgie
Was den Einsatz von Chirurgie zur Kontrolle von GD bei Schwangeren betrifft, so sind sich die verschiedenen Konsense und klinischen Leitlinien6,7,43 darin einig, sie nur zu empfehlen, wenn die folgenden Fälle auftreten:
- 1
Nebenwirkungen auf ATDs, die deren Einsatz verhindern.
- 2
Die Notwendigkeit hoher ATD-Dosen.
- 3
Nichtbeachtung der medizinischen Behandlung durch den Patienten.
Außerdem empfehlen die italienischen Leitlinien43 eine Operation bei ausgedehnter mütterlicher Struma mit Atemwegskompression.
Wenn eine Operation durchgeführt wird, ist der beste Zeitpunkt ab dem zweiten Trimester. Dies rechtfertigt den Einsatz von Betablockern und Natriumjodid (50-100 mg/Tag)45 für einen kurzen Zeitraum (10-14 Tage) bei schwangeren Frauen mit GD als Vorbereitung auf die Operation. Wie bereits erwähnt, sollte eine Langzeitbehandlung mit Betablockern vermieden werden. Vorsicht ist auch geboten, wenn Kaliumjodid verabreicht wird, um die Entwicklung eines Kropfes und/oder einer Fhypo zu verhindern.
Die Operation bewirkt eine tiefgreifende Veränderung der Situation. Einerseits wird die Hyperthyreose bei der Schwangeren behoben, andererseits wird bei der Mutter eine Hypothyreose induziert, die eine schnelle Substitution und eine regelmäßige TSH-Kontrolle erfordert. Auch die TSI-Werte sollten kontrolliert und die fetale Hyperthyreose bei Bedarf überwacht werden.
Veränderungen der Schilddrüsenautoimmunität während der Schwangerschaft
Einige Autoren haben zumindest in einigen Fällen gezeigt, dass sich die funktionelle Aktivität von Antikörpern gegen den TSH-Rezeptor von einer stimulierenden zu einer hemmenden oder blockierenden Aktivität verändert.46,47 Das bedeutet, dass die Schwangerschaft nicht nur die Autoantikörperspiegel, sondern auch ihr funktionelles Profil verändert. Dieses Konzept impliziert, dass sich GD in der Schwangerschaft nicht nur zu einer normalen Funktion, sondern sogar zu einer Unterfunktion entwickeln kann, und zwar aufgrund dieser Veränderung der stimulierenden und blockierenden Aktivität, wie in einigen Fällen berichtet wurde.48 Das heißt, dass GD in der Schwangerschaft ein veränderlicher Prozess ist, der eine ständige und regelmäßige Überwachung erfordert und der nicht vernachlässigt werden sollte, selbst wenn eine Situation scheinbarer Remission erreicht wurde, die keine ATDs erfordert.
Messung der schilddrüsenstimulierenden Antikörper in der Schwangerschaft
Um die Auswirkungen möglicher TSI-Autoantikörper auf die fetale Schilddrüse zu verhindern, veröffentlichte die ETA 199849 Kriterien, die die Indikationen für die TSI-Messung in der Schwangerschaft in Abhängigkeit von den Merkmalen der GD bei der Mutter festlegen (Tabelle 5).
Tabelle 5.Indikationen für die Messung des TSI gemäß der European Thyroid Association.
(I) Euthyreote Frau mit GD, die vor der Schwangerschaft medikamentös behandelt wurde
– Keine Messung
(II) Euthyreote Frau mit GD, die nach131I oder Operation geheilt wurde
– TSI frühzeitig messen: wenn positiv, Überwachung der fetalen Hyperthyreose
– TSI im dritten Trimester messen (wenn positiv im ersten Trimester): wenn positiv, Überwachung der neonatalen Hyperthyreose
(III) Frau, die während der Schwangerschaft wegen GD behandelt wird
– TSI im dritten Trimester messen, wenn positiv, Überwachung der neonatalen Hyperthyreose
GD: Morbus Basedow.
Quelle: Laurberg et al.49
In Fällen, in denen GD vor der Schwangerschaft durch eine medizinische Behandlung geheilt wurde, gilt die Immunerkrankung als behoben, und eine TSI-Messung ist nicht erforderlich.
Wenn GD durch eine Ablationstherapie (Operation oder Strahlentherapie) behoben wird, kann die Immunerkrankung fortbestehen. Die TSI-Werte werden in der Regel 12-18 Monate nach der Operation negativ. Nach einer 131I-Ablationstherapie steigen die Werte in den ersten Monaten zunächst an und nehmen dann ab, obwohl sie bis zu fünf Jahre lang hoch bleiben können.50 Das bedeutet, dass eine langfristige Empfängnisverhütung beibehalten werden muss, um einen möglichen Fhyper nach 131I zu verhindern. Daher ist bei Frauen mit Kinderwunsch und hohen TSI-Titern eine Operation der 131I-Behandlung vorzuziehen. In all diesen Fällen sollten die TSI-Werte frühzeitig bestimmt werden, um das potenzielle HF-Risiko abzuschätzen, und sie sollten im dritten Trimester erneut gemessen werden, um festzustellen, ob sie weiterhin positiv sind und somit ein Risiko für eine neonatale Hyperthyreose besteht.
Im Falle einer aktiven GD während der Schwangerschaft wird das potenzielle Fhyper-Risiko durch die Behandlung der Mutter mit ATDs kontrolliert. Es wird jedoch als ratsam erachtet, die TSI am Ende der Schwangerschaft zu testen, um das Risiko einer neonatalen Hyperthyreose abzuschätzen.
Die ATA6 rät zu einer Testung bei etwa 20-24 Wochen und gibt sehr viel allgemeinere Empfehlungen:
- –
Mutter mit aktiver Hyperthyreose.
- –
Vorgeschichte der Behandlung mit 131I.
- –
Vorangegangene Thyreoidektomie.
- –
Vorangegangenes Neugeborenes mit Hyperthyreose.
Graves-Krankheit beim Fötus
Es ist zu bedenken, dass die fetale Schilddrüse ab der 20. Woche reif ist und daher auf die gleichen Einflüsse (ATDs und TSI) wie die erwachsene Schilddrüse reagieren kann. Aus diesem Grund können sowohl Fhypo als auch Fhyper im Rahmen einer GD in der Schwangerschaft auftreten.
Fetale Hypothyreose
Fhypo tritt in der Regel aufgrund einer relativen ATD-Überdosierung auf, die bei der Mutter eine normale Funktion aufrechterhalten kann, beim Fötus jedoch eine deutliche Unterfunktion verursacht.
Suggestive klinische Anzeichen
Klinisch kann der Verdacht auf eine fetale Struma im geburtshilflichen Ultraschall und in der Entwicklung eines Polyhydramnios bei einer mit ATDs behandelten Schwangeren begründet sein.
Das Vorhandensein einer fetalen Struma ist unabhängig von funktionellen Aspekten aufgrund ihres Masseneffekts ein Alarmsignal51 (Abb. 1). Es sollte berücksichtigt werden, dass eine Schilddrüsenvergrößerung eine Hyperextension des fetalen Nackens verursacht, die wiederum die intrauterine fetale Mobilität beeinträchtigt und infolgedessen zu einer abnormalen Präsentation bei der Geburt führt (Schulterdystokie, Steißlage usw.). Selbst wenn diese Hyperextension eine adäquate Schädellage des Fötus nicht verhindert, verhindert sie eine adäquate Beugung des fetalen Halses bei der Entbindung, was zu einer Gesichtslage führt. All diese Situationen erfordern die Durchführung eines Kaiserschnittes. Dies ist jedoch nicht die Hauptkomplikation, denn die Kompression, die die Struma auf die unreifen Trachealknorpel des Fötus ausübt, kann eine Kompression der Trachea und der Speiseröhre verursachen. Dies führt zu einer Obstruktion der Atemwege mit dem damit verbundenen Risiko einer Asphyxie. Außerdem wird durch die Ösophaguskompression das Schlucken von Fruchtwasser beeinträchtigt, was zu einer Flüssigkeitsansammlung und der Entwicklung von Polyhydramnion führt. Dies begünstigt Frühgeburten, die Hauptursache für neonatale Morbidität und Mortalität.
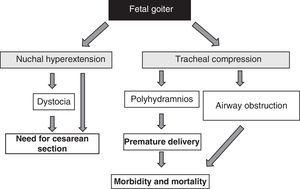 Abbildung 1.
Abbildung 1.Folgen der Kropfentwicklung beim Fötus.
(0.1MB).Diagnose
Das einzige völlig zuverlässige Verfahren zur Bestätigung eines Fhypo-Verdachts ist die Messung des fetalen TH-Spiegels mittels Chordozentese. Dieses Verfahren ist nicht frei von Komplikationen (es ist mit einem 2%igen Risiko des fetalen Todes verbunden52) und ist komplexer als eine einfache Fruchtwasseruntersuchung. Die Messung der fetalen TH-Werte im Fruchtwasser ist jedoch nicht zuverlässig und korreliert nicht mit der Messung im fetalen Blut.53 Es ist zu bedenken, dass THs mütterlichen Ursprungs im Fruchtwasser gefunden werden können.54 Gemäß den verschiedenen Leitlinien6,43 sollte eine Chordozentese nur dann durchgeführt werden, wenn bei einem Fötus, dessen Mutter ATDs einnimmt, eine Struma festgestellt wird und eine sichere Diagnose von Fhyper oder Fhypo nicht gestellt werden kann, und zwar immer in einem erfahrenen Zentrum.
Anstelle dieses Ansatzes wurde kürzlich die Messung der Verbindung W vorgeschlagen, die aus dem Metabolismus fetaler THs resultiert. Anders als bei Erwachsenen folgt der Metabolismus von THs beim Fötus dem Sulfo-Konjugationsweg zur Bildung von Dijodthyroninsulfat; diese Verbindung wird wiederum in der Plazenta und der Uteruswand methyliert, bevor sie in den mütterlichen Kreislauf gelangt und Verbindung W bildet. Diese Verbindung wird bei allen schwangeren Frauen ab der Entwicklung der fetalen Schilddrüsenfunktion gefunden und nimmt während der Schwangerschaft allmählich zu, um nach der Entbindung zu verschwinden. Sie wurde daher als Marker für die fetale Schilddrüsenfunktion vorgeschlagen.55 Vor diesem Hintergrund kann ein unzureichender Anstieg der W-Verbindung bei einer mit ATD behandelten Schwangeren auf die Entwicklung einer Fhypo hindeuten.56 Allerdings handelt es sich hierbei vorerst nur um eine quasi-experimentelle Methode.
Behandlung
Die erste Maßnahme, die ergriffen werden muss, ist das Absetzen der ATD. Wegen der Latenz der ATD-Effekte nach dem Absetzen ist jedoch auch ein TH-Ersatz erforderlich, bis sich die fetale Schilddrüse vollständig erholt hat. Die Plazentapassage von THs ist begrenzt, daher sollten sie auf dem intra-amniotischen Weg verabreicht werden. Dieser Weg ist zwar invasiv, aber viel sicherer als die Chordozentese, und das Risiko einer Fehlgeburt nach der ersten Hälfte der Schwangerschaft ist minimal.57
Für die intra-amniotische Behandlung des Fötus mit T4 gibt es kein etabliertes Behandlungsschema, und die Daten in der Literatur sind recht widersprüchlich.53,58,59 Ein kürzlich durchgeführter Überblick51 über die bisher gemeldeten Fälle kam zu dem Schluss, dass die durchschnittliche Dosis bei etwa 279μg Levothyroxin einmal wöchentlich (über einen Zeitraum von einer bis sechs Wochen) liegt. Dies scheint die fetale Struma 0,5-2,5 Wochen nach der ersten Dosis rückgängig zu machen. In einigen Fällen wurden wiederholte TH-Messungen durchgeführt, während in anderen Fällen das Verschwinden der Struma nur per Ultraschall überwacht wurde.
Fetale Hyperthyreose
Fhyper ist eine seltene Komplikation und kann bei bis zu 1-2 % der Babys von Müttern mit aktueller oder früherer GD auftreten, obwohl es sich möglicherweise um eine unterdiagnostizierte Erkrankung handelt.60,61
Die Entwicklung von Fhyper kann, abgesehen von den sehr seltenen Fällen von TSH-Rezeptor-Mutationen,62 das Ergebnis einer schlecht kontrollierten GD bei einer schwangeren Frau sein oder, was noch häufiger vorkommt, bei einer schwangeren Frau mit GD, die vor der Schwangerschaft durch eine Ablationstherapie geheilt wurde und weiterhin hohe TSI-Werte aufweist. Die Indikationen für die Messung des TSI zur Bestimmung des Fhyper-Risikos wurden bereits erörtert. TSI-Werte, die 3- oder 5-fach höher sind als normal6,63, bergen ein Fhyper-Risiko.
Suggestive klinische Anzeichen
Das Auftreten einer fetalen Struma ist eines der frühesten Merkmale. Eine fetale Bradykardie, ein fortgeschrittenes Knochenalter, eine allgemeine Wachstumsretardierung und eine Kraniosynostose können ebenfalls auftreten.64 Bei schwereren Formen kann es zu einer Herzinsuffizienz mit fetalem Hydrops oder einer gestörten Reifung des zentralen Nervensystems mit geistiger Retardierung kommen. Schließlich kann es zu einer Frühgeburt kommen.65
Diagnose
Die oben genannten Anzeichen sind nicht eindeutig; Tachykardie tritt nicht immer auf, und das Vorhandensein einer Struma im Ultraschall ist ein häufiger Befund bei Fhypo. Wenn Zweifel bestehen, ob es sich um Fhypo aufgrund der Wirkung von ATDs oder um Fhyper aufgrund schlechter mütterlicher Kontrolle handelt, haben einige Autoren ein auf Ultraschalldaten basierendes Scoring-System vorgeschlagen66 (Tabelle 6). Im Zweifelsfall sollten die fetalen THs mittels Chordozentese gemessen werden, wie im Abschnitt Fhypo beschrieben. Compound W (zuvor besprochen) könnte zu diesem Zweck in Zukunft hilfreich sein.
Tabelle 6.Ultraschall-Scoring zur Unterscheidung von Hyperthyreose und Hypothyreose bei fetaler Struma.
Ultraschallmerkmale Punkte Fetale Herzfrequenz Tachykardie 1 Normal 0 Großvaskularisation Zentral 1 Peripher oder nicht vorhanden 0 Fetale Bewegungen Normal 1 Erhöht 0 Knochen Reifung Beschleunigt -1 Normal 0 Verzögert 1 Score-Interpretation ≥2 legt nahe Hyperthyreose Abgeleitet von Huel et al.66Behandlung
Die Behandlung sollte auf ATDs basieren. Im Gegensatz zu Fhypo sollte die Behandlung in diesem Fall nicht intra-amniotisch erfolgen, da ATDs die Plazenta ungehindert passieren. Im Falle von Fhyper bei einer schwangeren Frau mit schlecht kontrollierter GD ist nur eine Anpassung der Behandlung bei der Mutter erforderlich. Wenn dagegen die Mutter dank einer früheren Ablationstherapie eine normale Funktion hat und nur der Fötus eine Überfunktion aufweist, sollte MM/CM der Mutter mit einer Dosis von 10-20 mg/Tag verabreicht werden. Die Behandlung sollte alle 4-5 Tage anhand der fetalen Herzfrequenz und des Verlaufs der Struma überwacht werden, um den Fötus nicht zu überdosieren und eine Fhypo zu verursachen.10
Wenn die Mutter bei der Verabreichung von ATDs eine Hypothyreose entwickelt, sollte sie Levothyroxin erhalten, das die Plazenta kaum passiert und daher die Hypothyreose ausgleicht, ohne den Fötus zu beeinträchtigen. Dies ist die einzige Situation, in der das kombinierte Schema angewendet werden kann.
Graves-Krankheit beim Neugeborenen
Bei Neugeborenen kann GD während der Schwangerschaft sowohl eine Hyperthyreose als auch eine Hypothyreose verursachen.
Neonatale Hyperthyreose
Diese kann bei 1-5% der Babys von Schwangeren mit aktiver GD10 und hohen TSI-Titern im letzten Trimester auftreten. Der Fötus behält seine normale Funktion während der Schwangerschaft aufgrund der Wirkung der von der Mutter aufgenommenen ATDs bei. ATDs haben eine Halbwertszeit von 24-72 Stunden und wirken nach diesem Zeitraum nicht mehr auf die fetale Schilddrüse. Dieser wird dem mütterlichen TSI ausgesetzt, das bis zu 12 Wochen nach der Entbindung bestehen bleiben kann.
Eine Schilddrüsenüberfunktion und sogar eine Herzinsuffizienz, die einige Tage nach der Entbindung bei einem zunächst asymptomatischen Neugeborenen auftritt, sind die Folge.
Dieser Zustand kann auch bei Neugeborenen von Müttern auftreten, die vor der Schwangerschaft eine Ablationstherapie erhalten haben und weiterhin erhöhte TSI-Werte aufweisen, bei denen eine nicht diagnostizierte Fhyper aufgetreten ist. In diesen Fällen ist die neonatale Hyperthyreose eine Fortsetzung von Fhyper; die Neugeborenen zeigen bei der Geburt eine schwere Beteiligung, ein niedriges Gewicht und eine beschleunigte Knochenreifung.
Die Behandlung sollte aus der Verabreichung von MM/CM in Dosen von 0,5-1mg/kg Körpergewicht/Tag und Propranolol 2mg/kg Körpergewicht/Tag36 bestehen, je nach klinischem Verlauf und unter Berücksichtigung der Tatsache, dass es sich um eine vorübergehende Situation handelt. Es sollte beachtet werden, dass TSI ihr funktionelles Profil ändern können, so dass sie zu Rezeptorblockern werden und eine Hypothyreose entwickeln.
Sekundäre neonatale Hypothyreose
Bei Säuglingen von Müttern mit schlecht kontrollierter GD kann festgestellt werden, dass erhöhte TH-Spiegel, denen sie während der Schwangerschaft ausgesetzt waren, die Unterdrückung der TSH-Sekretion verursacht haben, was zu einer sekundären Hypothyreose bei der Geburt führt.67 Diese Situation kann vorübergehend oder endgültig sein, da die TSH-Sekretion in der Hypophyse dauerhaft beeinträchtigt ist.
Neugeborene sollten Levothyroxin erhalten, gefolgt von regelmäßigen Untersuchungen, bis sich die TSH-Sekretion wieder erholt hat.
Eine vorübergehende neonatale Hypothyreose aufgrund der Persistenz mütterlicher Autoantikörper, die den RSH-Rezeptor blockieren, kann ebenfalls auftreten.68
Graves-Krankheit bei Frauen nach der Geburt
Eine zuvor kontrollierte Schilddrüsenunterfunktion, entweder vor oder nach der Schwangerschaft, kann nach der Entbindung erneut auftreten. Die Rezidivrate nach der Entbindung kann bis zu 84 % betragen, im Vergleich zu 56 % bei Frauen ohne Schwangerschaft.69 Es wird daher empfohlen, die mütterlichen THs sechs Wochen nach der Entbindung und bis zu einem Jahr lang zu messen.10
Wenn GD wieder auftritt, ist eine medizinische Behandlung mit MM/CM erforderlich. Obwohl ATDs in die Muttermilch sezerniert werden, birgt ihre Verabreichung während der Stillzeit kein Risiko, und bis zu 20-30 mg MM/CM können ohne Auswirkungen auf die Schilddrüse von Neugeborenen eingenommen werden.70 ATDs sollten in geteilten Dosen und immer nach Ende der Milchaufnahme eingenommen werden.
Es wurde vermutet, dass TSI in der Muttermilch durch das unreife Magen-Darm-Epithel des Säuglings in den allgemeinen Kreislauf des Neugeborenen gelangen und eine neonatale Hyperthyreose verursachen oder verlängern könnten. Es gibt jedoch noch keine schlüssigen Beweise dafür, dass dies der Fall ist.71
Addendum
Nach der Einreichung dieses Manuskripts hat die North American Society of Endocrinology neue klinische Praxisrichtlinien zum Management von Schilddrüsenfehlfunktionen während der Schwangerschaft und nach der Geburt herausgegeben (J Clin Endocrinol Metab 2012; 97: 2543-2565). Die Empfehlungen im Abschnitt über Hyperthyreose in der Schwangerschaft unterscheiden sich nicht wesentlich von denen, die in dieser Übersichtsarbeit diskutiert werden.
Interessenkonflikte
Der Autor erklärt, dass er keine Interessenkonflikte hat.
- –